Ene
31
¡La curiosidad humana! Siempre queriéndo saber
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Aquellos filósofos de la naturaleza ~
Clasificado en Aquellos filósofos de la naturaleza ~
 Comments (0)
Comments (0)
Hubo que descubrir la historia antes de explorarla. Los mensajes del pasado se transmitían primero a través de las habilidades de la memoria, luego de la escritura y, finalmente, de modo explosivo, en los libros. El insospechado tesoro de reliquias que guardaba la tierra se remontaba a la prehistoria. El pasado se convirtió en algo más que un almacén de mitos y leyendas o un catálogo de lo familiar.
de explorarla. Los mensajes del pasado se transmitían primero a través de las habilidades de la memoria, luego de la escritura y, finalmente, de modo explosivo, en los libros. El insospechado tesoro de reliquias que guardaba la tierra se remontaba a la prehistoria. El pasado se convirtió en algo más que un almacén de mitos y leyendas o un catálogo de lo familiar.
¡Qué tiempos!
Hoy los tiempos han cambiado y, todo aquello pasó a la historia. Llegaron los ordenadores con Internet, el mundo dio un vuelco de 360 grados, las Sociedades han cambiado y, no estoy seguro de que sea para mejor.
Algunos mensajes que todavía podemos leer en algunos perdidos lugares de la geografía española (el de arriba es el mejor ejemplo), ¡son tan inocentes! que nos remontan a otros tiempos, a otro mundo que, aunque nos parezca mentira, es el mundo nuestro, el mismo que habitamos ahora y la diferencia está marcada por el paso del tiempo y la evolución. Es fácil pasar de lo cotidiano y entrañable al átomo invisible que está, sin estar, presente en todo y en todos.
y la diferencia está marcada por el paso del tiempo y la evolución. Es fácil pasar de lo cotidiano y entrañable al átomo invisible que está, sin estar, presente en todo y en todos.
Nuevos mundos terrestres y marinos, riquezas de continentes remotos, relatos de viajeros aventureros que nos traían otras formas de vida de pueblos ignotos y lejanos, abrieron perspectivas de progreso y novedad. La sociedad, la vida diaria del hombre en comunidad, se convirtió en un nuevo y cambiante escenarios de descubrimientos. Muy atrás quedaron aquellos tiempos en que la vida que pululaba por el planeta era rudimentaria, sin consciencia. El nacimiento de la Humanidad, lleno el mundo de pensamientos.
y cambiante escenarios de descubrimientos. Muy atrás quedaron aquellos tiempos en que la vida que pululaba por el planeta era rudimentaria, sin consciencia. El nacimiento de la Humanidad, lleno el mundo de pensamientos.
Cuando en el Neolítico se descubrió la rueda y el arado, ¿Qué salto hacia el futuro no daría la Humanidad?
Aquí, como sería imposible hacer un recorrido por el ámbito de todos los descubrimientos de la Humanidad, me circunscribo al ámbito de la física, y, hago un recorrido breve por el mundo del átomo que es el tema de hoy, sin embargo, sin dejar de mirar al hecho cierto de que, TODA LA HUMANIDAD ES UNA, y, desde luego, teniendo muy presente que, todo lo que conocemos es finito y lo que no conocemos infinito. Es bueno tener presente que intelectualmente nos encontramos en medio de un océano ilimitado de lo inexplicable. La tarea de cada generación es reclamar un poco más de terreno, añadir algo a la extensión y solidez de nuestras posesiones del saber (eso nos aconseja Wheeler).
luego, teniendo muy presente que, todo lo que conocemos es finito y lo que no conocemos infinito. Es bueno tener presente que intelectualmente nos encontramos en medio de un océano ilimitado de lo inexplicable. La tarea de cada generación es reclamar un poco más de terreno, añadir algo a la extensión y solidez de nuestras posesiones del saber (eso nos aconseja Wheeler).
Como decía Einstein: “El eterno misterio del mundo es su comprensibilidad.”
Ahora , amigos, hablemos del átomo. Veamos, para comenzar como es, la imagen de un átomo en movimiento (aunque aquí lo veamos estático, utilizad la imaginación).
, amigos, hablemos del átomo. Veamos, para comenzar como es, la imagen de un átomo en movimiento (aunque aquí lo veamos estático, utilizad la imaginación).
“Ha supuesto un gran avance en el campo de la Física. Científicos de la Universidad de Otago, en Nueva Zelanda, desarrollaron una técnica para aislar sistemáticamente y capturar un átomo en rápido movimiento neutral, y también han conseguido en primicia ver y fotografiar este átomo por primera vez, lo que han denominado desde
la universidad como el “sueño de los científicos.
La captura del átomo de rubidio 85 es el resultado de un proyecto de investigación de tres años de duración financiado por la Fundación para la Investigación, Ciencia y Tecnología, y ha suscitado el interés en la comunidad científica internacional por las nuevas investigaciones que podrán surgir de este hito.”
¡Hay tantos mundos dentro de este nuestro! Sí, dentro de cada Mente existe un mundo… ¡Tan diferentes!
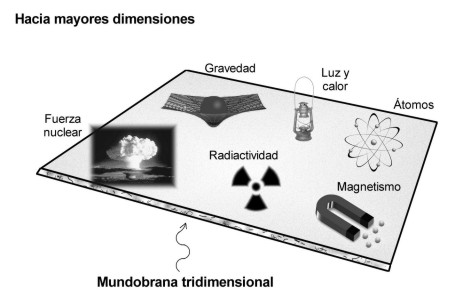
De lo Grande a lo Pequeño
El 6 de Agosto de 1945 el mundo recibió estupefacto desde Hiroshima la noticia de que el hombre había desembarcado en el oscuro continente del átomo. Sus misterios habrían de obsesionar al siglo XX. Sin embargo, el “átomo” había sido más de dos mil años una de las más antiguas preocupaciones de los filósofos naturales. La palabra griega átomo significa unidad mínima de materia, que se suponía era indestructible. Ahora el átomo era un término de uso corriente, una amenaza y una promesa sin precedentes.
el átomo era un término de uso corriente, una amenaza y una promesa sin precedentes.
Leucipo (c. 450-370 a.C.), filósofo griego. Es reconocido como creador de la teoría atómica de la materia, más tarde desarrollada por su discípulo, el filósofo griego Demócrito. Según esta teoría, toda materia está formada por partículas idénticas e indivisibles llamadas átomos.
teoría, toda materia está formada por partículas idénticas e indivisibles llamadas átomos.
Leucipo fue un griego legendario. Sin embargo, fue su discípulo Demócrito el que dio al atomismo su forma clásica como filosofía: “la parte invisible e indivisible de la materia”, se divertía tanto con la locura de los hombres que era conocido como “el filósofo risueño” o “el filósofo que ríe”. No obstante fue uno de los primeros en oponerse a la idea de la decadencia de la Humanidad a partir de una Edad de Oro mítica, y predicó sobre una base de progreso. Si todo el Universo estaba compuesto solamente por átomos y vacío, no sólo no era infinitamente complejo, sino que, de un modo u otro, era inteligible, y seguramente el poder del hombre no tenía límite.
clásica como filosofía: “la parte invisible e indivisible de la materia”, se divertía tanto con la locura de los hombres que era conocido como “el filósofo risueño” o “el filósofo que ríe”. No obstante fue uno de los primeros en oponerse a la idea de la decadencia de la Humanidad a partir de una Edad de Oro mítica, y predicó sobre una base de progreso. Si todo el Universo estaba compuesto solamente por átomos y vacío, no sólo no era infinitamente complejo, sino que, de un modo u otro, era inteligible, y seguramente el poder del hombre no tenía límite.
Lo cierto es que, nuestro futuro es un libro en blanco y, lo que se pueda leer en él, aún no está escrito pero
… ¿dependerá de nosotros?
Lucrecio (c. 95 a.C. -c. 55 a.C.) perpetuó en De rerum natura (De la naturaleza de las cosas) uno de los más importantes poemas latinos, al atomismo antiguo. Con la intención de liberar al pueblo del temor a los dioses, el poeta demostró que el mundo entero estaba constituido por vacío y átomos, los cuales se movían según sus leyes propias; que el alma moría con el cuerpo y que por consiguiente no había razón para temer a la muerte o a los poderes sobrenaturales.
temer a la muerte o a los poderes sobrenaturales.
Lucrecio decía que comprender la Naturaleza era el único modo de hallar la paz de espíritu, y, como era de esperar, los padres de la Iglesia que pregonaban la vida eterna, atacaron sin piedad a Lucrecio y este fue ignorado y olvidado durante toda la Edad Media que, como sabéis, fue la culpable de la paralización del saber de la Humanidad. Sin embargo, Lucrecio fue, una de las figuras más influyentes del Renacimiento.
fue ignorado y olvidado durante toda la Edad Media que, como sabéis, fue la culpable de la paralización del saber de la Humanidad. Sin embargo, Lucrecio fue, una de las figuras más influyentes del Renacimiento.
Así pues, en un principio el atomismo vino al mundo como sistema filosófico. Del mismo modo que la simetría pitagórica había proporcionado un marco a Copérnico, la geometría había seducido a Kepler y el círculo perfecto aristotélico hechizo a Harvey, así los “indestructibles” átomos de los filósofos atrajeron a los físicos y a los químicos. Francis Bacon observó que “la teoría de Demócrito referida a los átomos es, si no cierta, al menos aplicable con excelentes resultados al análisis de la Naturaleza”.
sistema filosófico. Del mismo modo que la simetría pitagórica había proporcionado un marco a Copérnico, la geometría había seducido a Kepler y el círculo perfecto aristotélico hechizo a Harvey, así los “indestructibles” átomos de los filósofos atrajeron a los físicos y a los químicos. Francis Bacon observó que “la teoría de Demócrito referida a los átomos es, si no cierta, al menos aplicable con excelentes resultados al análisis de la Naturaleza”.
Descartes
Descartes (1596-1650) inventó su propia noción de partículas infinitamente pequeñas que se movían en un medio que llamó éter. Otro filósofo francés, Pierre Gassendi (1592-1655), pareció confirmar la teoría de Demócrito y presentó otra versión más del atomismo, que Robert Boyle (1627-1691) adaptó a la química demostrando que los “elementos clásicos -tierra, aire, fuego y agua- no eran en absoluto elementales.
Las proféticas intuiciones de un matemático jesuita, R.G. Boscovich (1711-1787) trazaron los caminos para una nueva ciencia, la física atómica. Su atrevido concepto de “los puntos centrales” abandonaba la antigua idea de una variedad de átomos sólidos diferentes. Las partículas fundamentales de la materia, sugería Boscovich, eran todas idénticas, y las relaciones espaciales alrededor de esos puntos centrales constituían la materia… Boscovich que había llegado a estas conclusiones a partir de sus conocimientos de matemáticas y astronomía, anunció la íntima conexión entre la estructura del átomo y la del Universo, entre lo infinitesimal y lo infinito.
una nueva ciencia, la física atómica. Su atrevido concepto de “los puntos centrales” abandonaba la antigua idea de una variedad de átomos sólidos diferentes. Las partículas fundamentales de la materia, sugería Boscovich, eran todas idénticas, y las relaciones espaciales alrededor de esos puntos centrales constituían la materia… Boscovich que había llegado a estas conclusiones a partir de sus conocimientos de matemáticas y astronomía, anunció la íntima conexión entre la estructura del átomo y la del Universo, entre lo infinitesimal y lo infinito.
John Dalton
El camino experimental hacia el átomo fue trazado por John Dalton (1766-1844). Era este un científico aficionado cuáquero y autodidacta que recogió un sugestivo concepto de Lavoisier (1743-1794). Considerado una de los fundadores de la química moderna, Lavoisier, cuando definió un “elemento” como una sustancia que no puede ser descompuesta en otras sustancias por medio de ningún método conocido, hizo del átomo un útil concepto de laboratorio y trajo la teoría atómica a la realidad.
ser descompuesta en otras sustancias por medio de ningún método conocido, hizo del átomo un útil concepto de laboratorio y trajo la teoría atómica a la realidad.
Dalton había nacido en el seno de una familia de tejedores de Cumberland, localidad inglesa situada en la región de los lagos, y estuvo marcada toda su vida por su origen humilde. A los doce años ya se encontraba a cargo de la escuela cuáquera de su pueblo. Después, comenzó a ejercer la enseñanza en la vecina Kendal, y en la biblioteca del colegio encontró ejemplares de los Principia de Newton, de las Obras de la Historia Natural de Buffón, así como
ya se encontraba a cargo de la escuela cuáquera de su pueblo. Después, comenzó a ejercer la enseñanza en la vecina Kendal, y en la biblioteca del colegio encontró ejemplares de los Principia de Newton, de las Obras de la Historia Natural de Buffón, así como un telescopio reflectante de unos setenta centímetros y un microscopio doble. Dalton recibió allí la influencia de John Gough, un notable filósofo natural ciego.
un telescopio reflectante de unos setenta centímetros y un microscopio doble. Dalton recibió allí la influencia de John Gough, un notable filósofo natural ciego.
Dalton escribió a un amigo, “entiende muy bien todas las diferentes ramas de las matemáticas…Conoce por el tacto, el sabor y el olor de casi todas las plantas que crecen a casi treinta kilómetros a la redonda”. También Wordsworth elogia a Gough en su Excursión. Dalton recibió del filósofo ciego una educación básica en latín, griego y francés, y fue introducido en las matemáticas, la astronomía y todas las ciencias “de la observación”. Siguiendo el ejemplo de Gough, Dalton comenzó a llevar un registro meteorológico diario, que continuó hasta el día de su muerte.
meteorológico diario, que continuó hasta el día de su muerte.
Cuando los “disidentes” fundaron su colegio propio en Manchester, Dalton fue designado profesor de matemáticas y de filosofía natural. Halló una audiencia muy receptiva para sus experimentos en la Sociedad Literaria y Filosófica de Manchester, y presentó allí sus Hechos extraordinarios concernientes a la visión de los colores, que probablemente fue el primer trabajo sistemático sobre la imposibilidad de percibir los colores, o daltonismo, enfermedad que padecían tanto John Dalton como su hermano Jonathan. “He errado tantas veces el camino por aceptar los resultados de otros que he decidido escribir lo menos posible y solamente lo que pueda afirmar por mi propia experiencia”.
sistemático sobre la imposibilidad de percibir los colores, o daltonismo, enfermedad que padecían tanto John Dalton como su hermano Jonathan. “He errado tantas veces el camino por aceptar los resultados de otros que he decidido escribir lo menos posible y solamente lo que pueda afirmar por mi propia experiencia”.
Al final del túnel oscuro de la ignorancia, siempre nos aguarda la luz del saber pero, hay que recorrer la distancia para alcanzar el resplandor el saber.
alcanzar el resplandor el saber.
Dalton observó la aurora boreal, sugirió el probable origen de los vientos alisios, las causas de la formación de nubes y de la lluvia y, sin habérselo propuesto, introdujo mejoras en los pluviómetros, los barómetros, los termómetros y los higrómetros. Su interés por la atmósfera le proporcionó una visión de la química que lo condujo al átomo.
Newton había confiado en que los cuerpos visibles más pequeños siguieran las leyes cuantitativas que gobernaban los cuerpos celestes de mayor tamaño. La química sería una recapitulación de la Astronomía. Pero , ¿Cómo podía el hombre observar y medir los movimientos y la atracción mutua de estas partículas invisibles? En los Principios Newton había conjeturado que los fenómenos de la Naturaleza no descritos en este libro podrían “depender todos de ciertas fuerzas por las cuales las partículas de los cuerpos, debido a causas hasta ahora
, ¿Cómo podía el hombre observar y medir los movimientos y la atracción mutua de estas partículas invisibles? En los Principios Newton había conjeturado que los fenómenos de la Naturaleza no descritos en este libro podrían “depender todos de ciertas fuerzas por las cuales las partículas de los cuerpos, debido a causas hasta ahora desconocidas, se impulsan mutuamente unas hacia otras y se unen formando figuras regulares, o bien se repelen y se apartan unas de otras.”
desconocidas, se impulsan mutuamente unas hacia otras y se unen formando figuras regulares, o bien se repelen y se apartan unas de otras.”
Dalton se lanzó a la búsqueda de “estas partículas primitivas” tratando de encontrar algún medio experimental que le permitiera incluirlas en un sistema cuantitativo. Puesto que los gases eran la forma de materia más fluida, más móvil, Dalton centró su estudio en la atmósfera, la mezcla de gases que componen el aire, el cual constituyó el punto de partida de toda su reflexión sobre los átomos.
de materia más fluida, más móvil, Dalton centró su estudio en la atmósfera, la mezcla de gases que componen el aire, el cual constituyó el punto de partida de toda su reflexión sobre los átomos.
“¿Por qué el agua no admite un volumen similar de cada gas?, preguntó Dalton a sus colegas de la Sociedad Literaria y Filosófica de Manchester en 1803. “Estoy casi seguro de que la circunstancia depende del peso y el número de las partículas últimas de los diversos gases; aquellos cuyas partículas son más ligeras y simples se absorben con más dificultad, y los demás con mayor facilidad, según vayan aumentando en peso y en complejidad.”
gas?, preguntó Dalton a sus colegas de la Sociedad Literaria y Filosófica de Manchester en 1803. “Estoy casi seguro de que la circunstancia depende del peso y el número de las partículas últimas de los diversos gases; aquellos cuyas partículas son más ligeras y simples se absorben con más dificultad, y los demás con mayor facilidad, según vayan aumentando en peso y en complejidad.”


Teoría cinética de los Gases: La termodinámica se ocupa solo de variables microscópicas, como la presión, la temperatura y el volumen. Sus leyes básicas, expresadas en términos de dichas cantidades, no se ocupan para nada de que la materia esta formada por átomos. Sin embargo, la mecánica estadística, que estudia las mismas áreas de la ciencia que la termodinámica, presupone la existencia de los átomos. Sus leyes básicas son las leyes de la mecánica, las que se aplican en los átomos que forman el sistema.
formada por átomos. Sin embargo, la mecánica estadística, que estudia las mismas áreas de la ciencia que la termodinámica, presupone la existencia de los átomos. Sus leyes básicas son las leyes de la mecánica, las que se aplican en los átomos que forman el sistema.
Dalton había descubierto que, contrariamente a la idea dominante, el aire no era un vasto disolvente químico único sino una mezcla de gases, cada uno de los cuales conservaban su identidad y actuaba de manera independiente. El producto de sus experimentos fue recogido en la trascendental TABLE: Of the Relative Weights of Ultimate Particles of Gaseous and Other Bodies (“Tabla de los pesos relativos de las partículas últimas de los cuerpos gaseosos y de otros cuerpos”).
uno de los cuales conservaban su identidad y actuaba de manera independiente. El producto de sus experimentos fue recogido en la trascendental TABLE: Of the Relative Weights of Ultimate Particles of Gaseous and Other Bodies (“Tabla de los pesos relativos de las partículas últimas de los cuerpos gaseosos y de otros cuerpos”).
En las reacciones químicas, los átomos no se crean ni se destruyen, solamente cambian de distribución.
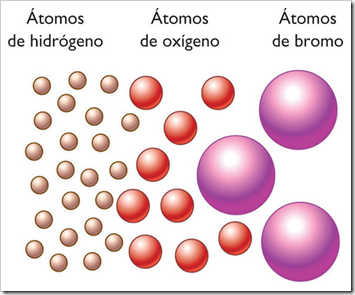
Mucho hemos avanzado desde aquellos primeros elementos que, según Empédocles, lo conformaban todo mezclados en la debida proporción. Él decía que la tierra, el agua, el aire y el fuego eran todos los elemetos del mundo físico y que todo estaba hecho de a partir de ellos. No hay que quitarle mérito a la idea germinal que nos trajo muy lejos, hasta la Tabla periódica con sus 92 elementos naturales.
Finalmente trazará un programa de investigación que él mismo resume así: Es objetivo principal de este trabajo mostrar las ventajas que reporta la determinación precisa de los pesos relativos de las partículas últimas, tanto de los cuerpos simples como de los compuestos, determinar el número de partículas simples elementales que constituyen una partícula compuesta y el número mínimo de partículas compuestas que entran en la formación de una nueva partícula compuesta.
de partículas simples elementales que constituyen una partícula compuesta y el número mínimo de partículas compuestas que entran en la formación de una nueva partícula compuesta.
Tomando al Hidrógeno como número uno, Dalton detalló en esta obra veintiuna sustancias. Describió las invisibles “partículas últimas” como diminutas bolitas sólidas, similares a balas pero mucho más pequeñas, y propuso que se les aplicaran las leyes newtonianas de las fuerzas de atracción de la materia. Dalton se proponía lograr “una nueva perspectiva de los primeros principios de los elementos de los cuerpos y sus combinaciones”, que “sin duda…con el tiempo, producirá importantísimos cambios en el sistema de la química y la reducirá a una ciencia de gran simplicidad, inteligible hasta para los intelectos menos dotados”. Cuando Dalton mostró una “partícula de aire que descansa sobre cuatro partículas de agua como una ordenada pila de metralla” donde cada pequeño globo está en contacto con sus vecinos, proporcionó el modelo de esferas y radio de la química del siglo siguiente.
sustancias. Describió las invisibles “partículas últimas” como diminutas bolitas sólidas, similares a balas pero mucho más pequeñas, y propuso que se les aplicaran las leyes newtonianas de las fuerzas de atracción de la materia. Dalton se proponía lograr “una nueva perspectiva de los primeros principios de los elementos de los cuerpos y sus combinaciones”, que “sin duda…con el tiempo, producirá importantísimos cambios en el sistema de la química y la reducirá a una ciencia de gran simplicidad, inteligible hasta para los intelectos menos dotados”. Cuando Dalton mostró una “partícula de aire que descansa sobre cuatro partículas de agua como una ordenada pila de metralla” donde cada pequeño globo está en contacto con sus vecinos, proporcionó el modelo de esferas y radio de la química del siglo siguiente.
Dalton inventó unas “señales arbitrarias como signos elegidos para representar los diversos elementos químicos o partículas últimas”, organizadas en una tabla de pesos atómicos que utilizaba en sus populares conferencias. Naturalmente, Dalton no fue el primero en emplear una escritura abreviada para representar las sustancias químicas, pues los alquimistas también tenían su código. Pero él fue probablemente el primero que utilizó este tipo de simbolismo en un sistema cuantitativo de “partículas últimas”. Dalton tomó como unidad el átomo de Hidrógeno, y a partir de él calculó el peso de las moléculas como la suma de los pesos de los átomos que la componían, creando así una sintaxis moderna para la química. Las abreviaturas actuales que utilizan la primera letra del nombre latino (por ejemplo H2O) fueron ideadas por el químico sueco Berzelius (1779-1848).
latino (por ejemplo H2O) fueron ideadas por el químico sueco Berzelius (1779-1848).

Habiendo cumplido más de 350 años, la Institución que presidiera Newton “Real Sociedad de Londres para el Avance de la Ciencia Natural” más conocida como “Royal Society”, sigue en plena forma y ostenta el respetado título de Sociedad más Antigua. ¡Si nos pudiera contar todo lo que allí se vivió”.
y ostenta el respetado título de Sociedad más Antigua. ¡Si nos pudiera contar todo lo que allí se vivió”.
La teoría del átomo de Dalton no fue recibida en un principio con entusiasmo. El gran sir Humphry Davy desestimó inmediatamente sus ideas tachándolas de “más ingeniosas que importantes”. Pero las nociones de Dalton, desarrolladas en A New System of Chemical Philosophy (1808), eran tan convincentes que en 1826 le fue concedida la medalla real. Como Dalton no olvidó nunca su origen plebeyo, permaneció siempre apartado de la Royal Society de Londres, pero fue elegido miembro, sin su consentimiento, en 1822. Receloso del tono aristocrático y poco profesional de la Sociedad, él se encontraba más a gusto en Manchester, donde realizó la mayor parte de su obra, colaboró con Charles Babage y contribuyó a fundar la Asociación Británica para el Progreso de la Ciencia, cuyo objetivo era llevar la ciencia hasta el pueblo. Los newtonianos partidarios de la ortodoxia religiosa no creían que Dios hubiera hecho necesariamente sus invisibles “partículas últimas” invariables e indestructibles. Compartían con Isaac Newton la sospecha de que Dios había utilizado su poder “para
el Progreso de la Ciencia, cuyo objetivo era llevar la ciencia hasta el pueblo. Los newtonianos partidarios de la ortodoxia religiosa no creían que Dios hubiera hecho necesariamente sus invisibles “partículas últimas” invariables e indestructibles. Compartían con Isaac Newton la sospecha de que Dios había utilizado su poder “para variar las leyes de la Naturaleza y crear mundos diversos en distintos lugares del Universo”.
variar las leyes de la Naturaleza y crear mundos diversos en distintos lugares del Universo”.
Propuso que la materia estaba hecha de partículas
Las verdaderas investigaciones sobre el átomo comenzaron en el siglo XVII, cuando los experimentos de Robert Boyle dieron nuevo impulso a la investigación de las intimidades de la materia. En 1803, el científico inglés John Dalton propuso por primera vez, la teoría de que cada elemento tiene un tipo particular de átomo y que cualquier cantidad de un mismo elemento está formada por átomos idénticos. Lo que distingue a un elemento de otro es la naturaleza de sus átomos.
impulso a la investigación de las intimidades de la materia. En 1803, el científico inglés John Dalton propuso por primera vez, la teoría de que cada elemento tiene un tipo particular de átomo y que cualquier cantidad de un mismo elemento está formada por átomos idénticos. Lo que distingue a un elemento de otro es la naturaleza de sus átomos.
El átomo indestructible de Dalton se convirtió en el fundamento de una naciente ciencia de la química, proporcionando los principios elementales, las leyes de composición constante y de proporciones múltiples y la combinación de elementos químicos en razón de su peso atómico. “El análisis y la síntesis química no van más allá de la separación de unas partículas de otras y su reunión”, insistió Dalton. “La creación o la destrucción de la materia no está al alcance de ningún agente químico. Sería lo mismo tratar de introducir un planeta nuevo en el Sistema Solar o aniquilar uno de los ya existentes que crear o destruir una partícula de Hidrógeno.” Dalton continuó usando las leyes de los cuerpos celestes visibles como indicios del Universo infinitesimal. El profético sir Humphry Davy, sin embargo, no se convencía, “no hay razón para suponer que ha sido descubierto un principio real indestructible”, afirmó escéptico.
en el Sistema Solar o aniquilar uno de los ya existentes que crear o destruir una partícula de Hidrógeno.” Dalton continuó usando las leyes de los cuerpos celestes visibles como indicios del Universo infinitesimal. El profético sir Humphry Davy, sin embargo, no se convencía, “no hay razón para suponer que ha sido descubierto un principio real indestructible”, afirmó escéptico.
Gay-Lussac
Dalton no era más que un Colón. Los Vespucios aún no habían llegado, y cuando lo hicieron trajeron consigo algunas sorpresas muy agradables y conmociones aterradoras. Entretanto, y durante medio siglo, el sólido e indestructible átomo de Dalton fue muy útil para los químicos, y dio lugar a prácticas elaboraciones. Un científico francés, Gay-Lussac, demostró que cuando los átomos se combinaban no lo hacían necesariamente de dos en dos, como había indicado Dalton, sino que podían agruparse en asociaciones distintas de unidades enteras. Un químico italiano, Avogadro (1776-1856), demostró que volúmenes iguales de gases a la misma temperatura y presión contenían el mismo número de moléculas. Un químico ruso Dmitri Mendeléiev, nos trajo la Tabla Periódica de los elementos, propuso una sugestiva “Ley periódica” de los elementos. Si los elementos estaban dispuestos en orden según su creciente peso atómico entonces grupos de elementos de características similares se repetirían periódicamente.
de moléculas. Un químico ruso Dmitri Mendeléiev, nos trajo la Tabla Periódica de los elementos, propuso una sugestiva “Ley periódica” de los elementos. Si los elementos estaban dispuestos en orden según su creciente peso atómico entonces grupos de elementos de características similares se repetirían periódicamente.
Dimitri Mendeléiev
Más tarde se trasladó a Alemania, para ampliar estudios en Heidelberg, donde conoció a los químicos más destacados de la época. A su regreso a Rusia fue nombrado profesor del Instituto Tecnológico de San Petersburgo (1864) y profesor de la universidad (1867), cargo que se vería forzado a abandonar en 1890 por motivos políticos, si bien se le concedió la dirección de la Oficina de Pesos y Medidas (1893).
ampliar estudios en Heidelberg, donde conoció a los químicos más destacados de la época. A su regreso a Rusia fue nombrado profesor del Instituto Tecnológico de San Petersburgo (1864) y profesor de la universidad (1867), cargo que se vería forzado a abandonar en 1890 por motivos políticos, si bien se le concedió la dirección de la Oficina de Pesos y Medidas (1893).
Entre sus trabajos destacan los estudios acerca de la expansión térmica de los líquidos, el descubrimiento del punto crítico, el estudio de las desviaciones de los gases reales respecto de lo enunciado en la ley de Boyle-Mariotte y una formulación más exacta de la ecuación de estado . En el campo práctico destacan sus grandes contribuciones a las industrias de la sosa y el petróleo de Rusia.
. En el campo práctico destacan sus grandes contribuciones a las industrias de la sosa y el petróleo de Rusia.
Todos recordamos cuán difícil era memorizar la tabla periódica en el colegio. Más todavía que memorizar la tabla de multiplicar. Porque, además, la tabla periódica estaba compuesta por nombres y valores extraños, poco útiles para la vida diaria. Sin embargo, algunos profesores de vocación, se valían de mil triquiñuelas para que, los niños la pudieran memorizar.
la vida diaria. Sin embargo, algunos profesores de vocación, se valían de mil triquiñuelas para que, los niños la pudieran memorizar.
Con todo, su principal logro investigador fue el establecimiento del llamado sistema periódico de los elementos químicos, o tabla periódica, gracias al cual culminó una clasificación definitiva de los citados elementos (1869) y abrió el paso a los grandes avances experimentados por la química en el siglo XX.
Aunque su sistema de clasificación no era el primero que se basaba en propiedades de los elementos químicos, como su valencia, sí incorporaba notables mejoras, como la combinación de los pesos atómicos y las semejanzas entre elementos, o el hecho de reservar espacios en blanco correspondientes a elementos aún no descubiertos como el eka-aluminio o galio (descubierto por Boisbaudran, en 1875), el eka-boro o escandio (Nilson, 1879) y el eka-silicio o germanio (Winkler, 1886).
Mendeléiev demostró, en controversia con químicos de la talla de Chandcourtois, Newlands y L. Meyer, que las propiedades de los elementos químicos son funciones periódicas de sus pesos atómicos. Dio a conocer una primera versión de dicha clasificación en marzo de 1869 y publicó la que sería la definitiva a comienzos de 1871. Mediante la clasificación de los elementos químicos conocidos en su época en función de sus pesos atómicos crecientes, consiguió que aquellos elementos de comportamiento químico similar estuvieran situados en una misma columna vertical, formando un grupo. Además, en este sistema periódico hay menos de diez elementos que ocupan una misma línea horizontal de la tabla. Tal como se evidenciaría más adelante, su tabla se basaba, en efecto, en las propiedades más profundas de la estructura atómica de la materia, ya que las propiedades químicas de los elementos vienen determinadas por los electrones de sus capas externas.
sistema periódico hay menos de diez elementos que ocupan una misma línea horizontal de la tabla. Tal como se evidenciaría más adelante, su tabla se basaba, en efecto, en las propiedades más profundas de la estructura atómica de la materia, ya que las propiedades químicas de los elementos vienen determinadas por los electrones de sus capas externas.
Tabla de elementos de Dalton, siglo XIX
Convencido de la validez de su clasificación, y a fin de lograr que algunos elementos encontrasen acomodo adecuado en la tabla, Mendeléiev «alteró» el valor de su peso atómico considerado correcto hasta entonces, modificaciones que la experimentación confirmó con posterioridad. A tenor de este mismo patrón, predijo la existencia de una serie de elementos, desconocidos en su época, a los que asignó lugares concretos en la tabla.
mismo patrón, predijo la existencia de una serie de elementos, desconocidos en su época, a los que asignó lugares concretos en la tabla.
Pocos años después (1894), con el descubrimiento de ciertos gases nobles (neón, criptón, etc.) en la atmósfera, efectuado por el químico británico William Ramsay (1852-1816), la tabla de Mendeléiev experimentó la última ampliación en una columna, tras lo cual quedó definitivamente establecida.
después (1894), con el descubrimiento de ciertos gases nobles (neón, criptón, etc.) en la atmósfera, efectuado por el químico británico William Ramsay (1852-1816), la tabla de Mendeléiev experimentó la última ampliación en una columna, tras lo cual quedó definitivamente establecida.
La sustancia más caliente de todas se creó al colisionar átomos de oro entre sí a velocidades cercanas a las de la luz. Es llamada “sopa de quarks y gluones” y alcanza unos humildes 4 trillones grados centígrados, lo que equivale a una temperatura de 250 mil veces más caliente que el interior del sol.
La disolución del indestructible átomo sólido provendría de dos fuentes, una conocida y la otra bastante nueva: el estudio de la luz y el descubrimiento de la electricidad. El propio Einstein describió este histórico movimiento como la decadencia de una perspectiva “mecánica” y el nacimiento de una perspectiva “de campo” del mundo físico, que le ayudó a encontrar su propio camino hacia la relatividad, hacia
la relatividad, hacia explicaciones y misterios nuevos.
explicaciones y misterios nuevos.
Albert Einstein tenía en la pared de su estudio un retrato de Michael Faraday (1791-1867), y ningún otro hubiera podido ser más apropiado, pues Faraday fue el pionero y el profeta de la gran revisión que hizo posible la obra de Einstein. El mundo ya no sería un escenario newtoniano de “fuerzas a distancias”, objetos mutuamente atraídos por la fuerza de la Gravedad inversamente proporcional al cuadrado de la distancia que hay entre ellos. El mundo material se convertiría en una tentadora escena de sutiles y omnipresentes “campos de fuerzas”. Esta idea era tan radical como la revolución newtoniana, e incluso más difícil de comprender para los legos en la materia.
idea era tan radical como la revolución newtoniana, e incluso más difícil de comprender para los legos en la materia.
Como he dicho tantas veces… ¡Qué bonito es saber! A mí me gustaría.
Emilio Silvera Vázquez
















 Totales: 75.659.407
Totales: 75.659.407 Conectados: 48
Conectados: 48













:format(jpg)/f.elconfidencial.com%2Foriginal%2Fd1c%2Fb60%2F633%2Fd1cb60633b738916a9a7eab75c82cf6a.jpg)