
IMPRESIÓN NO PERMITIDA - TEXTO SUJETO A DERECHOS DE AUTOR

 (1)
(1)
 (1)
(1)
 (18)
(18)
 (4)
(4)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (69)
(69)
 (206)
(206)
 (3)
(3)
 (2)
(2)
 (2)
(2)
 (8)
(8)
 (10)
(10)
 (31)
(31)
 (1)
(1)
 (2)
(2)
 (6)
(6)
 (8)
(8)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (9)
(9)
 (9)
(9)
 (4)
(4)
 (54)
(54)
 (571)
(571)
 (6)
(6)
 (1)
(1)
 (5)
(5)
 (1)
(1)
 (96)
(96)
 (31)
(31)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (11)
(11)
 (4)
(4)
 (15)
(15)
 (83)
(83)
 (3)
(3)
 (5)
(5)
 (13)
(13)
 (49)
(49)
 (1)
(1)
 (3)
(3)
 (16)
(16)
 (13)
(13)
 (10)
(10)
 (6)
(6)
 (2)
(2)
 (4)
(4)
 (1)
(1)
 (28)
(28)
 (2)
(2)
 (5)
(5)
 (3)
(3)
 (3)
(3)
 (5)
(5)
 (20)
(20)
 (1)
(1)
 (46)
(46)
 (2)
(2)
 (5)
(5)
 (43)
(43)
 (4)
(4)
 (1)
(1)
 (31)
(31)
 (2)
(2)
 (4)
(4)
 (20)
(20)
 (1)
(1)
 (1)
(1)
 (8)
(8)
 (10)
(10)
 (39)
(39)
 (5)
(5)
 (4)
(4)
 (1)
(1)
 (1)
(1)
 (65)
(65)
 (8)
(8)
 (5)
(5)
 (1)
(1)
 (5)
(5)
 (2)
(2)
 (5)
(5)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (4)
(4)
 (5)
(5)
 (1)
(1)
 (1)
(1)
 (33)
(33)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (3)
(3)
 (1)
(1)
 (1)
(1)
 (13)
(13)
 (11)
(11)
 (2)
(2)
 (3)
(3)
 (41)
(41)
 (75)
(75)
 (14)
(14)
 (31)
(31)
 (2)
(2)
 (4)
(4)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (5)
(5)
 (23)
(23)
 (6)
(6)
 (23)
(23)
 (21)
(21)
 (5)
(5)
 (6)
(6)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (6)
(6)
 (27)
(27)
 (2)
(2)
 (44)
(44)
 (2)
(2)
 (1)
(1)
 (9)
(9)
 (9)
(9)
 (14)
(14)
 (4)
(4)
 (80)
(80)
 (393)
(393)
 (37)
(37)
 (10)
(10)
 (18)
(18)
 (157)
(157)
 (15)
(15)
 (206)
(206)
 (22)
(22)
 (73)
(73)
 (89)
(89)
 (324)
(324)
 (67)
(67)
 (217)
(217)
 (21)
(21)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (9)
(9)
 (2)
(2)
 (8)
(8)
 (2)
(2)
 (5)
(5)
 (4)
(4)
 (10)
(10)
 (5)
(5)
 (4)
(4)
 (1)
(1)
 (5)
(5)
 (5)
(5)
 (2)
(2)
 (22)
(22)
 (2)
(2)
 (1)
(1)
 (4)
(4)
 (6)
(6)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (15)
(15)
 (1)
(1)
 (2)
(2)
 (4)
(4)
 (1)
(1)
 (4)
(4)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (7)
(7)
 (1)
(1)
 (1.650)
(1.650)
 (517)
(517)
 (68)
(68)
 (2)
(2)
 (9)
(9)
 (2)
(2)
 (1)
(1)
 (6)
(6)
 (16)
(16)
 (20)
(20)
 (2)
(2)
 (3)
(3)
 (1)
(1)
 (17)
(17)
 (12)
(12)
 (1)
(1)
 (3.607)
(3.607)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (21)
(21)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (6)
(6)
 (16)
(16)
 (15)
(15)
 (19)
(19)
 (2)
(2)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (1)
(1)
 (5)
(5)
 (6)
(6)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (9)
(9)
 (12)
(12)
 (4)
(4)
 (1)
(1)
 (6)
(6)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (30)
(30)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (5)
(5)
 (2)
(2)
 (1)
(1)
 (13)
(13)
 (6)
(6)
 (4)
(4)
 (1)
(1)
 (5)
(5)
 (3)
(3)
 (135)
(135)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (6)
(6)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (7)
(7)
 (39)
(39)
 (2)
(2)
 (7)
(7)
 (16)
(16)
 (2)
(2)
 (6)
(6)
 (2)
(2)
 (20)
(20)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (20)
(20)
 (1)
(1)
 (4)
(4)
 (4)
(4)
 (3)
(3)
 (1)
(1)
 (9)
(9)
 (2)
(2)
 (2)
(2)
 (6)
(6)
 (3)
(3)
 (20)
(20)
 (3)
(3)
 (8)
(8)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (7)
(7)
 (4)
(4)
 (24)
(24)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (1)
(1)
 (8)
(8)
 (28)
(28)
 (1)
(1)
 (2)
(2)
 (2)
(2)
 (5)
(5)
 (4)
(4)
 (1)
(1)
 (5)
(5)
 (1)
(1)
 (3)
(3)
 (81)
(81)
 (6)
(6)
 (11)
(11)
 (5)
(5)
 (4)
(4)
 (8)
(8)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (2)
(2)
 (1)
(1)
 (4)
(4)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (8)
(8)
 (13)
(13)
 (5)
(5)
 (1)
(1)
 (1)
(1)
 (16)
(16)
 (6)
(6)
 (2)
(2)
 (6)
(6)
 (1)
(1)
 (8)
(8)
 (19)
(19)
 (36)
(36)
 (3)
(3)
 (23)
(23)
 (11)
(11)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (6)
(6)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (20)
(20)
 (154)
(154)
 (2)
(2)
 (1)
(1)
 (5)
(5)
 (6)
(6)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (2)
(2)
 (4)
(4)
 (8)
(8)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (19)
(19)
 (1)
(1)
 (2)
(2)
 (3)
(3)
 (4)
(4)
 (1)
(1)
 (25)
(25)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (8)
(8)
 (2)
(2)
 (1)
(1)
 (11)
(11)
 (5)
(5)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (6)
(6)
 (2)
(2)
 (12)
(12)
 (34)
(34)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (9)
(9)
 (1)
(1)
 (1)
(1)
 (3)
(3)
 (3)
(3)
 (8)
(8)
 (10)
(10)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (250)
(250)
 (34)
(34)
 (3)
(3)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (22)
(22)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (4)
(4)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (6)
(6)
 (4)
(4)
 (8)
(8)
 (2)
(2)
 (1)
(1)
 (4)
(4)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (18)
(18)
 (1)
(1)
 (13)
(13)
 (15)
(15)
 (1)
(1)
 (24)
(24)
 (1)
(1)
 (2)
(2)
 (3)
(3)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (8)
(8)
 (1)
(1)
 (8)
(8)
 (7)
(7)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (2)
(2)
 (5)
(5)
 (1)
(1)
 (1)
(1)
 (6)
(6)
 (3)
(3)
 (1)
(1)
 (3)
(3)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (6)
(6)
 (3)
(3)
 (1)
(1)
 (9)
(9)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (12)
(12)
 (3)
(3)
 (5)
(5)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (2)
(2)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 (1)
(1)
 Totales: 75.287.574
Totales: 75.287.574 Conectados: 45
Conectados: 45
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en El cerebro ~
Clasificado en El cerebro ~
 Comments (0)
Comments (0)


Somos capaces de crear nuevas neuronas, incluso de adultos. Este hallazgo es relativamente nuevo, porque se pensaba que se nacía con un determinado “banco de neuronas” que iba menguando con el paso del tiempo, pero que no era posible renovar ni ampliar. Sin embargo, los últimos hallazgos en neurociencia desmontan esta creencia. El cerebro es plástico: es posible crear conexiones diferentes e incluso en algunas zonas, como es el hipocampo, se puede conseguir que nazcan nuevas neuronas, según explica el profesor Terry Sejnowski, de The Salk Institute for Biological Studies. Hay margen de maniobra con independencia de la edad.
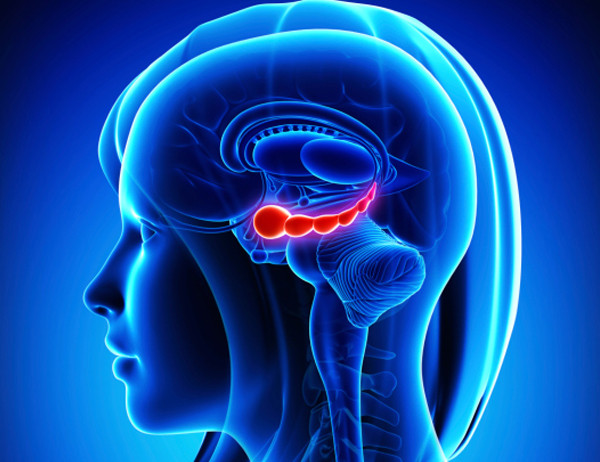
El hipocampo tiene forma de caballito de mar y es uno de los responsables de nuestra memoria y de nuestra capacidad espacial. Las investigaciones sobre esta zona del cerebro comenzaron con ratas a las que se mostraban varias imágenes que tenían que aprender a diferenciar. Cuando los roedores lo lograban se observó que en su hipocampo se habían generado nuevas neuronas. Pero si el animal dejaba de hacer el ejercicio, las neuronas jóvenes desaparecían. Si retomaba la actividad volvían a aparecer, es decir: la práctica repetida ayuda a que se generen nuevas neuronas en el hipocampo. En el caso de los humanos, si hubiera que decidir qué actividad nos permite realmente mantener joven el cerebro, Sejnowski no lo duda. El deporte es el mejor tratamiento antiedad para la masa gris.

Se sabía que practicar deporte es una manera de cuidar el cuerpo y reducir el estrés gracias a los bailes hormonales que se activan de dopamina, serotonina y noradrenalina. Pero investigaciones más recientes demuestran que el ejercicio físico mejora también la secreción del factor neurotrófico cerebral (que influye positivamente en la memoria y en un estado de ánimo más positivo) y permite que nazcan nuevas neuronas en nuestro hipocampo. A pesar de sus ventajas, no parece que exista demasiada conciencia del vínculo entre aprendizaje y deporte. Pero educar en el deporte a niños y adultos no solo ayuda a mantener la salud corporal, sino también a que el cerebro se mantenga más joven y con capacidad para generar neuronas. Como resume Sejnowski, “el gimnasio y el recreo son las partes más importantes del plan de estudios”.

Los expertos sugieren que es preciso practicar ejercicio tres veces por semana con una duración mínima de 30 minutos. Vale por ello la pena buscar un ejercicio amable, un grupo de amigos y ponerse las zapatillas deportivas. El hipocampo lo agradecerá.
 •
Using theme by Shalafi
•
Using theme by Shalafi  •
•
 XHTML 1.0
•
XHTML 1.0
•
 CSS 3
CSS 3


