Sep
6
¡Desvelar los Secretos del Universo! ¿Podremos?
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en General ~
Clasificado en General ~
 Comments (6)
Comments (6)

No debemos descartar la posibilidad de que seamos capaces de utilizar las unidades de Planck-Stoney para clasificar todo el abanico de estructuras que vemos en el universo, desde el mundo de las partículas elementales hasta las más grandes estructuras astronómicas. Este fenómeno se puede representar en un gráfico que recree la escala logarítmica de tamaño desde el átomo a las galaxias. Todas las estructuras del universo existen porque son el equilibrio de fuerzas dispares y competidoras que se detienen o compensan las unas a las otras; la atracción y la repulsión. Ese es el equilibrio de las estrellas donde la repulsión termonuclear tiende a expandirla y la atracción (contracción) de su propia masa tiende a comprimirla; así, el resultado es la estabilidad de la estrella. En el caso del planeta Tierra, hay un equilibrio entre la fuerza atractiva de la gravedad y la repulsión atómica que aparece cuando los átomos se comprimen demasiado juntos.
Sep
5
¿Qué será del Universo? ¿Hay otras dimensiones?
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astronomía y Astrofísica, General ~
Clasificado en Astronomía y Astrofísica, General ~
 Comments (1)
Comments (1)
Sep
5
¿Lo que pasó? ¿Lo que pasará? o, simple imaginación
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Lo que creemos que sabemos ~
Clasificado en Lo que creemos que sabemos ~
 Comments (1)
Comments (1)
¿Cómo podríamos resolver la estructura del Universo?
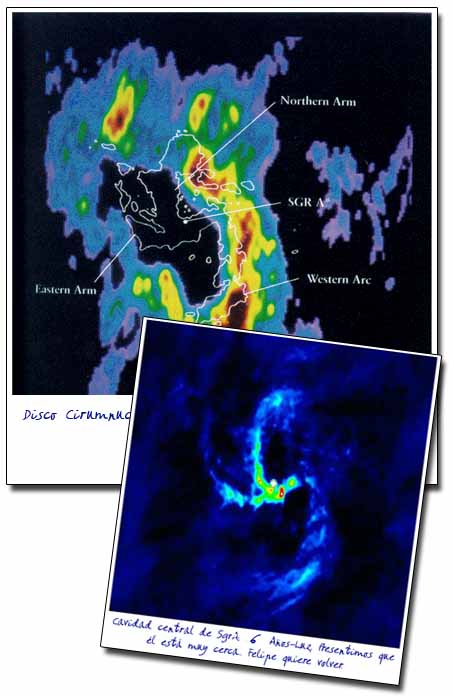
“Imaginaos ahora este instante en que los murmullos se arrastran discretamente y las espesas tinieblas llenan el navío del Universo.”
Esas palabras de Chakesperare en Enrique V (acto IV, esc. 1), nos podría valer ahora a nosotros para estrapolarlas a este tiempo y haciendo un ejercicio de imaginación, convertir esas tinieblas en la “materia oscura”, esa clase de materia que postulan los cosmólogos, que no podemos ver, que no emite radiación, que no sabemos de qué está hecha y, en realidad, tampoco sabemos donde está (sólo lo suponemos) pero, nos soluciona, de un plumazo, todos los problemas de la estructura del Universo.
“Un investigador británico propone en su nuevo trabajo que la materia oscura y la energía oscura están unidas en un solo “fluido oscuro de masas negativas”.
El astrofísico Jamie Farnes, de la Universidad de Oxford (Reino Unido), podría tener la explicación a uno de los principales misterios de la cosmología moderna: la invisibilidad del 95 % del universo, según apunta su estudio publicado este miércoles en la revista Astronomy & Astrophysics.”
Esa clase de materia “transparente” que sí emite la fuerza gravitatoria podría explicar el ritmo a grandes escalas que hemos podido observar en el comportamiento de nuestro universo y que antes de la llegada de la “materia oscura”, no sabíamos, a qué era debido… “¡ahora sí lo sabemos!”. Bueno, al menos, eso dicen algunos pero, lo tienen que demostrar.


Sitios como este, en nuestro planeta, los tenemos en multitud de lugares
No pocas veces me encuentro mirando al cielo nocturno estrellado desde la orilla del Atlántico cuya superficie brilla con millones de luces titilando al reflejar el resplendor de la Luna, la inmensidad del océano que se pierde en el horizonte y, la infinitud del firmamento me podrían hacer sentir insignificante. Sin embargo, no es así como lo siento. He dicho alguna vez que todo lo grande está hecho de cosas pequeñas, y, esa afirmación, nos da la respuesta. Formamos parte de algo muy grande: El Universo.
De las estrellas venimos y, a las estrellas tendremos que volver
Estamos en un punto, o en un nivel de sabiduría aceptable pero insuficiente, es mucho el camino que nos queda por recorrer y, como dijo el sabio, la energía necesaria para explorar la décima dimensión es mil millones de veces mayor que la energía que puede producirse en nuestros mayores colisionadores de átomos. La empresa resulta difícil para seres que, como nosotros, apenas tenemos medios seguros para escapar del débil campo gravitatorio del planeta Tierra.
Nada puede surgir de la “nada”, si surgió… ¡es porque había!
“Energías de tal calibre, que sepamos, solo han estado disponibles en el instante de la creación del Universo, en su nacimiento, en eso que llamamos Big Bang. Solamente allí estuvo presente la energía del Hiperespacio de once dimensiones y, por eso se suele decir que, cuando se logre verificar la certeza de la teoría de cuerdas, sabremos y podremos desvelar el secreto del origen del Universo.”
A los físicos teóricos siempre les resultó provechoso introducir dimensiones más altas para fisgar libremente en secretos celosamente escondidos.
Según esa nueva teoría, antes del Big Bang nuestro cosmos era realmente un universo perfecto de once dimensiones, un mundo en el que el viaje inter-dimensional era posible. Sin embargo, ese mundo decadimensional era inestable, y eventualmente se “rompió” en dos, dando lugar a dos universos separados: un universo de cuatro y otro universo de siete dimensiones.
El Universo en el que vivimos nació en ese cataclismo cósmico. Nuestro Universo tetradimensional se expandió de forma explosiva, mientras que nuestro universo gemelo de siete dimensiones se contrajo violentamente hasta que se redujo a un tamaño casi infinitesimal.

Surgió la sustancia cósmica de la que, miles de millones de años más tarde, nacería la consciencia

Eso podría explicar el origen del Big Bang, y, si la teoría es correcta, demuestra que la rápida expansión del Universo fue simple consecuencia de un cataclismo cósmico mucho mayor, la ruptura de los propios espacio y tiempo. La energía que impulsa la expansión observada del Universo se halla entonces en el colapso del espacio-tiempo de once dimensiones. Según la teoría, las estrellas y las Galaxias distantes están alejándose de nosotras a velocidades astronómicas debido al colapso original del espacio y el tiempo de once dimensiones.

Esta teoría predice que nuestro Universo sigue teniendo un gemelo enano, un universo compañero que se ha enrollado en una pequeña bola de seis dimensiones (en la escala de Planck) muy pequeña para ser observada.
Ese Universo con once dimensiones, lejos de ser un apéndice inútil de nuestro mundo, podría ser en última instancia, nuestra salvación. Claro que, si las galaxias siguen alejándose las unas de las otras, será la muerte térmica del universo, y, en ese escenario, ni los átomos se moverán.

Todo quedará quieto, congelado en los -273 ºC
Para el cosmólogo, la única certeza es que el Universo morirá un día. Algunos creen que la muerte final del Universo llegará en la forma del big crunch. La gravitación invertirá la expansión cósmica generada por el big bang y comprimirá las estrellas y las galaxias, de nuevo, en una masa primordial. A medida que las estrellas se contraen, las temperaturas aumentan espectacularmente hasta que toda la materia y la energía del universo están concentradas en una colosal bola de plasma ardiente que será el resultado final de la destrucción del Universo tal como lo conocemos.
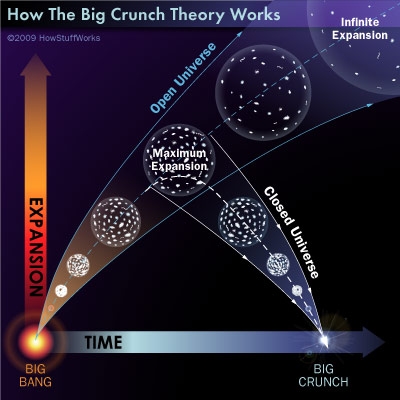
Todas las formas de vida serán borradas de la faz de los mundo que las pudieran contener: evaporadas por las enormes temperaturas o aplastadas, ¡qué más dá! No habrá escape. Y, sabiendo lo que ahora sabemos, conociendo la historia del universo mismo que, durante miles de millones de años ha estado fabricando materiales en las estrellas para que los seres vivos conscientes pudieran venir, ¿cómo imaginar un final así? ¿Para qué tánto trabajo y tanto tiempo perdido? Seguramente, para cuando eso puede ir llegando, si es que la inteligencia sigue aquí, habrá buscado ya la manera de escapar a tal desastre y, las especies inteligentes se salvarán saltanto a otros universos, o, incluso, ¿por qué no? viajando hacia atrás en el Tiempo, hacia otras épocas de tiempos más benignas para tener otros miles de millones de años por delante y hacer las cosas, de manera diferente. ¡Una segunda oportunidad!

“La soberbia obra intelectual del filósofo británico enseña al hombre moderno a rebelarse contra su destino sin caer ni en las trampas de la religión ni en la indignidad de la sumisión.”
Científicos y filósofos, como Charles Darwin y Bertrand Russell, han escrito lamentándose de la futilidad de nuestras míseras existencias, sabiendo que nuestra civilización morirá inexorablemente cuando llegue el fin de nuestro mundo. Las leyes de la física, aparentemente, llevan la garantía de una muerte final e irrevocable para todas las formas de vida, inteligente o no, del Universo.
Yo, como Gerald Feinberg, físico de la Universidad de Columbia (ya desaparecido), creo que sí puede haber, quizá sólo una esperanza de evitar la calamidad final. Ese atisbo de esperanza está en nosotros mismos, es decir, si somos capaces de no destruirnos antes, si procuramos comprender los mensajes que el universo nos envía continuamente, si desvelamos secretos de la Naturaleza que nos posibilitarán para hacer cosas, ahora inimaginables, entonces y solo entonces, habrá alguna esperanza.

Poder escapar a universos conexos que, como el nuestro, nos de cobijo
Gerald Feinberg especuló que la vida inteligente, llegando a dominar los misterios del espacio de más dimensiones (para lo que contaba con un poderoso aliado, el Tiempo de miles de millones de años), sabría utilizar las dimensiones extras para escapar de la catástrofe del Big Crunch. En los momentos finales del colapso de nuestro Universo, el Universo hermano se abriría de nuevo y el viaje inter-dimensional se haría posible mediante un túnel en el Hiperespacio hacia un Universo alternativo, evitando así la pérdida irreparable de la inteligencia de la que somos portadores.
Si algo así es posible, entonces, desde su santuario en el espacio de más dimensiones, la Humanidad, podría ser testigo de la muerte del Universo que la vio nacer y florecer.

Son muchas las cosas que no sabemos
Aunque la teoría de campos demuestra que la energía necesaria para crear estas maravillosas distorsiones del espacio y el tiempo está mucho más allá de cualquier cosa que pueda imaginar la civilización moderna, esto nos plantea dos cuestiones importantes:
¿cuánto tardaría nuestra civilización, que está creciendo exponencialmente en conocimiento y poder, en alcanzar el punto de dominar la teoría de hiperespacio?
¿Y qué sucede con otras formas de vida inteligente en el Universo, que puedan haber alcanzado ya este punto?
“Impresión artística de una hipotética «Nave propulsada por inducción de agujero de gusano», basada indirectamente en un trabajo de 1994 de Miguel Alcubierre. Crédito: NASA CD-98-76634 por Les Bossinas”.
“El Hiperespacio en ciencia ficción es una especie de región conectada con nuestro universo gracias a los agujeros de gusano, y a menudo sirve como atajo en los viajes interestelares para viajar más rápido que la luz.”
“Asimov, no obstante, describen el hiperespacio como una condición más que un lugar. El salto al hiperespacio sería en realidad un cambio de condición de la materia, que viajaría como una onda taquiónica. Al reaparecer en el espacio real, la onda colapsaría, restaurando la materia a su composición de mesones.”
Sea un cambio de condiciones, una incursión en un espacio paralelo o la manipulación de una cuarta dimensión, el hiperespacio no ha sido probado científicamente, aunque tampoco ha podido ser rebatido.
En general, como toda forma de viajar a velocidades mayores que la luz, mantiene el inconveniente según el cual superar esta barrera implicaría también la posibilidad de viajar en el tiempo y, consecuentemente, violar el principio de causalidad, dando lugar a paradojas que parecen contradecir tal posibilidad.
Lo que hace interesante esa discusión es que científicos serios han tratado de cuantificar el progreso de la civilización en un futuro lejano, cuando los viajes por el espacio sean una rutina en los sistemas estelares o incluso las galaxias vecinas hayan sido colonizadas. Aunque la escala de energía necesaria para manipular el Hiperespacio es astronómicamente grande, estos científicos señalan que el crecimiento del conocimiento científico aumentara, sin ninguna duda, de forma exponencial durante los siglos y milenios próximos, superando las capacidades de las mentes humanas para captarlo (como ocurre ahora con la teoría M, parada en seco, esperando que alguien vea las matemáticas necesarias para continuar su desarrollo).

Calaboré con el Año Internacional de la Astronomía y, por aquellos días, pude aprender muchas cosas
Somos conscientes de que el Tiempo inexorable sigue su implacable caminar y la Entropía, que sabe hacer bien su trabajo, lo transforma todo, lo que ayer era una cosa, hoy se ha convertido en otra distinsta, irreconocible, y, sin embargo, ese deterioro natural no es algo perdido, sino que, por el contrario, hasta que llega ese final, se hizo un trabajo que dará sus frutos en la mente de otros seres, en las cosas mismas que, transformadas, servirán y tendrán cometidos nuevos. Nada se pierde y todo tiene su por qué. La Naturaleza no hace nada porque sí, todo está programado y tiene un fin. Y, si eso es así (que los es), ¿que nos deparará el destino a nosotros? Habiendo llegado al nivel de cpomprensión alcanzado, no creo que el final sea el de la desaparición sin más, algo más debe estar oculto en los designios de la Naturaleza que no llegamos a comprender.

La incomprensión de la función exponencial
Cada 10/15 años el conocimiento científico se doblará, crecerá el cien por ciento, así que, el avance superará todas las previsiones. Tecnologías que hoy solo son un sueño (la energía de fusión o en robótica, los cerebros positrónicos), serán realidad en un tiempo muy corto en el futuro. Quizá entonces podamos discutir con cierto sentido la cuestión de si podremos o no ser señores del Hiperespacio.
Viaje en el tiempo. Universos paralelos. Ventana dimensional.
¡Sueños! Claro que, si echamos una atenta mirada a la Historia veremos que, muchos sueños se hicieron realidad.
emilio silvera
Sep
4
¡Es tan grande el Universo! No, no estamos sólos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en El Universo asombroso ~
Clasificado en El Universo asombroso ~
 Comments (2)
Comments (2)
La sinfonía de los agujeros negros binarios ¿La oirémos algún día?

“Simulación por computador del agujero negro binario detectado por LIGO, tal como se vería por un observador. Las estrellas en el fondo parecen rotar y moverse debido al enorme lente gravitacional generado mientras se distorsiona el espacio-tiempo alrededor del sistema.”
Según nos cuentan sí se ha podido oír (por fin) la sinfonía.
Maravillas sin fin, extraños objetos que nos llevan a imaginar lo que podrían ser. Una figura que parece ser el ojo que nos vigila, o, moléculas y sustancias necesarias para la vida y mucho más podemos encontrar en nuestro Universo.

Pensar que estamos solos en el Universo “infinito”, es demasiado pretencioso y no creo que seamos “la especie elegida” ni nada parecido. En cientos de miles de mundos como el nuestro y parecidos, estarán presentes las más diversas criaturas que, en algunos casos tendrán entendimiento y en otros, como pasa en la Tierra, simplemente serán seres vivos vegetativos sin ninguna clase de conciencia, o, con una conciencia limitada.
La vida inteligente es algo extraño que aún no hemos sabido explicar. El chimpancé tiene el 98% de nuestra estructura genética, y, sin embargo, mientras nosotros hablamos de mecánica cuántica ellos siguen en la copa de los árboles, Según nos dicen los científicos, ambas especies (la humana y la chimpanée) tienen un ancestro común que no era ni Homo ni Pan, de él surgieron las dos ramos que divergieron cada cual a un destino diferente.

Poco esfuerzo mental tendriamos que hacer para vernos en ellos reflejados
Una característica sorprendente de nuestro retrato reconstruido del antepasado primitivo es su carácter moderno. Si este organismo lo encontráramos hoy, seguramente no delataría su inmensa antigüedad, excepto por sus secuencias de DNA. Tuvo que estar precedido, necesariamente, por formas más rudimentarias, estadios intermedios en la génesis de sistemas estructurales, metabólicos, energéticos y genéticos complejos que son compartidos por todos los seres vivos de hoy en día. Por desgracia, tales formas no han dejado descendientes igualmente primitivos que permitan su caracterización. carencia complica mucho el problema del origen de la vida.
Aquella “bola” candente ae fue enfriando y en los océanos que se formaron se crearon aminoácidos
“Hace más de seis décadas, dos científicos realizaron un experimento con el que demostraron que los aminoácidos, aquellas moléculas indispensables para las proteínas, pueden formarse de manera espontánea simulando las condiciones primitivas de la Tierra. Con ello cobró mayor fuerza la teoría del origen heterotrófico de la vida en nuestro planeta.”
El comienzo y la formación de nuestro planeta fue violento. En sus primeros días, la Tierra tenía un calor abrasador y no tenía una atmósfera o agua. Si al comienzo se originó vida, ésta fue extinguida por las terribles condiciones. Los fósciles dee formas de vida más antiguos han sido datados en 3.850 millones de años

La Tierra nació hace unos 4.550 millones de años. Se condensó, junto con los otros planetas del sistema solar, en un disco de gas y polvo que giraba alrededor de una joven estrella que iba a convertirse en nuestro Sol. Fenómenos de violencia extrema, incompatible con el mantenimiento de ningún de vida, rodearon este nacimiento. Durante al menos quinientos millones de años, cometas y asteroides sacudieron la Tierra en formación, con lo que la hicieron incapaz de albergar vida durante todo este tiempo. Algunos impactos pudieron haber sido incluso suficientemente violentos como para producir la pérdida de toda agua terrestre por vaporización, después de lo cual los océanos se habrían vuelto a llenar con agua aportada por cometas. Según esta versión de los acontecimientos, los océanos actuales de remontarían a la última oleada de bombardeo cometario intenso, que los expertos creen que tuvo lugar hace unos cuatro mil millones de años. Existen señales de que había vida en la Tierra poco después de que dichos cataclismos llegaran a su fin.

El tiempo inexorable no deja de transcurrir, el Universo dinámico hace que todo lo que contiene, sobre todo la materia, evolucione desde formas simples a complejas y, en algunos lugares que han logrado tener las para ello, puede estar presente la vida. Nosotros, seres evolucionados a partir de la matería inerte creada en las estrellas, hemos logrado saber algunas cosas y no dejamos de hacernos preguntas como aquella de: ¿Habrá otros mundos? ¿Estarán, como la Tierra, llenos de vida? Bueno, lo de los mundos sí hemos sido capaces de saberlo y estarán muy cerca del millar los mundos que hemos descubierto. Sin embargo, la vida, sólo la hemos podido encontrar aquí en nuestra casa, en la Tierra.
No dejamos de mandar ingenios espaciales a mundos cercanos, como Marte, para tratar de saber. Nos embarga una ilusión, una esperanza, y…, al mismo tiempo, un temor: ¿Estaremos sólos? Y, si no lo estamos, ¿cómo serán esos otros mundos y que criaturas lo habitan? ¿Si alguna vez llegamos allí, seremos tan destructivos como lo hemos sido aquí en la Tierra? ¿Le querremos quitar lo que ellos tienen? ¡Esperémos que no! Y, sobre todo, en ese primer , ¿Sabremos comportarnos y respetar sus derechos?
Seres parecidos a nosotros que tenían un profundo sentido de respeto hacia la Naturaleza
Cuando pude ver la película Avatar, quedé fascinado por el mundo que allí quedaba escenificado y las criaturas que lo poblaban, y, sobre todo, era sobrecogedor el alto grado espiritual que tenían de la Naturaleza con la que se sentían en comunidad, formaban una simbiosis perfecta que nosotros, los humanos, nunca podremos alcanzar. Cuando miramos la Naturaleza nos llama la atención la cascada y el bello paisaje pero… ¡No pensamos más allá! ¡Que botarates podemos llegar a ser!
Hemos sabido recrear historias de esos mundos presentidos y de sus habitantes. En ellas, han quedado reflejados los instintos humanos, tantos los buenos como los malos y, mientras que unos querían preservar aquella Naturaleza, otros, sin embargo, querían destriuirla apoderarse de sus preciados tesoros. ¡La condición Humana! ¿Estamos acaso destinados al desacuerdo que nos lleve a la destrucción, o, por el contrario, es precisamente esa condición la que nos llevará lejos?
![]()
La belleza que se describe en el mundo llamado “Pandora” también está aquí pero, ¡no sabemos cuidarla!
Fascinantes criaturas de exóticas bellezas nos podrían estar esperando, en un futuro lejano, en esos mundos soñados que tantas veces hemos podido imaginar. Es difícil saber qué comportamiento tendremos con ellos si eso llega a sucecder, sin embargo, el ejemplo que nos deja la película a la que pertene la imagen de arriba, no es muy alentador ni dice mucho en de nuestra especie que, irrumpimos por la fuerza en un planeta extraño y, violando todas las reglas, pasamos por encima de los derechos de otros para conseguir nuestros objetivos. ¿La Civilización que ocupa el planeta? ¿Qué importa? Si hay que destruirla, ¡adelante!

La fuerza bruta que siempre acompañó a la falta de inteligencia, es la única salida para seres de cuya racionalidad podríamos dudar, sin el menor temor a equivocarnos. Destruir nunca será el camino más conveniente. Creo que sería aconsejable guiarse por ese principio de la física, la causalidad. Si respetamos seremos respetados. Sobre todo, no podemos llegar a nuevos lugares pretendiendo imponer nuestras costumbres y nuestras reglas. En esos otros lugares donde posiblemente existan seres que tienen su propia de vivir, se impone, sobre todo, que supeditemos nuestro comportamiento a su propias reglas a su propio mundo. Los extraños allí seremos nosotros. Ellos, los seres de la hisotira, a diferencia de nuestra Civilización Terrestre, sí han sabido convivir con su entorno, han creado una especie de simbiosis que une a todos los seres de aquel fascionante mundo, sean seres racionales o plantas, hasta el punto de poder comunicarse entre ellos en un alto grado de compenetración que va mucho más allá de lo físico.
![]()
En esos otros Mundos pueden estar presentes seres maravillosos que han optado por otras maneras de vivir, más cercana y conectados con la Naturaleza a la que respetan y comprenden al ser conscientes de que ellos mismos, forman de ella que es algo que, los humanos no han acabado de comprender y, se comportan como si la Tierra fuera un simple instrumento a su servicio, sin ser conscientes que tal comportamiento, los puede llevar a la extinción de la especie.
Las montañas, los árboles, los ríos y el viento, todo bañado por la luz y el calor de esa estrella que nos alumbra, forman un todo que mantiene el equilibrio que hace posible la vida. Si alguno de esos parámetros se viera alterado seriamente… ¡Mal nos iría! Y, sin embargo, algunos se empeñan en no ver lo evidente.
Si algún día conseguimos llegar a otros mundos y en ellos encontramos a criaturas vivas más o mneos evolucionadas, lo conveniente sería respetarlos y, dentro de lo posible, aprender de ellos procurando alterar lo menos posible lo que allí nos encontremos y, si tienen algo que nosotros necesitamos, hacer un intercambio justo olvidándonos de la fuerza bruta que conlleva la destrucción irreparable.
La historia que nos cuentan en esa maravillosa película, , desde el principio nos pone a favor de los habitantes de aquel Mundo agredido y de sus habitantes, hasta tal punto es así que muchos de los terrestres que visitan aquél planeta, no dudan, en dar sus propias vidas por preservar aquel entorno, para nosotros de fantasía y que para aquellos seres tan especiales que han sido capaces de convivir con su mundo y “hablar” con él, demostrando de alguna manera que, son mucho mñás civilizados que nosotros. Cuando ví aquella película… ¡Qué envidia me dieron!
Utilizar lo que la Naturaleza les ofrecía sin dañar, no coger más de lo estrictamente necesario para vivir, respetando las otras formas de vida del planeta y dejando que el ritmo de la Naturalerza sea el que desarrolle las cosas, sin agredir el entorno y dejando que cada cosa ocupe su lugar sin tratar de violentar, de alguna manera, su desarrollo natural.
Si el caso llega, tendremos que aprender a mirar más allá de la superficie, a entender los mensajes que nos envían la mirada de esos nuevos y exóticos seres y, sobre todo, tratar de comprender su mundo, sus maneras para poder respetarlas y hacernos acreedores, nosotros también, a su respeto.
¡Quién pudiera ser uno de los afortunados que, en el futuro, visitarán algunos de esos Mundos!
Nos quedan muchos muros por derribar, muchas puertas que abrir para las que aún no poseemos las llaven, y, sobre todo, para que cuando eso llegue y sea una realidad (esperemos que así sea), lo más importante: ¡Que hayamos podido evolucionar hasta ese deseado estadio de sabiduría que ahora no tenemos! De todas las maneras, no me gustaría que ese primer encuentro se produjera aquí en la Tierra. Es preferible que los visitantes seamos nosotros y, como antes digo, espero que para entonces, la Humanidad sea otra.

Claro que, también podríamos toparnos con civilizaciones mucho más avanzadas que la nuestra y, en ese caso… ¡La desventaja sería nuestra! Siempre hemos oído decir que no debemos hacer a otros lo que no queremos que nos hagan a nosotros y, si respetamos esa máxima… ¡Todo podrá ir mejor! El presente es el que tenemos y no sabemos lo que nos depara el futuro pero, una cosa es bien cierta: ¡No dejamos de avanzar! Cada día que pasa damos un paso hacia ese futuro que presentimos y estamos más cerca de saber… ¡Si realmente, como pensamos, estamos miuy bien acompañados en este inmenso Universo nuestro! Y, digo en éste universo nuestro porque, en realidad, pienso que tampoco es, el único Universo.
emilio silvera
Sep
3
La Imperfecta perfección
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (3)
Comments (3)

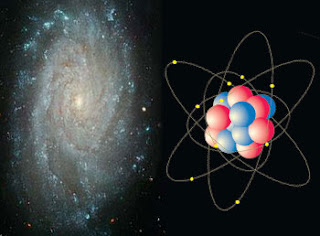
Todo lo que existe en nuestro Universo es el fruto de dos fuerzas antagónicas que se equilibran la una a la otra y produce la estabilidad que podemos observar en las galaxias y en las estrellas, en los átomos…
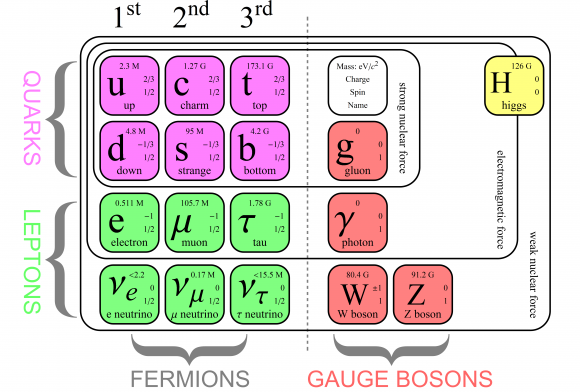
«A pesar de sus limitaciones, el modelo estándar es una herramienta básica para el avance de la física actual, como hace cien años lo fue el electromagnetismo. [Un] gran avance en nuestra comprensión del universo. Aunque no podamos hallar en él un candidato para la enigmática materia oscura, esta podrá ser identificada gracias a su interacción con detectores terrestres, y podrá ser interpretada gracias al modelo estándar».
Mario E. Gómez Santsamaría
“El modelo estándar de la física de partículas es una teoría relativista de campos cuánticos desarrollada entre 1970 y 1973 [cita requerida] basada en las ideas de la unificación y simetrías1 que describe la estructura fundamental de la materia y el vacío considerando las partículas elementales como entes irreducibles cuya cinemática está regida por las cuatro interacciones fundamentales conocidas (exceptuando la gravedad, cuya principal teoría, la relatividad general, no encaja con los modelos matemáticos del mundo cuántico).”
Wikipedia
Con el título que arriba podemos leer de “La perfección imperfecta”, me quiero referir al Modelo estándar de la física de partículas y de las interacciones fundamentales y, algunos, han llegado a creer que sólo faltan algunos detalles técnicos y, con ellos, la física teórica está acabada. Tenemos un modelo que engloba todo lo que desamos saber acerca de nuestro mundo físico. ¿Qué más podemos desear? Los pobres ilusos no caen en la de que el tal Modelo, al que no podemos negarle su valía como una herramienta muy valiosa para la física, no deja de estar incompleto y, además, ha sido construido con algunos parámetros aleatorios (unos veinte) que no tienen justificación. Uno de ellos era el Bosón de Higgs y, según nos han contado los del LHC, ha sido hallado. Sin embargo, esperamos que nos den muchas explicaciones que no han presente en todas las algaradas y fanfarrias que dicho “hallazgo” ha producido, incluidos el Principe de Asturias y el Nobel. ¡Veremos en que queda todo esto al final!

Bueno, lo que el momento hemos logrado no está mal del todo pero, no llega, ni con mucho, a la perfección que la Naturaleza refleja y que, nosotros perseguimos sin llegar a poder agarrar sus múltiples entrecijos y parámetros que conforman ese todo en el que, sin ninguna clase de excusas, todo debe encajar y, de momento, no es así. Muchos son los flecos sueltos, muchas las incognitas, múltiples los matices que no sabemos perfilar.
Es cierto que, el Modelo estándar, en algunos momento, nos produce y nos da la sensación de que puede ser perfecto. Sin embargo, esa ilusoria perfección, no es permanente y en algunas casos efímera. En primer lugar, podríamos empezar a quejarnos de las casi veinte constantes que no se pueden calcular. Pero si esta fuese la única queja, habría poco que hacer. luego, se han sugerido numerosas ideas para explicar el origen de estos números y se han propuesto varias teorías para “predecir” sus valores. El problema con todas estas teorías es que los argumentos que dan nunca llegan a ser convincentes.

Algunos tienen la esperanza de que se verá la Supersimetría en el LHC para saber, qué hay más allá del Modelo Estándar. ¿Serán las cuerdas vibrantes de la Teoría M?
“El Modelo Estándar agrupa, pero no unifica, las dos primeras teorías –el modelo electrodébil y la cromodinámica cuántica– lo que proporciona una teoría internamente consistente que describe las interacciones entre todas las partículas observadas experimentalmente.”
“Aceleración recíproca de dos líneas de universo geodésicas. Como vemos, conforme se avanza en la coordenada temporal, el tensor de Riemann curva las geodésicas y provoca el acercamiento recíproco de las dos partículas.
En relatividad general, la aceleración de marea viene originada por el tensor de Riemann. Hay una correspondencia casi natural entre las ecuaciones newtonianas y las relativistas. En efecto, la ecuación newtoniana utilizada para computar las fuerzas de marea es la siguiente:
donde a es la aceleración de marea,
el potencial gravitatorio y
la distancia entre las dos partículas. Las fuerzas de marea vienen determinadas por las derivadas de segundo orden del potencial gravitatorio.”
Si deseamos medir la contracción de volumen producida por la masa-energía presente en una determinada región, hemos de aplicar las ecuaciones de universo de Einstein:
Computemos ahora los valores de
:
Tras ello obtenemos:
Como vemos, la atracción gravitatoria viene determinada nosolo por la masa-energía sino también por la presión, aunque la contribución de ésta es
inferior a la de la primera. Por eso, en las regiones del espacio-tiempo sometidas a bajas presiones y temperaturas, como las nebulosas o nuestro Sistema Solar, la masa es prácticamente la única fuente de atracción gravitatoria y por ello las ecuaciones de la gravitación universal newtonianas constituyen una muy buena aproximación de la realidad física. En cambio, en fluidos sometidos a altas presiones, como las estrellas que se colapsan, la materia que se precipita en los agujeros negros o los chorros que son expelidos de los centros de las galaxias; en todos ellos la presión puede tener cierta importancia a la hora de computar la atracción gravitatoria y la curvatura del espacio-tiempo.”

“Un principio de relatividad es un principio general sobre la forma que debe tomar una teoría física. Frecuentemente los principios de relatividad establecen equivalencias entre observadores, de acuerdo con principios de simetría o invariancia entre situaciones físicamente equivalentes. De acuerdo con estos principios una determinada descripción de un fenómeno podría ser incorrecta si no respeta el principio de relatividad básico que define la teoría (así la teoría de la gravitación de Newton era incompatible con el principio de relatividad que definía la teoría de la relatividad especial, razón que llevó a Einstein a formular una nueva teoría de la gravitación como parte de la relatividad general).”
¿Por qué se iba a preocupar la Naturaleza de una fórmula mágica si en ausencia de tal fórmula no hubiera contradicciones? Lo que realmente necesitamos es algún principio fundamental , tal como el proncipio de la relatividad, pero nos resistimos a abandonar todos los demás principios que ya conocemos; ¡esos, después de todo, han sido enormemente útiles en el descubrimiento del Modelo estándar! una herramienta que ha posibilitado a todos los físicos del mundo poder construir sus trabajos en ese fascinante mundo de la mecánica cuántica, donde partículas infinitesimales interactúan con las fuerzas y podemos ver, como se comporta la materia en determinadas circunstancias. El mejor lugar para buscar nuevos principios es precisamente donde se encuentran los puntos débiles de la presente teoría.

“Colisión del Bosón de Higgs desintegrándose en fermiones”. Primeras evidencias de un modo de desintegración del bosón de Higgs. Las primeras evidencias de la desintegración del recién descubierto bosón de Higgs en dos partículas denominadas tau, pertenecientes a la familia de partículas que compone la materia que vemos en el Universo. Hasta los experimentos del LHC habían detectado la partícula de Higgs mediante su desintegración en otro de partículas denominadas bosones, portadoras de las fuerzas que actúan en la Naturaleza, mientras las evidencias de desintegraciones en fermiones no eran concluyentes. Esta es la primera evidencia clara de este nuevo modo de desintegración del bosón de Higgs.”
La regla universal en la física de partículas es que cuando las partículas chocan con energías cada vez mayores, los efectos de las colisiones están determinados por estructuras cada vez menores, más pequeñas en el espacio y en el tiempo. Supongamos por un momento que tenemos a nuestra disposición un Acelerador de Partículas 10.000 veces más potente que el LHC, donde las partículas pueden adquirir esas tantas veces más energías de las alcanzadas actualmente. Las colisiones que tendrían lugar nos dirían algo acerca de los detalles estructurales de esas partículas que ahora no conocemos, que serían mucho más pequeñas que las que ahora podemos contemplar. En este punto se me ocurre la pregunta: ¿Seguiría siendo correcto el Modelo estándar? 0, por el contrario, a medida que nos alejemos en las profundidades de lo muy pequeño, también sus normas podrían variar al mismo tiempo que varían las dimensiones de los productos hallados. Recordad que, el mundo no funciona de la misma manera en nuestro ámbirto macroscópico que ante ese otro “universo” cuántico de lo infinitesimal.

¿Podeis imaginar conseguir colisiones a 70.000 TeV? ¿Que podríamos ver? Y, entonces, seguramente, podríamos oir en los medios la algarada de las protestas de algunos grupos: “Ese monstruo creado por el hombre abrir en el espacio tiempo agujeros de gusano que se tragará el mundo y nos llevará otros universos” Comentarios así estarían a la orden del día. Los hay que siempre están dispuestos a protestar por todo y, luego, no siempre llevan razón, toda vez que, la mayoría de las veces, ignoran de qué están hablando y juzgan si el conocimiento de causa necesario para ello. De todas las maneras, sí que debemos tener sumo cuidado con el manejo de fuerzas que… ¡no siempre entendemos! Cuando el LHC se vuelvsa a poner en marcha, se utilizarán energías que llegan hasta los 14 TeV, y, esas son palabras mayores.
Hay que reconocer que imaginación se le ponemos a simples conjeturas
¿Justifica el querer detectar las partículas que conforman la “materia oscura”, o, verificar si al , podemos vislumbrar la sombra de las “cuerdas” vibrantes de esa Teoria del Todo, el que se gasten ingentes cantidades de dinero en esos artilugios descomunales? Bueno, a pesar de todos los pesares, la respuesta es que SÍ, el rendimiento y el beneficio que hemos podido recibir de los aceleradores de partículas, justifica de manera amplia todo el esfuerzo realizado, toda vez que, no nos ha llevado a conocer muchos secretos que la Naturaleza celosamente guardaba, sino que, de sus actividades hemos tenido beneficios muy directos en ámbitos como la medicina, las comunicaciones y otros que la gente corriente desconocen.
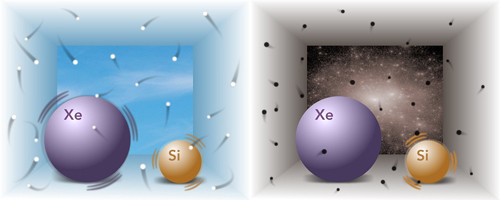
Hoy, el Modelo estándar es una construcción matemática que predice sin ambigüedad cómo debe ser el mundo de las estructuras aún más pequeñas. Pero tenemos algunas razones para sospechar que tales predicciones resultan estar muy alejadas de la realidad, o, incluso, ser completamente falsas. Cuando tenemos la posibilidad de llegar más lejos, con sorpresa podemos que aquello en lo que habíamos creído durante años, era totalmente diferente. El “mundo” cambia a medida que nos alejamos más y más de lo grande y nos sumergimos en ese otro “mundo” de lo muy pequeño, allí donde habitan los minúsculos objetos que conforman la materia desde los cimientos mismos de la creación.
Encendamos nuestro supermicroscopio imaginario y enfoquemosló directamente en el centro de un protón o de cualquier otra partícula. Veremos hordas de partículas fundamentales desnudas pululando. Vistas a través del supermicroscopio, el modelo estándar que contiene veinte constantes naturales, describen las fuerzas que rigen la forma en que se mueven. Sin embargo, esas fuerzas no sólo son bastante fuertes sino que también se cancelan entre ellas de una forma muy especial; están ajustadas para conspirar de tal manera que las partículas se comportan como partículas ordinarias cuando se vuelven a colocar el microscopio en la escala de ampliación ordinaria.
Si en nuestras ecuaciones matemáticas cualquiera de estas constantes fueran reemplazadas por un número ligeramente diferente, la mayoría de las partículas obtendrían inmediatamente masas comparables a las gigantescas energías que son relevantes en el de las muy altas energías. El hecho de que todas las partículas tengan masa que corresponden a energías mucho menores repentinamente llega a ser bastante poco natural.
¿Implica el ajuste fino un diseño con propósito? ¿Hay tantos parámetros que deben tener un ajuste fino y el grado de ajuste fino es tan alto, que no parece posible ninguna otra conclusión?
decía: “El hecho de que todas las partículas tengan masa que corresponden a energías mucho menores repentinamente llega a ser bastante poco natural”. Es lo que se llama el “problema del ajuste fino”. Vistas a través del , las constantes de la Naturaleza parecen estar cuidadosamente ajustadas sin ninguna otra razón aparente que hacer que las partículas parezcan lo que son.
Hay algo muy erróneo aquí. Desde un punto de vista matemático, no hay nada que objetar, pero la credibilidad del Modelo estándar se desploma cuando se mira a escalas de tiempo y longitud extremadamente pequeñas o, lo que es lo mismo, si calculamos lo que pasaría cuando las partículas colisionan con energías extremadamente altas.
¿Y por qué debería ser el modelo válido hasta ahí? Podrían existir muchas clases de partículas súper pesadas que no han nacido porque se necesitan energías aún inalcanzables, ellas podrían modificar completamente el mundo que Gulliver planeaba visitar. Si deseamos evitar la necesidad de un delicado ajuste fino de las constantes de la Naturaleza, creamos un problema:

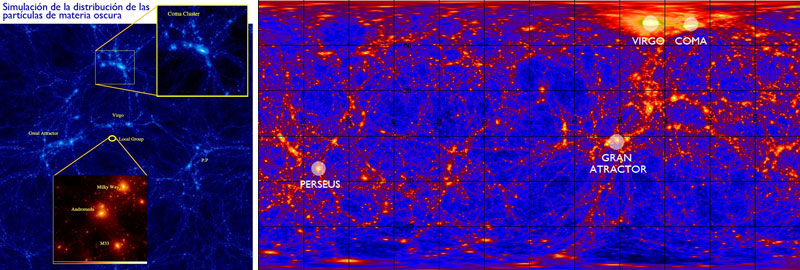
Aquí dicen: “La materia oscura podría estar hecha de extrañas partículas inmortales”
Es cierto que nuestra imaginación es grande … No pocas veces ¡la realidad la supera!
¿Cómo podemos modificar el modelo estándar de tal manera que el ajuste-fino no sea necesario? Está claro que las moficiaciones son necesarias , lo que implica que muy probablemente hay un límite más allá del cual el modelo deja de ser válido. El Modelo estándar no será más que una aproximación matemática que hemos sido capaces de crear, tal que todos los fenómenos observados el presente están de acuerdo con él, pero cada vez que ponemos en marcha un aparato más poderoso, debemos esperar que sean necesarias nuevas modificaciones para ir ajustando el modelo, a la realidad que descubrimos.
Tendremos que convenir que… ¡Imaginación no nos falta!
¿Cómo hemos podido pensar de otra manera? ¿Cómo hemos tenido la “arrogancia” de pensar que podemos tener la teoría “definitiva”? Mirando las cosas de esta manera, nuestro problema puede muy bien ser el opuesto al que plantea la pregunta de dónde acaba el modelo estándar: ¿cómo puede ser que el modelo estándar funcione tan extraordinariamente bien? y ¿por qué aún no hemos sido capaces de percibir nada parecido a otra generación de partículas y fuerzas que no encajen en el modelo estándar? La respuesta puede estar en el hecho cierto de que no disponemos de la energía necesaria para poder llegar más lejos de lo que hasta el momento hemos podido viajar con ayuda de los aceleradores de partículas.
:quality(85)//s3.amazonaws.com/arc-wordpress-client-uploads/infobae-wp/wp-content/uploads/2017/04/20092708/particula-cern-1024x575.jpg)
Los asistentes escuchan la presentación de los resultados del experimento ATLAS, durante el seminario del Centro Europeo de Física de Partículas (CERN) presentar los resultados de los dos experimentos paralelos que buscan la prueba de la existencia de la “partícula de Higgs, base del modelo estándar de física.
La pregunta “¿Qué hay más allá del Modelo estándar”? ha estado facinando a los físicos durante años. Y, luego, todos sueñan con llegar a saber, qué es lo que realmente es lo que conforma el “mundo” de la materia, qué partículas, cuerdas o briznas vibrantes. En realidad, lo cierto es que, la Física que conocemos no tiene que ser, necesariamente, la verdadera física que conforma el mundo y, sí, la física que conforma “nuestro mundo”, es decir, el mundo al que hemos podido tener acceso hasta el momento y que no necesariamente tiene que coincidir con el mundo real que no hemos podido alcanzar.
¡Que mundo más hermoso, parece de verdad!

Nuestros sentidos imperfectos no nos deja ver… Lo que la Nutaraleza esconde
No todo lo que vemos es, necesariamente, un reflejo de la realidad de la Naturaleza que puede tener escondidos más allá de nuestras percepciones, otros escenarios y otros objetos, a los que, por , no hemos podido acceder, toda vez que, físicamente tenemos carencias, intelectualmente también, y, nuestros conocimientos avanzar despacio para conseguir, nuevas máquinas y tecnologías nuevas que nos posibiliten “ver” lo que ahora nos está “prohibido” y, para ello, como ocurre siempre, necesitamos energías de las que no disponemos.

Hay dos direcciones a lo largo de las cuales se podría extender el Modelo estándar, tal lo conocemos actualmente, que básicamente se caraterizan así:
– Nuevas partículas raras y nuevas fuerzas extremadamente débiles, y
– nuevas partículas pesadas y nuevas estructuras a muy altas energías.
Podrían existir partículas muy difíciles de producir y de detectar y que, por esa razón, hayan pasado desapaercibidas neutrino rotando a derecha. Recordaremos que si se toma el eje de rotación paralelo a la dirección del movimiento los neutrinos sólo rotan a izquierdas , esa sería otra historia.
En alguna parte pude leer:

“Los interferómetros atómicos tienen la sensibilidad para observar nuevas fuerzas más allá del modelo estándar de la física de partículas. “Las nuevas fuerzas a corta distancia son una predicción frecuente de las teorías más allá del Modelo Estándar y la búsqueda de estas nuevas fuerzas es un canal prometedor para una nueva física”, dice Jay Wackerdel Laboratorio del Acelerador Nacional SLAC en California. La pregunta es cómo encontrarlas”

Los neutrinos siempre me han fascinado. Siempre se han manifestado como si tuvieran masa estrictamente nula. Parece como si se movieran exactamente con la velocidad de la luz. Pero hay un límite la precisión de nuestras medidas. Si los neutrinos fueran muy ligeros, por ejemplo, una cienmillonésima de la masa del electrón, seríamos incapaces de detectar en el laboratorio la diferencia éstos y los neutrinos de masa estrictamente nula. Pero, para ello, el neutrino tendría que tener una componente de derechas.
En punto, los astrónomos se unen a la discusión. No es la primera vez, ni será la última, que la astronomía nos proporciona información esencial en relación a las partículas elementales. Por ejemplo, debido a las interacciones de corriente neutra (las interacciones débiles originadas por un intercambio Zº), los neutrinos son un facto crucial en la explosión supernova de una estrella. sabemos que debido a las interacciones por corriente neutra, pueden colisionar con las capas exteriores de la estrella y volarlas con una fuerza tremenda.

En realidad, los neutrinos nos tienen mucho que decir, todavía y, no lo sabemos todo acerca de ellos, sino que, al contrario, son muchos los y fenómenos que están y subyacen en ellos de los que no tenemos ni la menor idea que existan o se puedan producir. Nuestra ignorancia es grande, y, sin embargo, no nos arredra hablar y hablar de cuestiones que, la mayoría de las veces…ni comprendemos.
Aquí lo dejar´ñe por hoy, el tema es largo y de una fascinación que te puede llevar a lugares en los que no habías pensado al comenzar a escribir, lugares maravillosos donde reinan objetos exóticos y de fascinante que, por su pequeñez, pueden vivir en “mundos” muy diferentes al nuestro en los que, ocurren cosas que, nos llevan el asombro y , a ese mundo mágico de lo fascinante y maravilloso.
emilio silvera
















 Totales: 83.324.571
Totales: 83.324.571 Conectados: 52
Conectados: 52


































