Oct
26
Abundancia Cósmica de Elementos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Alquimia estelar ~
Clasificado en Alquimia estelar ~
 Comments (3)
Comments (3)
Nuevas ideas, ideas viejas

¿Será cierto que todo surgió de una Singularidad? ¿Produjo una fluctuación de “vacío” la dinámica que nos trajo el Universo? ¿Cómo se pudieron formar las galaxias a pesar de la expansión de Hubble? ¿Existía allí, desde aquel primer momento una sustancia cósmica que generaba Gravedad para retener a la materia recién creada?
El cúmulo de preguntas es tal que, deja al descubierto nuestra enorme ignorancia y tenemos que seguir rigiendo nuestros pensamientos por conjeturas y teorías no verificadas, o, en el mejor de los casos, verificadas a medias.
“En física, la inercia es la propiedad que tienen los cuerpos de permanecer en su estado de reposo relativo o movimiento relativo. Dicho de forma general, es la resistencia que opone la materia al modificar su estado de movimiento, incluyendo cambios en la velocidad o en la dirección del movimiento. Como consecuencia, un cuerpo conserva su estado de reposo relativo o movimiento rectilíneo uniforme relativo si no hay una fuerza que, actuando sobre él, logre cambiar su estado de movimiento.
En la naturaleza no existe el reposo, siempre toda la materia está en movimiento, por eso cuando se habla de reposo o Movimiento Rectilíneo Uniforme (MRU) se debe añadir la palabra “relativo” (relativo a un sistema de referencia). El cuerpo está en reposo o en MRU solo con respecto de ese sistema de referencia. Cuando un cuerpo está en reposo relativo sobre la superficie de la Tierra, en realidad está participando de los distintos movimientos que realiza el planeta y está sometido a diferentes fuerzas como las gravitatorias de la Tierra, el Sol, La Luna y otros cuerpos, así como la resistencia mecánica que impide que se hunda en la tierra, o se deslice. Se puede decir que el cuerpo se encuentra en equilibrio sobre la superficie de la Tierra y por lo tanto en reposo relativo.
Podríamos decir que es la resistencia que opone un sistema de partículas a modificar su estado dinámico.
En física se dice que un sistema tiene más inercia cuando resulta más difícil lograr un cambio en el estado físico del mismo. Los dos usos más frecuentes en física son la inercia mecánica y la inercia térmica.”

Se encuentran elementos esenciales para la vida alrededor de una estrella joven. Usando el radiotelescopio ALMA (Atacama Large Millimeter/submillimeter Array), un grupo de astrónomos detectó moléculas de azúcar presentes en el gas que rodea a una estrella joven, similar al sol. Esta es la primera vez que se ha descubierto azúcar en el espacio alrededor de una estrella de estas características. Tal hallazgo demuestra que los elementos esenciales para la vida se encuentran en el momento y lugar adecuados para poder existir en los planetas que se forman alrededor de la estrella.
La abundancia, distribución y comportamiento de los elementos químicos en el Cosmos es uno de los tópicos clásicos de la astrofísica y la cosmoquímica. En geoquímica es también importante realizar este estudio ya que:

– Una de las principales finalidades de la Geoquímica es establecer las leyes que rigen el comportamiento, distribución, proporciones relativas y relaciones entre los distintos elementos químicos.
– Los datos de abundancias de elementos e isótopos en los distintos tipos de estrellas nos van a servir para establecer hipótesis del origen de los elementos.
– Los datos de composición del Sol y las estrellas nos permiten establecer hipótesis sobre el origen y evolución de las estrellas. Cualquier hipótesis que explique el origen del Sistema Solar debe explicar también el origen de la Tierra, como planeta de dicho Sistema Solar.
– Las distintas capas de la Tierra presentan abundancias diferentes de elementos. El conocer la abundancia cósmica nos permite tener un punto de referencia común. Así, sabiendo cuales son las concentraciones normales de los elementos en el cosmos las diferencias con las abundancia en la Tierra nos pueden proporcionar hipótesis de los procesos geoquímicos que actuaron sobre la Tierra originando migraciones y acumulaciones de los distintos elementos, que modificaron sus proporciones y abundancias respecto al Cosmos.
La tabla periódica de los elementos es un arreglo sumamente ingenioso que permite presentar de manera lógica y estructurada las más simples sustancias de las que se compone todo: absolutamente todo lo que conocemos. Todos los elementos que conocemos, e incluso con lo que todavía no nos hemos encontrado, tienen un lugar preciso en ella, cuya posición nos permite conocer muchas de sus características. Ese grupo de casi cien ingredientes permite crear cualquier cosa. Pero no siempre fue así

Me gusta la Gran Nebulosa de Orión. Hay ahí tántas cosas, nos cuenta tantas historias…
FUENTES DE DATOS DE ABUNDANCIAS COSMICAS DE LOS ELEMENTOS. Estos datos deben obtenerse a partir del estudio de la materia cósmica. La materia cósmica comprende: Gas interestelar, de muy baja densidad (10-24 g/cm3) y Nébulas gaseosas o nubes de gas interestelar y polvo.
Las nébulas gaseosas se producen cuando una porción del medio interestelar está sujeta a radiación por una estrella brillante y muy caliente, hasta tal punto se ioniza que se vuelve fluorescente y emite un espectro de línea brillante (que se estudian por métodos espectroscopios). Por ejemplo las nébulas de “Orión” y “Trifidos”. Las ventajas de estas nébulas difusas para el estudio de las abundancias son:
![[Espada+de+Orion.jpg]](http://4.bp.blogspot.com/_hfB00NeNnmw/Sdv45L0CS1I/AAAAAAAAAms/31O1WKtM1Nc/s1600/Espada%2Bde%2BOrion.jpg)
‑ Su uniformidad de composición.
‑ El que todas sus partes sean accesibles a la observación, al contrario de lo que ocurre en las estrellas.
También tiene desventajas:
‑ Solo se observan las líneas de los elementos más abundantes.
‑ Cada elemento se observa solo en uno o pocos estadios de ionización aunque puede existir en muchos.
‑ La mayoría de las nébulas exhiben una estructura filamentosa o estratiforme es decir que ni la D ni la T son uniformes de un punto a otro. A partir del medio interestelar (gas interestelar y nébulas gaseosas) se están formando continuamente nuevas estrellas.

Los pilares de la Creación
En las estrellas podemos encontrar muchas respuestas de cómo se forman los elementos que conocemos. Primero fue en el hipotético big bang donde se formaron los elementos más simples: Hidrógeno, Helio y Litio. Pasados muchos millones de años se formaron las primeras estrellas y, en ellas, se formaron elementos más complejos como el Carbono, Nitrógeno y Oxígeno. Los elementos más pesados se tuvieron que formar en temperaturas mucho más altas, en presencia de energías inmensas como las explosiones de las estrellas moribundas que, a medida que se van acercando a su final forman materiales como: Sodio, Magnesio, Aluminio, Silicio, Azufre, Cloro, Argón, Potasio, Titanio, Hierro, Cobalto, Niquel, Cobre, Cinc, Plomo, Torio…Uranio. La evolución cósmica de los elementos supone la formación de núcleos simples en el Big Bang y la posterior fusión de estos núcleos ligeros para formar núcleos más pesados y complejos en el interior de las estrellas y en la transición de fase de las explosiones supernovas.

Sir Fred Hoyle en una de sus clases
No me parece justo hablar de los elementos sin mencionar a Fred Hoyle y su inmensa aportación al conocimiento de cómo se producían en las estrellas. Él era temible y sus críticas de la teoría del Big Bang hizo época por su mordacidad. Hoyle condenó la teoría por considerarla epistemológicamente estéril, ya que parecía poner una limitación temporal inviolable a la indagación científica: el big bang era una muralla de fuego, más allá de la cual la ciencia de la época no sabía como investigar. Él no concebía y juzgó “sumamente objetable que las leyes de la física nos condujeran a una situación en la que se nos prohíbe calcular que ocurrió en cierto momento del tiempo”. En aquel momento, no estaba falto de razón.

Pero no es ese el motivo de mencionarlo aquí, Hoyle tenía un dominio de la física nuclear nunca superado entre los astrónomos de su generación, había empezado a trabajar en la cuestión de las reacciones de la fusión estelar a mediado de los cuarenta. Pero había publicado poco, debido a una batalla continua con los “arbitros”, colegas anónimos que leían los artículos y los examinaban para establecer su exactitud, cuya hostilidad a las ideas más innovadoras de Hoyle hizo que éste dejara de presentar sus trabajos a los periódicos. Hoyle tuvo que pagar un precio por su rebeldía, cuando, en 1951, mientras él, permanecía obstinadamente entre bastidores, Ernest Opik y Edwin Sepeter hallaron la síntesis en las estrellas de átomos desde el Berilio hasta el Carbono. Lamentando la oportunidad perdida, Hoyle rompió entonces su silencio y en un artículo de 1954 demostró como las estrellas gigantes rojas podían corvertir Carbono en Oxígeno 16.

El Sol, dentro de 5.000 millones de años, será una Gigante roja primero y una enana blanca después
Pero, sigamos con la historia de Hoyle. Quedaba aún el obstáculo insuperable del hierro. El hierro es el más estable de todos los elementos; fusionar núcleos de hierro para formar nucleos de un elemento más pesado consume energía en vez de liberarla; ¿cómo, pues, podían las estrellas efectuar la fusión del hierro y seguir brillando? Hoyle pensó que las supernovas podían realizar la tarea, que el extraordinario calor de una estrella en explosión podía servir para forjar los elementos más pesados que el hierro, si el de una estrella ordinaria no podía. Pero no lo pudo probar.
Luego, en 1956, el tema de la producción estelar de elementos recibió nuevo ímpetu cuando el astrónomo norteamerciano Paul Merril identificó las reveladoras líneas del Tecnecio 99 en los espectros de las estrellas S. El Tecnecio 99 es más pesado que el hierro. También es un elemento inestable, con una vida media de sólo 200.000 años. Si los átomos de Tecnecio que Merril detectó se hubiesen originado hace miles de millones de años en el big bang, se habrían desintegrado desde entonces y quedarían hoy muy pocos de ellos en las estrellas S o en otras cualesquiera. Sin embargo, allí estaban. Evidentemente, las estrellas sabían como construir elementos más allá del hierro, aunque los astrofísicos no lo supiesen.
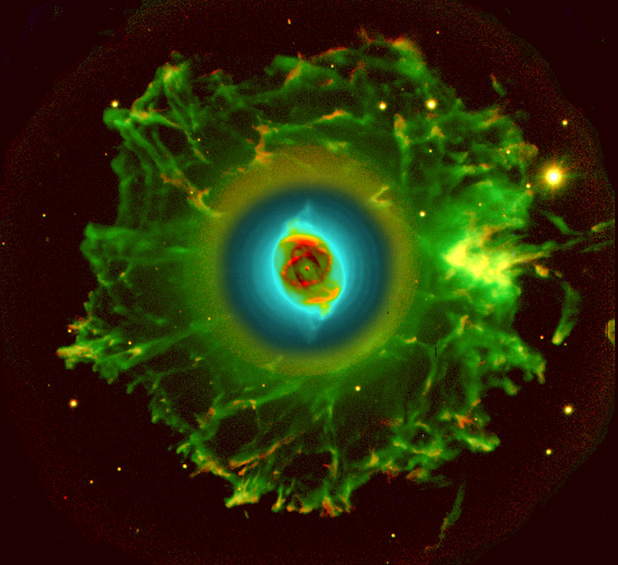
Estrella muy evolucionada que se transforma en otra cosa
Las estrellas de tecnecio son estrellas cuyo espectro revela la presencia del elemento tecnecio. Las primeras estrellas de este tipo fueron descubiertas en 1952, proporcionando la primera prueba directa de la nucleosíntesis estelar, es decir, la fabricación de elementos más pesados a partir de otros más ligeros en el interior de las estrellas. Como los isótopos más estables de tecnecio tienen una vida media de sólo un millón de años, la única explicación para la presencia de este elemento en el interior de las estrellas es que haya sido creado en un pasado relativamente reciente. Se ha observado tecnecio en algunas estrellas M, estrellas MS, estrellas MC, estrellas S, y estrellas C.

Estimulado por el descubrimiento de Merril, Hoyle reanudó sus investigaciones sobre la nucleosíntesisestelar. Era una tarea que se tomó muy en serio. De niño, mientras se ocultaba en lo alto de una muralla de piedra jugando al escondite, miró hacia lo alto, a las estrellas, y resolvió descubrior qué eran, y el astrofísico adulto nunca olvidó su compromiso juvenil. Cuando visitó el California Institute Of Technology, Hoyle estuvo en compañía de Willy Fowler, un miembro residetente de la facultad con un conocimiento enciclopédico de la física nuclear, y Geoffrey y Margaret Burbidge, un talentoso equipo de marido y mujer que, como Hoyle, eran excépticos ingleses en la relativo al big bang.
Hubo un cambio cuando Geoffrey Burbidge, examinando datos a los que recientemente se había eximido de las normas de seguridad de una prueba atómica en el atolón Bikini, observó que la vida media de uno de los elementos radiactivos producidos por la explosión, el californio 254, era de 55 días. Esto sonó familiar: 55 días era justamente el período que tardó en consumirse una supernova que estaba estudiando Walter Baade. El californio es uno de los elementos más pesados; si fuese creado en el intenso calor de estrellas en explosión, entonces, suguramente los elementos situados entre el hierro y el californio -que comprenden, a fin de cuentas, la mayoría de la Tabla Periódica- también podrían formarse allí. Pero ¿cómo?.

Nucleosíntesis estelar
Las estrellas que son unas ocho veces más masivas que el Sol representan sólo una fracción muy pequeña de las estrellas en una galaxia espiral típica. A pesar de su escasez, estas estrellas juegan un papel importante en la creación de átomos complejos y su dispersión en el espacio. Los elementos más complejos surgen a partir de las explosiones Supernovas.

Elementos necesarios como carbono, oxígeno, nitrógeno, y otros útiles, como el hierro y el aluminio. Elementos como este último, que se cocinan en estas estrellas masivas en la profundidad de sus núcleos estelares, puede ser gradualmente dragado hasta la superficie estelar y hacia el exterior a través de los vientos estelares que soplan impulsando los fotones. O este material enriquecido puede ser tirado hacia afuera cuando la estrella agota su combustible termonuclear y explota. Este proceso de dispersión, vital para la existencia del Universo material y la vida misma, puede ser efectivamente estudiado mediante la medición de las peculiares emisiones radiactivas que produce este material. Las líneas de emisión de rayos gamma del aluminio, que son especialmente de larga duración, son particularmente apreciadas por los astrónomos como un indicador de todo este proceso. El gráfico anterior muestra el cambio predicho en la cantidad de un isótopo particular de aluminio, Al26, para una región de la Vía Láctea, que es particularmente rica en estrellas masivas. La franja amarilla es la abundancia de Al 26 para esta región según lo determinado por el laboratorio de rayos gamma INTEGRAL. La coincidencia entre la abundancia observada y la predicha por el modelo re-asegura a los astrónomos de nuestra comprensión de los delicados lazos entre la evolución estelar y la evolución química galáctica.
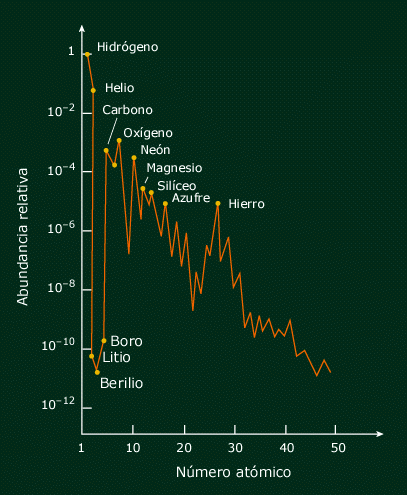
Pero sigamos con la historia recorrida por Hoyle y sus amigos. Felizmente, la naturaleza proporcionó una piedra Rosetta con la cual Hoyle y sus colaboradores podían someter a prueba sus ideas, en la forma de curva cósmica de la abundancia. Ésta era un gráfico del peso de los diversos átomos -unas ciento veinte especies de núcleos, cuando se tomaban en cuanta los isótopos- en función de su abundancia relativa en el universo, establecido por el estudio de las rocas de la Tierra, meteoritos que han caido en la Tierra desde el espacio exterior y los espectros del Sol y las estrellas.

Supernova que calcina a un planeta cercano. Ahí, en esa explosión se producen transiciones de fase que producen materiales pesados y complejos. En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es: H, He, (Li, Be, B) C, N, O… Fe.
¿Apreciáis la maravilla?

Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del universo y… de la vida inteligente. Esos materiales para la vida sólo se pudieron fabricar el las estrellas, en sus hornos nucleares y en las explosiones supernovas al final de sus vidas. Esa era la meta de Hoyle, llegar a comprender el proceso y, a poder demostrarlo.
“El problema de la síntesis de elementos -escribieron- está estrechamente ligado al problema de la evolución estelar.” La curva de abundancia cósmica de elementos que mostraba las cantidades relativas de las diversas clases de átomos en el universo a gran escala. Pone ciertos límites a la teoría de cómo se formaron los elementos, y, en ella aparecen por orden creciente:
Como reseñamos antes la lista sería Hidrógeno, Helio, Carbono, Litio, Berilio, Boro, Oxígeno, Neón, Silicio, Azufre, Hierro (damos un salto), Plomo, Torio y Uranio. Las diferencias de abundancias que aparecen en los gráficos de los estudios realizados son grandes -hay, por ejemplo, dos millones de átomos de níquel por cada cuatro átomos de plata y cincuenta de tunsgteno en la Via Láctea- y por consiguiente la curva e abundancia presenta una serie de picos dentados más accidentados que que la Cordillera de los Andes. Los picos altos corresponden al Hidrógeno y al Helio, los átomos creados en el big bang -más del p6 por ciento de la materia visible del universo- y había picos menores pero aún claros para el Carbono, el Oxígeno, el Hierro y el Plamo. La acentuada claridad de la curva ponía límites definidos a toda teoría de la síntesis de elementos en las estrellas. Todo lo que era necesario hacer -aunque dificultoso) era identificar los procesos por los cuales las estrellas habían llegado preferentemente a formar algunos de los elementos en cantidades mucho mayores que otros. Aquí estaba escrita la genealogía de los átomos, como en algún jeroglífico aún no traducido: “La historia de la materia éscribió Hoyle, Fwler y los Burbidge_…está oculta en la distribuciíon de la anundancia de elementos”
En el Big Bang: Hidrógeno, Helio, Litio.
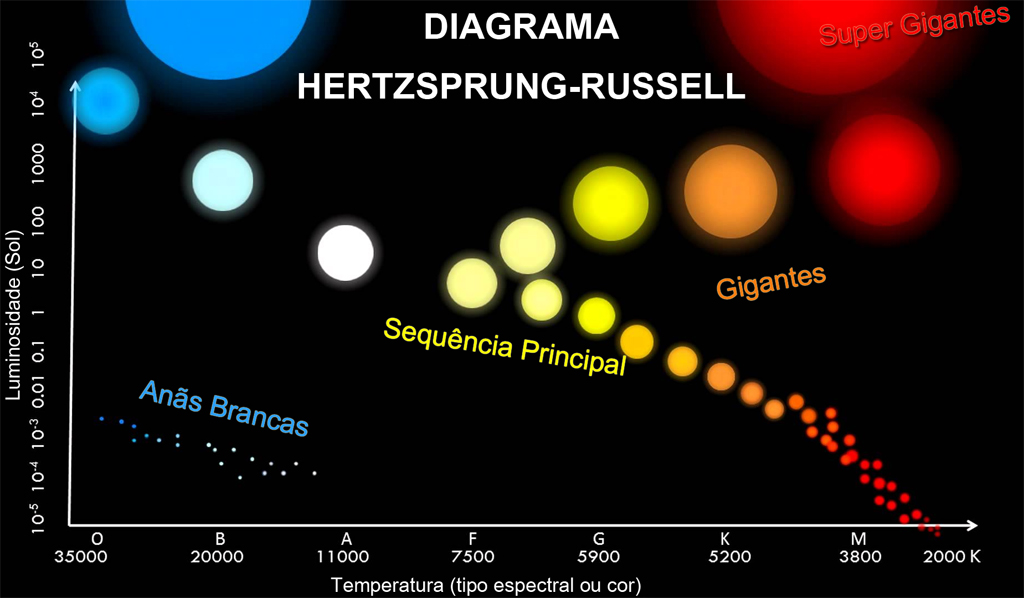
En las estrellas de la serie principal: Carbono, Nitrógeno, Oxígeno.
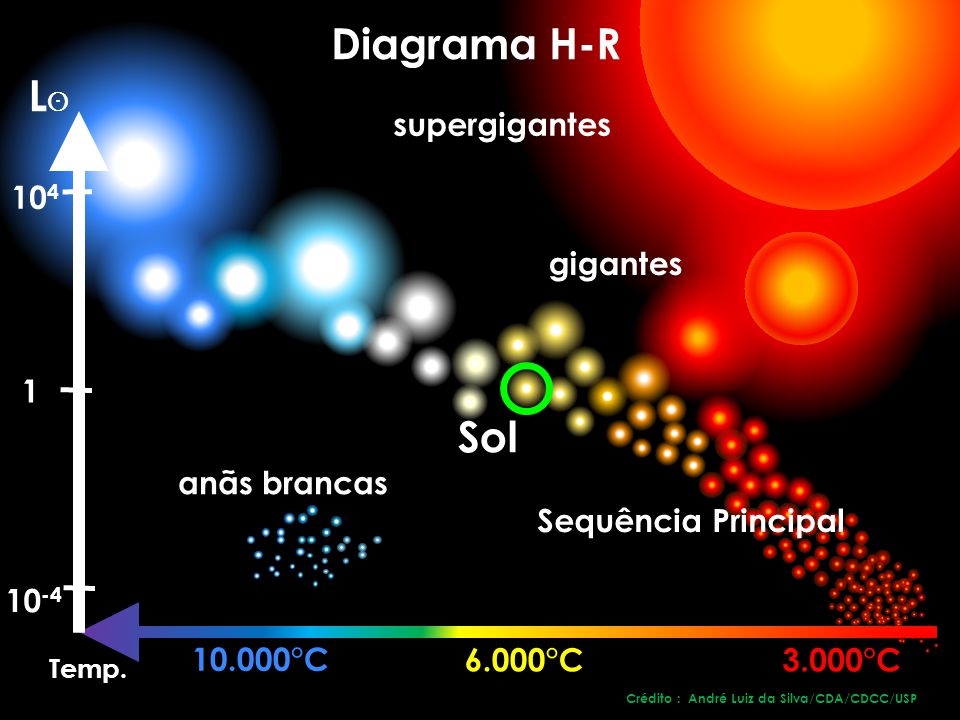
En las estrellas moribundas: Sodio, Magnesio, Aluminio, Silicio, Azufre, Cloro, Argón, Potasio, Titanio, Hierro, Cobalto, Níquel, Cobre, Cinc, Plomo, Torio y Uranio.
Como habeis podido comprobar, nada sucede por que sí, todo tiene una explicación satisfactoria de lo que, algunas veces, decimos que son misterios escondidos de la Naturaleza y, sin embargo, simplemente se trata de que, nuestra ignorancia, no nos deja llegar a esos niveles del saber que son necesarios para poder explicar algunos fenómenos naturales que, exigen años de estudios, observaciones, experimentos y, también, mucha imaginación.

En la imagen de arriba se refleja el proceso Triple Alpha descubierto por Hoyle:
Amigos míos, son las 5,53 h., me siento algo cansado de teclear y me parece que con los datos aquí expuestos podéis tener una idea bastante buena de la formación de elementos en el cosmos y de cómo las estrellas son las máquinas creadoras de la materia cada vez más compleja y, el Universo, nos muestra de qué mecanismos se vale para poder traer elementos que más tarde formarán parte de los planetas, de los objetos en ellos presentes y, de la Vida.
emilio silvera
Oct
26
Ya podemos “viajar” desde el núcleo atómico hasta las...
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astronomía y Astrofísica ~
Clasificado en Astronomía y Astrofísica ~
 Comments (1)
Comments (1)
Interacciones fundamentales

Existen en el Universo cuatro fuerzas fundamentales (al menos son las que hasta el momento conocemos), éstas cuatro fuerzas son las que rigen en todas las regiones del Universo y, junto a las constantes universales, hacen que el Universo sea tal como lo podemos observar. Le dan un ritmo a los objetos que lo pueblan y, ya pueden estar conformados por “materia inerte” y tratarse de seres vivos, todo responde a sus mandatos y de acuerdo a ellos se comportan.
Nada de lo que sucede en el Universo es “porque sí”, todo tiene su por qué. Nos ha costado miles de años de pensamientos, de estudios, de observaciones, de experimentos y de experiencia el llegar a conocer, en cierta medida, como funciona la Naturaleza.
En un Tiempo Pasado, algunos optimistas decían: “Ya nada nuevo podemos aprender, sabemos el origen y el por qué de todas las cosas”. Aquellos pobres ilusos, en realidad, eran unos grandes ignorantes que no eran conscientes de lo mucho que nos quedaba por saber. Las preguntas siguen siendo mucho más abundantes que las respuestas.
El propio Rutherford empezó a vislumbrar la respuesta a la que arriba hacemos. Entre 1.906 y 1.908 (hace más de un siglo) realizó constantes experimentos disparando partículas alfa contra una lámina sutil de metal (como oro o platino), para analizar sus átomos. La parte de los proyectiles atravesaron la barrera sin desviarse (como balas a través de las hojas de un árbol), pero no todos.
En la placa fotográfica que le sirvió de blanco tras el metal, Rutherford descubrió varios impactos dispersos e insospechados alrededor del punto central. Comprobó que algunas partículas habían rebotado. Era como si en vez de atravesar las hojas, algunos proyectiles hubiesen chocado contra algo más sólido. Rutherford supuso que aquella “balas” habían chocado contra una especie de núcleo denso, que ocupaba sólo una parte mínima del volumen atómico y ese núcleo de intensa densidad desviaban los proyectiles que acertaban a chocar contra él. Ello ocurría en muy raras ocasiones, lo cual demostraba que los núcleos atómicos debían ser realmente ínfimos, porque un proyectil había de por fuerza muchos millones de átomos al atravesar la lámina metálica
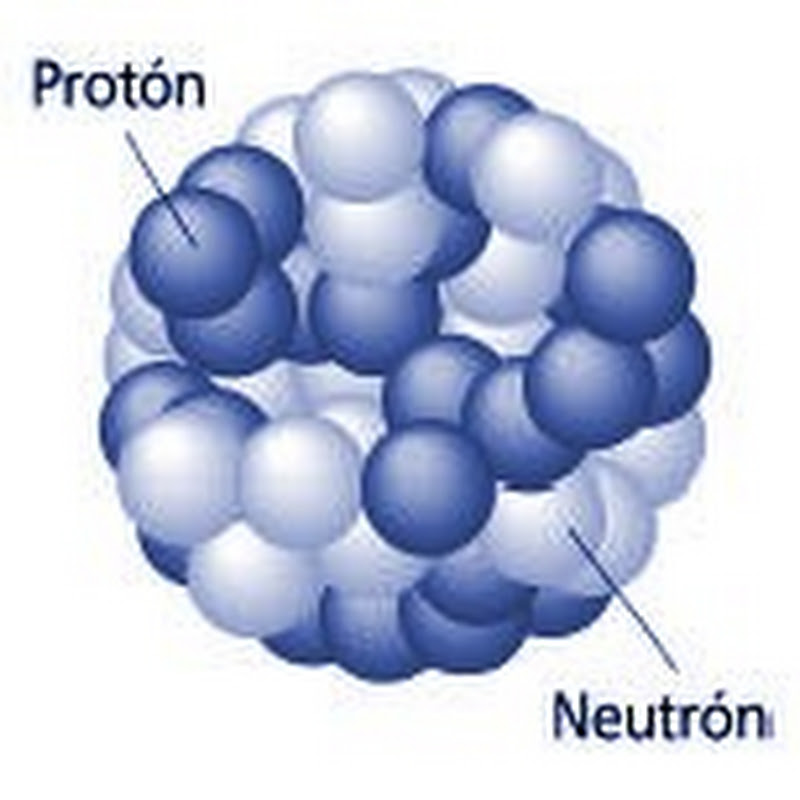
Era lógico , pues, que los protones constituían ese núcleo duro. Rutherford representó los protones atómicos como elementos apiñados alrededor de un minúsculo “núcleo atómico” que servía de centro (después de todo eso, hemos podido que el diámetro de ese núcleo equivale a algo más de una cienmilésima del volumen total del átomo).
En 1.908 se concedió a Rutherford el premio Nobel de Química por su extraordinaria labor de investigación sobre la naturaleza de la materia. Él fue el de importantes descubrimientos que permitieron conocer la estructura de los átomos en esa primera avanzadilla.
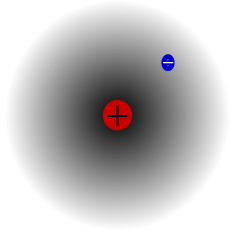
Átomo de hidrógeno, núcleo y electrón.
Desde entonces se pueden describir con términos más concretos los átomos específicos y sus diversos comportamientos. Por ejemplo, el átomo de hidrógeno posee un solo electrón. Si se elimina, el protónrestante se asocia inmediatamente a alguna molécula vecina; y cuando el núcleo desnudo de hidrógeno no encuentra por este medio un electrón que participe, actúa como un protón (es decir, una partícula subatómica), lo cual le permite penetrar en la materia y reaccionar con otros núcleos si conserva la suficiente energía.
El helio, que posee dos electrones, no cede uno con tanta facilidad. Sus dos electrones un caparazón hermético, por lo cual el átomo es inerte. No obstante, si se despoja al helio de ambos electrones, se convierte en una partícula alfa, es , una partícula subatómica portadora de dos unidades de carga positiva.

Hay un tercer elemento, el litio, cuyo átomo tiene electrones. Si se despoja de uno o dos, se transforma en ión, y si pierde los tres, queda reducida a un núcleo desnudo, con una carga positiva de tres unidades.
Las unidades de carga positiva en el núcleo atómico deben ser numéricamente idénticas a los electronesque contiene por norma, pues el átomo suele ser un cuerpo neutro, y esta igualdad de lo positivo con lo negativo es el equilibrio. De hecho, los números atómicos de sus elementos se basan en sus unidades de carga positiva, no en las de carga negativa, porque resulta fácil hacer variar el de electrones atómicos dentro de la iónica, pero en cambio se encuentran grandes dificultades si se desea alterar el número de sus protones.

Apenas esbozado este esquema de la construcción atómica, surgieron nuevos enigmas. El de unidades con carga positiva en un núcleo no equilibró, en ningún caso, el peso nuclear ni la masa, exceptuando el caso del átomo de hidrógeno. Para citar un ejemplo, se averiguó que el núcleo de helio tenía una carga positiva dos veces mayor que la del núcleo de hidrógeno; pero como ya se sabía, su masa era cuatro veces mayor que la de este último. Y la situación empeoró progresivamente a medida que se descendía por la tabla de elementos, e incluso cuando se alcanzó el uranio, se encontró un núcleo con una masa igual a 238 protones, pero una carga que equivalía sólo a 92.
¿Cómo era posible que un núcleo que contenía cuatro protones (según se suponía el núcleo de helio) tuviera sólo dos unidades de carga positiva? Según la más y primera conjetura emitida, la presencia en el núcleo de partículas cargadas negativamente y con peso despreciable neutralizaba dos unidades de carga. Como es natural, se pensó también en el electrón. Se podría componer el rompecabezas si se suponía que en núcleo de helio estaba integrado por cuatro protones y dos electronesneutralizadores, lo cual deja libre una carga positiva neta de dos, y así sucesivamente, hasta llegar al uranio, cuyo núcleo tendría, pues, 238 protones y 146 electrones, con 92 unidades libres de carga positiva. El hecho de que los núcleos radiactivos emitieran electrones (según se había comprobado ya, por ejemplo, en el caso de las partículas beta), reforzó esta idea . Dicha teoría prevaleció durante más de una década, hasta que por caminos indirectos, llegó una respuesta mejor como resultado de otras investigaciones.
Pero entre tanto se habían presentado algunas objeciones rigurosas contra dicha hipótesis. Por lo , si el núcleo estaba constituido esencialmente de protones, mientras que los ligeros electrones no aportaban prácticamente ninguna contribución a la masa, ¿cómo se explicaba que las masas relativas de varios núcleos no estuvieran representadas por enteros? Según los pesos atómicos conocidos, el núcleo del átomo cloro, por ejemplo, tenía una masa 35’5 veces mayor que la del núcleo de hidrógeno. ¿Acaso significaba esto que contenía 35’5 protones? Ningún científico (ni entonces ni ahora) podía aceptar la existencia de medio protón.
Este singular interrogante encontró una respuesta incluso antes de solventar el problema , y ello dio lugar a una interesante historia.

Los tres isótopos naturales del carbono: carbono-12 (6 protones y 6 neutrones), carbono-13 (6 protones y 7 neutrones) y carbono-14 (6 protones y 8 neutrones). En los tres casos es carbono, tiene el aspecto de carbono y se comporta químicamente como carbono, por tener seis protones (y forma parte de nuestro organismo, por ejemplo). Sin embargo, sus propiedades físicas varían. Por ejemplo, mientras que el carbono-12 y el carbono-13 son estables, el carbono-14 es inestable y radioactivo: emite radiación beta, uno de sus neutrones “extras” se transforma así en un protón y el núcleo se convierte en nitrógeno-14 (que tiene 7 protones y 7 neutrones), con el aspecto y las propiedades del nitrógeno (por tener 7 protones). Dado que la mitad de la masa del carbono-14 pasa a ser nitrógeno-14 cada 5.730 años aproximadamente (más o menos lo que llevamos de civilización humana), la presencia de este isótopo natural resulta especialmente útil para la datación precisa de objetos históricos.
Isótopos; construcción de bloques uniformes
Allá por 1.816, el físico inglés William Prout había insinuado ya que el átomo de hidrógeno debía en la constitución de todos los átomos. Con el tiempo se fueron desvelando los pesos atómicos, y la teoría de Prout quedó arrinconada, pues se comprobó que muchos elementos tenían pesos fraccionarios (para lo cual se tomó el oxígeno, tipificado al 16). El cloro, según dije antes, tiene un peso atómico aproximado de 35’5, o para ser exactos, 35’457. otros ejemplos son el antimonio, con un peso atómico de 121’75, el galio con 137’34, el boro con 10’811 y el cadmio con 112’40.

El Uranio 235 que es el único que de manera natural es apto para la fisión nuclear, es escaso, sólo el 7 por 1.000 es uranio 235, el , es uranio 238 que, no es combustible nuclear y, como la madera mojada, no arde. Sin embargo, si se bombardea con neutrones lentos del uranio 235, resulta que se convierte en Plutonio 239 que sí, es combustible nuclear válido. ¡Qué no idearemos para los objetivos!
El Uranio es muy radiactivo y si está enriquecido… ¡Ya sabemos las consecuencias!
Hacia principios de siglo se hizo una de observaciones desconcertantes, que condujeron al esclarecimiento. El inglés William Crookes (el del tubo Crookes) logró disociar del uranio una sustancia cuya ínfima cantidad resultó ser mucho más radiactiva que el propio uranio. Apoyándose en su experimento, afirmó que el uranio no tenía radiactividad, y que ésta procedía exclusivamente de dicha impureza, que él denominó uranio X. Por otra parte, Henri Becquerel descubrió que el uranio purificado y ligeramente radiactivo adquiría mayor radiactividad con el tiempo, por causas desconocidas. Si se deja reposar durante algún tiempo, se extraer de él repetidas veces uranio activo X. Para decirlo de otra manera, por su propia radiactividad, el uranio se convertía en el uranio X, más radiactivo aún.
Por entonces, Rutherford, a su vez, separó del torio un torio X muy radiactivo, y comprobó también que el torio seguía produciendo más torio X. Hacia aquellas fechas se sabía ya que el más famoso de los elementos radiactivos, el , emitía un gas radiactivo, denominado radón. Por tanto, Rutherford y su ayudante, el químico Frederick Soddy, dedujeron que durante la emisión de sus partículas los átomos radiactivos se transformaron en otras variedades de átomos radiactivos.
El Radón, uno de los llamados gases nobles, es incoloro, inodoro e insípido, además de –para nuestro mal- radioactivo. Suele presentarse según el tipo de suelos de determinadas zonas y con la descomposición de uranio, concentrándose en la superficie y siendo “arrastrado” en y por el aire que respiramos, y es en grandes cantidades es un gas perjudicial para la salud… y que anticipa terremotos.

químicos que investigaron tales transformaciones lograron obtener un surtido muy variado de nuevas sustancias, a las que dieron nombres tales como A, B, mesotorio I, mesotorio II y actinio C. Luego los agruparon todos en tres series, de acuerdo con sus historiales atómicos. Una serie se originó del uranio disociado; otra del torio, y la tercera del actinio (si bien más tarde se encontró un predecesor del actinio, llamado protactinio).
En total se identificaron unos cuarenta miembros de esas series, y cada uno se distinguió por su peculiar esquema de radiación. Pero los finales de las tres series fueron idénticos: en último término, todas las cadenas de sustancias conducían al mismo elemento, el plomo.
Ahora bien, esas cuarenta sustancias no podían ser, sin excepción, elementos disociados. Entre el uranio (92) y el plomo (82) había sólo diez lugares en la tabla periódica, y todos ellos, salvo dos, pertenecían a elementos conocidos.
En realidad, los químicos descubrieron que aunque las sustancias diferían entre sí por su radiactividad, algunas tenían propiedades químicas idénticas. Por ejemplo, ya en 1.907 los químicos americanos Herbert Newby McCoy y W. H. Ross descubrieron que el radiotorio (uno entre los varios de la desintegración del torio) mostraba el mismo comportamiento químico que el torio, y el D, el mismo que el plomo, tanto que a veces era llamado radioplomo. De todo lo cual se infirió que tales sustancias eran en realidad variedades de mismo elemento: el radiotorio, una forma de torio; el radioplomo, un miembro de una familia de plomos; y así sucesivamente.
En 1.913, Soddy esclareció esta idea y le dio más amplitud. Demostró que cuando un átomo emitía una partícula alfa, se transformaba en un elemento que ocupaba dos lugares más abajo en la lista de elementos, y que cuando emitía una partícula beta, ocupaba, después de su transformación, el lugar inmediatamente . Con arreglo a tal norma, el radiotorio descendía en la tabla hasta el lugar del torio, y lo mismo ocurría con las sustancias denominadas uranio X y uranio Y, es decir, que los tres serían variedades del elemento 90. Así mismo, el radio D, el radio B, el torio B y el actinio B compartirían el lugar del plomo como variedades del elemento 82.
Soddy dio el de isótopos (del griego iso y topos, “el mismo lugar”) a todos los miembros de una familia de sustancias que ocupaban el mismo lugar en la tabla periódica. En 1.921 se le concedió el premio Nobel de Química.
El modelo protón–electrón del núcleo concordó perfectamente con la teoría de Soddy sobre los isótopos. Al retirar una partícula alfa de un núcleo, se reducía en dos unidades la carga positiva de dicho núcleo, exactamente lo que necesitaba para bajar dos lugares en la tabla periódica. Por otra parte, cuando el núcleo expulsaba un electrón (partícula beta), quedaba sin neutralizar un protón adicional, y ello incrementaba en una unidad la carga positiva del núcleo, lo cual era como agregar una unidad al atómico, y por tanto, el elemento pasaba a ocupar la posición inmediatamente superior en la tabla periódica de los elementos. ¡Maravilloso!
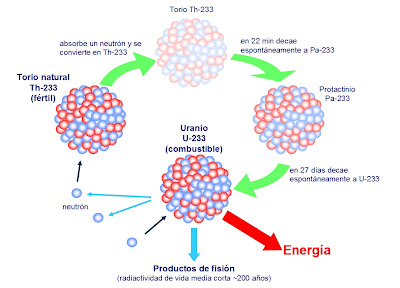
¿Cómo se explica que cuando el torio se descompone en radiotorio después de sufrir no una, sino tres desintegraciones, el producto siga siendo torio? Pues bien, en este proceso el átomo de torio pierde una partícula alfa, luego una partícula beta, y más tarde una segunda partícula beta. Si aceptamos la teoría sobre el bloque constitutivo de los protones, ello significa que el átomo ha perdido cuatro electrones (dos de ellos contenidos presuntamente en la partícula alfa) y cuatro protones. (La situación actual difiere bastante de este , aunque en cierto modo, esto no afecta al resultado).
El núcleo de torio constaba inicialmente (según se suponía) de 232 protones y 142 electrones. Al haber perdido cuatro protones y otros cuatro electrones, quedaba reducido a 228 protones y 138 electrones. No obstante, conservaba todavía el atómico 90, es decir, el mismo de antes.
Así pues, el radiotorio, a semejanza del torio, posee 90 electrones planetarios, que giran alrededor del núcleo. Puesto que las propiedades químicas de un átomo están sujetas al de sus electronesplanetarios, el torio y el radiotorio tienen el mismo comportamiento químico, sea cual fuere su diferencia en peso atómico (232 y 228 respectivamente).
Los isótopos de un elemento se identifican por su peso atómico, o número másico. Así, el torio corriente se denomina torio 232, y el radiotorio, torio 228. Los isótopos radiactivos del plomo se distinguen también por estas denominaciones: plomo 210 (radio D), plomo 214 (radio B), plomo 212 (torio B) y plomo 211 (actinio B).

Se descubrió que la noción de isótopo podía aplicarse indistintamente tanto a los elementos estables como a los radiactivos. Por ejemplo, se comprobó que las tres series radiactivas anteriormente mencionadas terminaban en tres formas distintas de plomo. La serie del uranio acababa en plomo 206, la del torio en plomo 208 y la del actinio en plomo 207. cada uno de estos era un isótopo estable y corrientedel plomo, pero los tres plomos diferían por su peso atómico.
Mediante un dispositivo inventado por cierto ayudante de J. J. Thomson, llamado Francis William Aston, se demostró la existencia de los isótopos estables. En 1.919, Thomson, empleando la versión primitiva de aquel artilugio, demostró que el neón estaba constituido por dos variedades de átomos: una cuyo de masa era 20, y otra con 22. El neón 20 era el isótopo común; el neón 22 lo acompañaba en la proporción de un átomo cada diez. Más tarde se descubrió un tercer isótopo, el neón 21, cuyo porcentaje en el neón atmosférico era de un átomo por cada 400.
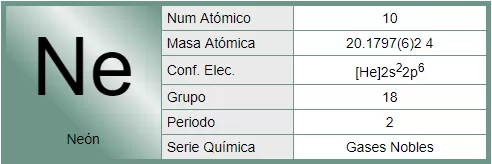
Entonces fue posible, al fin, razonar el peso atómico fraccionario de los elementos. El peso atómico del neón (20, 183) representaba el peso conjunto de los tres isótopos, de pesos diferentes, que integraban el elemento en su estado natural. Cada átomo individual tenía un másico entero, pero el promedio de sus masas (el peso atómico) era un número fraccionario.
Aston procedió a que varios elementos estables comunes eran, en realidad, mezclas de isótopos. Descubrió que el cloro, con un peso atómico fraccionario de 35’453, estaba constituido por el cloro 35 y el cloro 37, en la proporción de cuatro a uno. En 1.922 se le otorgó el premio Nobel de Química.

Sabiendo todo lo anteriormente explicado, hemos llegado a comprender cómo parte de la Astronomía que estudia las características físicas y químicas de los cuerpos celestes, la astrofísica es la parte más de la astronomía en la actualidad debido a que, al avanzar la física moderna: Efecto Doppler-Fizeau, el efecto Zeeman, las teorías cuánticas y las reacciones termonucleares aplicadas al estudio de los cuerpos celestes han permitido descubrir que el magnético solar, el estudio de las radiaciones estelares y sus procesos de fusión nuclear, y determinar la velocidad radial de las estrellas, etc. La radiación electromagnética de los cuerpos celestes permite realizar análisis de los espectros que nos dicen de qué están hechas las estrellas y los demás cuerpos del espacio interestelar y, de esa manera, hemos ido conociendo la materia y sus secretos que cada vez, van siendo menos.
emilio silvera
















 Totales: 75.502.921
Totales: 75.502.921 Conectados: 31
Conectados: 31





















