Mar
10
¿Tiempo de Planck? ¡Qué no imaginará el hombre!
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en General ~
Clasificado en General ~
 Comments (9)
Comments (9)
Es el tiempo que necesita el fotón (viajando a la velocidad de la luz, c, para moverse a través de una distancia igual a la longitud de Planck. Está dado por ![]() segundos, donde G es la constante gravitacional (6’672 59 (85) ×10-11 N m2 kg-2), ħ es la constante de Planck racionalizada (ħ = h/2π = 1’054589 × 10-34 Julios segundo) y c es la velocidad de la luz (299.792.458 m/s).
segundos, donde G es la constante gravitacional (6’672 59 (85) ×10-11 N m2 kg-2), ħ es la constante de Planck racionalizada (ħ = h/2π = 1’054589 × 10-34 Julios segundo) y c es la velocidad de la luz (299.792.458 m/s).
El valor del tiempo del Planck es del orden de 10-43 segundos. En la cosmología del Big Bang, hasta un tiempo Tp después del instante inicial, es necesaria usar una teoría cuántica de la gravedad para describir la evolución del universo.
Expresado en números corrientes que todos podamos entender, su valor es 0’0000000000000000000000000000000000000000010 de 1 segundo, que es el tiempo que necesita el fotón para recorrer la longitud de Planck, de 10-35 metros (veinte ordenes de magnitud menor que el tamaño del protón de 10-15 metros). El límite de Planck es ![]()
Todo, desde Einstein, es relativo. Depende de la pregunta que se formule y de quién nos de la respuesta.
Mar
10
De materiales y radiaciones (La imaginación del Ser Humano)
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)
Uranio 233
Uranio 235
Uranio 238
Plutonio 239
Al pensar en la desintegración me ha traído a la memoria otros materiales que también se desintegran de manera natural y que son materiales fértiles, o que sin serlo, se pueden transformar en otros que sí lo son.
Al hablar de material fértil me estoy refiriendo a núclidos que pueden absorber neutrones para formar material fisible. El uranio-238, por ejemplo, absorbe un neutrón para formar uranio-239, que se desintegra en plutonio-239. Este es el tipo de conversión que la imaginación del hombre hace que ocurra en un reactor reproductor.
Lo explicaré con más detalles:
El uranio-235 es un combustible práctico, es decir, los neutrones lentos son capaces de hacer que el uranio-235 se fisione, o lo que es lo mismo, se rompan sus átomos en dos, produciendo neutrones lentos, que a su vez inducen otras fisiones atómicas. El uranio-233 y el plutonio-239 son también combustibles nucleares prácticos por las mismas razones.
Desgraciadamente, el uranio-233 y el plutonio-239 no existen en estado natural sino en trazas mínimas, y el uranio-235, aunque existe en cantidades apreciables, no deja de ser raro. En cualquier muestra de uranio natural, sólo siete de cada mil átomos son de uranio-235, el resto es uranio-238.
Mar
10
Algún día sabremos lo que la Materia es
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)
AVANCES DE LA HUMANIDAD
William Crookes, 1906
Fue un químico inglés, uno de los científicos más importantes en Europa del siglo XIX, tanto en el campo de la física como en el de la química. En 1863 ingresó en la Royal Society, y fue nombrado Sir en 1910.
Tubo de rayos catódicos
Es conocido por ser el inventor del tubo de rayos catódicos, por el descubrimiento del elemento Talio, y por ser el primero en analizar el gas Helio en laboratorio.
Uranio X
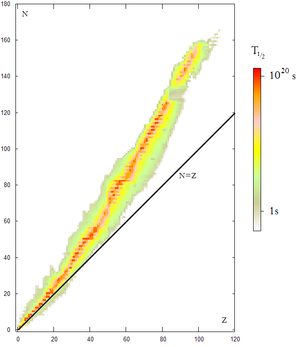
“Diagrama de Segrè. El color indica el periodo de semidesintegración de los isótopos radiactivos conocidos, también llamado semivida. Obsérvese que un ligero exceso de neutrones favorece la estabilidad en átomos pesados.”
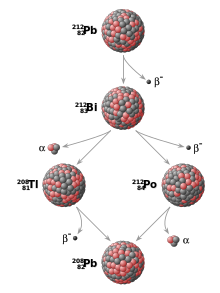
Productos de decaimiento intermedios de la cadena de desintegración desde plomo 212 hasta plomo 208.
En este ejemplo:
- 234Th, 234mPa,…,206Pb son los productos de decaimiento de 238U.
- 234Th es el hijo del padre 238U.
- 234mPa (234 metaestable) es el nieto de 238U.
A estos isótopos podría denominárseles también productos hijos de 238U.
Los productos de decaimiento son importantes para comprender la desintegración radiactiva y la administración de rediduos radiactivos.

Producción y gestión de residuos en una central nuclear.
El Uranio X
Antigua denominación radioquímica del nucleido 234Th, de la serie radiactiva natural del uranio. Su símbolo era UX1
Ha pasado más de un siglo desde que se hicieron una serie de observaciones desconcertantes, que condujeron al esclarecimiento. El inglés William Crookes (el del “tubo Crookes”) logró disociar del uranio una sustancia cuya ínfima cantidad resultó ser mucho más radiactiva que el propio uranio. Apoyándose en su experimento, afirmó que el uranio no tenía radiactividad, y que esta procedía exclusivamente de dicha impureza, que él denomino “uranio X”.
| Protactinio ← Uranio → Neptunio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
“El uranio es un elemento químico metálico de color plateado-grisáceo de la serie de los actínidos, su símbolo químico es U y su número atómico es 92. Por ello posee 92 protones y 92 electrones, con una valencia de 6. Su núcleo puede contener entre 142 y 146 neutrones, sus isótopos más abundantes son el 238U que posee 146 neutrones y el 235U con 143 neutrones. El uranio tiene el mayor peso atómico de entre todos los elementos que se encuentran en la naturaleza. El uranio es aproximadamente un 70 % más denso que el plomo, aunque menos denso que el oro o el wolframio. Es levemente radiactivo. Fue descubierto como óxido en 1789 por M. H. Klaproth que lo llamó así en el honor del planeta Urano que acababa de ser descubierto en 1781.”

Antoine Henri Becquerel
Por otra parte, Henri Becquerel descubrió que el uranio purificado y ligeramente radiactivo adquiría mayor radiactividad con el tiempo, por causas desconocidas. Si se dejan reposar durante algún tiempo, se podía extraer de él repetidas veces uranio activo X. Para decirlo de otra manera: por su propia radiactividad, el uranio se convertía en el uranio X, más activo aún.
Rutherford
Por entonces, Rutherford, a su vez, separó del torio un “torio X” muy radiactivo, y comprobó también que el torio seguía produciendo más torio X. Hacia aquellas fechas se sabía ya que el más famoso de los elementos radiactivos, el radio, emitía un gas radiactivo, denominado radón. Por tanto, Rutherford y su ayudante, el químico Frederick Soddy, dedujeron que, durante la emisión de sus partículas, los átomos radiactivos de transformaban en otras variedades de átomos radiactivos.
Actinio Torio
Varios químicos, que investigaron tales transformaciones, lograron obtener un surtido muy variado de nuevas sustancias, a los que dieron nombres tales como radio A, radio B, mesotorio I, mesotorio II y Actinio C. Luego los agruparon todos en tres series, de acuerdo con sus historiales atómicos. Una serie de originó del uranio disociado; otra, del torio, y la tercera, del actinio (si bien más tarde se encontró un predecesor del actinio, llamado “protactinio”).
















 Totales: 75.499.071
Totales: 75.499.071 Conectados: 37
Conectados: 37