Feb
21
Surgieron pensamientos… ¡Que nunca dejaran de asombrarnos!
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)

Ludwig Boltzmann será el protagonista de hoy
“En resumen, la fórmula de Boltzmann muestra la relación entre la entropía y el número de formas en que se pueden organizar los átomos o moléculas de un sistema termodinámico.”
Hay ecuaciones que son aparentemente insignificantes por su reducido número de exponentes que, sin embargo, ¡dicen tantas cosas…! En la mente de todos están las sencillas ecuaciones de Einstein y de Planck sobre la energía-masa y la radiación de cuerpo negro. Esa es la belleza de la que hablan los físicos cuando se refieren a “ecuaciones bellas”. La de arriba de Boltzmann tampoco se queda atrás.

Maxwell

Las ecuaciones de Maxwell…, “y se hizo la luz”
La identidad de Euler: Algunos dijeron de su ecuación: “la expresión matemática más profunda jamás escrita”, “misteriosa y sublime”, “llena de belleza cósmica”, “una explosión cerebral”.

Newton y su segunda ley que, aunque no funcione cuando nos acercamos a velocidades relativistas, rompió la marcha hacia la Gravedad.

Pitágoras y “su” teorema, también debe estar presente como lo está su teorema en las construcciones de todo el mundo y… mucho más.

Schrödinger y su función de onda que tampoco se queda atrás (aunque como la ecuación de Newton, si hablamos de velocidades relativistas…)
Bueno, E = mc2, nos lleva a profundidades de la materia antes jamás vistas y nos permite sacar conclusiones como que, en un gramo de materia está encerrada toda la energía consumida por la Humanidad durante un minuto. ¡Masa y Energía son la misma cosa!
Einstein, con su ecuación de campo de la relatividad general, vino a cambiar el mundo y, a partir de entonces, nació la verdadera cosmología. ¡Nos habla de tantas cosas!
¿Qué decir de la maravillosa fórmula de la entropía de Boltzman? (insisto de nuevo).
S = k log W
“Esta ecuación, conocida como la fórmula de entropía de Boltzmann , relaciona los detalles microscópicos, o microestados, del sistema (a través de W ) con su estado macroscópico (a través de la entropía S ). Es la idea clave de la mecánica estadística. En un sistema cerrado, la entropía nunca disminuye, por lo que en el Universo la entropía aumenta irreversiblemente. En un sistema abierto (por ejemplo, un árbol en crecimiento), la entropía puede disminuir y el orden puede aumentar, pero solo a expensas de un aumento de la entropía en otro lugar (por ejemplo, en el Sol).”
Creo que hoy, hablaremos de esta ecuación azul que arriba podéis contemplar. Boltzman con su trabajo e ingenio, le dio a la Humanidad la herramienta para que pudiera seguir avanzando en el difícil laberinto de la Cienca, fue, sin duda, uno de los físicos más ilustres del siglo XIX.
El trabajo científico desarrollado por Boltzmann en su época crítica de transición que puso el colofón a la física “clásica” –cuya culminación podríamos situar en Maxwell– y antecedió (en pocos años) a la “nueva” física, que podemos decir que comenzó con Max Planck y Einstein. Aunque ciertamente no de la importancia de los dos últimos, la labor científica de Boltzmann tiene una gran relevancia, tanto por sus aportaciones directas (creador junto con “su amigo” Maxwell y Gibbs de la mecánica estadística, aunque sea el formulismo de éste último el que finalmente haya prevalecido; esclarecedor del significado de la entropía, etc.) como por la considerable influencia que tuvo en ilustres físicos posteriores a los que sus trabajos dieron la inspiración, como es el caso de los dos mencionados, Planck y Einstein.
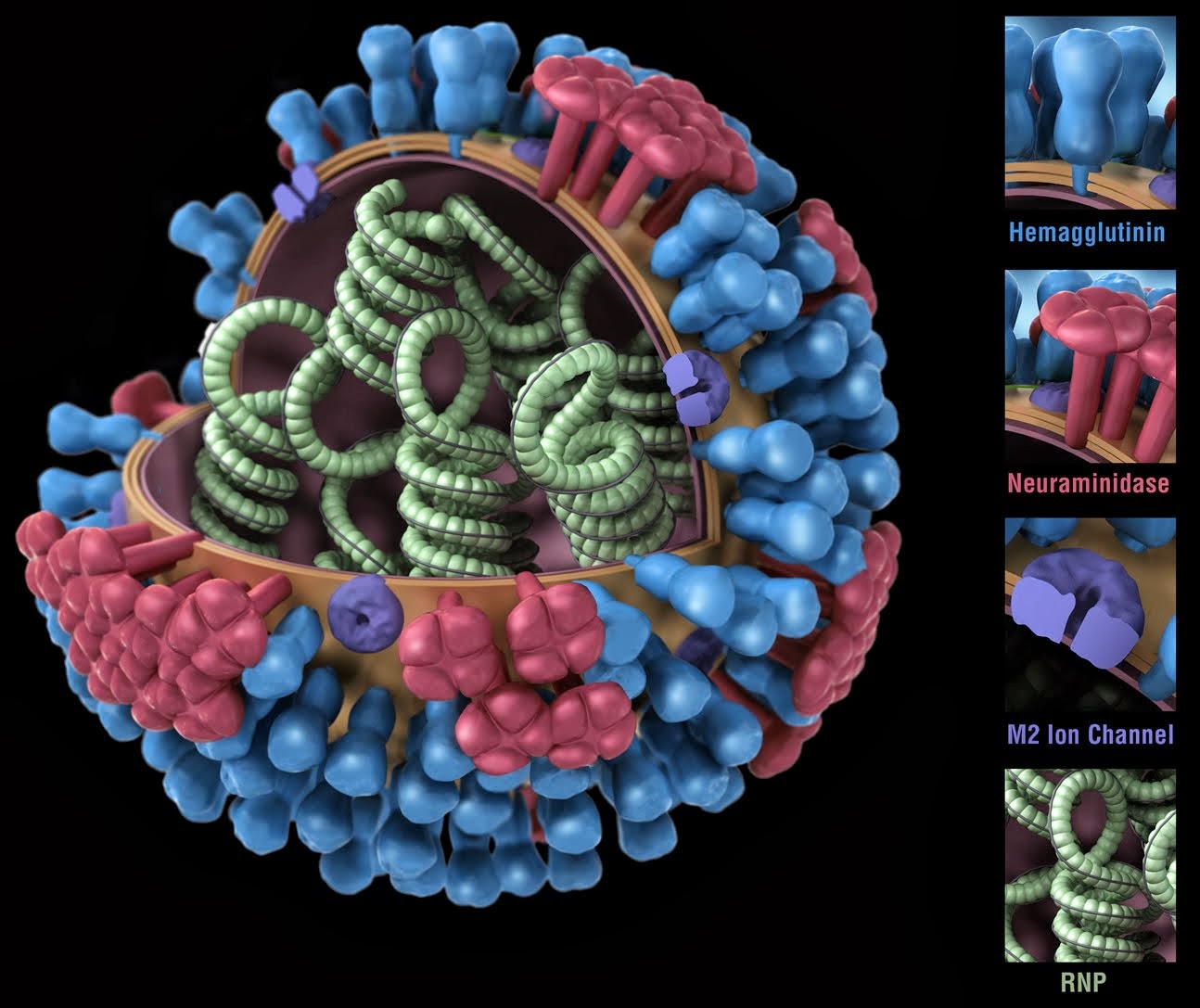
El principio, como suele pasar en todas las cosas, es siempre tosco y, con el tiempo, se van perfeccionando las cosas, la evolución va mejorando las formas.
Está constituido por dos transformaciones: la AB (representada en verde en la figura), que es irreversible, y la BA (en rojo) que es reversible. Como el ciclo en su conjunto es irreversible, debemos aplicar el teorema de Clausius con el signo menor:
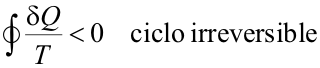 |
La integral de línea que aparece en la ecuación anterior puede ser descompuesta en la suma de las integrales evaluadas en cada etapa del ciclo, quedando:
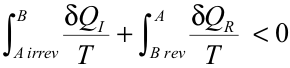 |
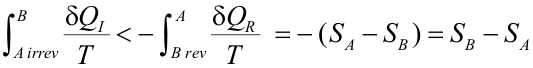 |
Ya que la integral evaluada a lo largo del tramo reversible es precisamente la variación de entropía entre los estados B y A. Por tanto,
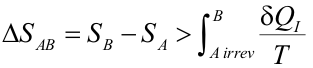 |
Esta ley indica la irreversibilidad de los procesos naturales . Los procesos reversibles son una ficción teórica útil y conveniente, pero no ocurren en la naturaleza. De esta ley se deduce que es imposible construir un dispositivo que funcione en un ciclo y cuyo único efecto sea la transferencia de calor de un cuerpo más frío a un cuerpo más caliente. De ello se deduce que las máquinas de movimiento perpetuo del segundo tipo son imposibles.
La entropía de un sistema se aproxima a un valor constante a medida que la temperatura se acerca al cero absoluto.
Ernst Mach, físico y filósofo austríaco.
Filósofo y científico alemán nacido en Turas (Moravia) y fallecido en Haar (Baviera). Realizó sus estudios en Viena y más tarde fue profesor de física en Graz (1864) y Praga (1867) y de historia y teoría de las ciencias inductivas en Viena (1895).
Friedrich Wilhelm Ostwald
“Químico, eugenista,profesor universitario y filósofo alemán, premio Nobel de Química en 1909 «por su trabajo en la catálisis y por sus investigaciones sobre los principios fundamentales que rigen los equilibrios químicos y las velocidades de reacción»
Inicialmente se opuso a la teoría atómica, pero luego de que se realizaran medidas del movimiento browniano y se comprobase que coinciden con las ecuaciones calculadas por Albert Einstein (medidas realizadas por Jean Perrin), cambió de opinión.”
Boltzmann fue un defensor a ultranza del atomismo, polemizando sobre todo con Mach y Ostwald, anti-atomistas partidarios de la energética y claros exponentes de la corriente idealista de la física alemana. Tuvo que abandonar su ambiciosa idea de explicar exactamente la irreversibilidad en términos estrictamente mecánicos; pero esta “derrota”, no ocultaré que dolorosa desde el punto de vista personal, le fue finalmente muy productiva, pues de alguna manera fue lo que le llevó al concepto probabilista de la entropía. Estas primeras ideas de Boltzmann fueron reivindicadas y extendidas, en el contexto de la teoría de los sistemas dinámicos inestables, sobre todo por la escuela de Prigogine, a partir de la década de 1970.
Ilya Prigogine (en ruso, Илья́ Рома́нович Приго́жин, Iliá Románovich Prigozhin) (Moscú, 25 de enero de 1917-Bruselas, 28 de mayo de 2003) fue un físico, químico, sistémico y catedrático universitario de origen ruso, nacionalizado belga.
La personalidad de Boltzmann era bastante compleja. Su estado de ánimo podía pasar de un desbordante optimismo al más negro pesimismo en cuestión de unas pocas horas. Era muy inquieto; él decía – medio en serio, medio en broma – que eso se debía a haber nacido en las bulliciosas horas finales de los alegres bailes del Martes de Carnaval, previas a los “duelos y quebrantos” (entonces) del Miércoles de Ceniza.

Ludwig Boltzmann and co-workers in Graz, 1887. (standing, from the left) Nernst, Streintz, Arrhenius, Hiecke, (sitting, from the left) Aulinger, Ettingshausen, Boltzmann, Klemenčič, Hausmanninger
Su lamentable final, su suicidio en Duino (Trieste) el 5 de septiembre de 1906, muy probablemente no fue ajeno a esa retorcida personalidad, aunque su precaria salud física fue seguramente determinante a la hora de dar el trágico paso hacia el lado oscuro.
Uno de los problemas conceptuales más importantes de la física es cómo hacer compatible la evolución irreversible de los sistemas macroscópicos (el segundo principio de la termodinámica) con la mecánica reversible (las ecuaciones de Hamilton o la ecuación de Schrödinger) de las partículas (átomos o moléculas) que las constituyen. Desde que Boltzmann dedujo su ecuación en 1872, este problema ha dado lugar a muy amplios debates, y el origen de la irreversibilidad es, aún hoy en día, controvertido.

Ludwig Eduard Boltzmann
“Viena, 20 de febrero de 1844–Duino, 5 de septiembre de 1906)1 fue un físico austríaco pionero de la mecánica estadística, a quien debe su nombre la llamada constante de Boltzmann, concepto fundamental de la termodinámica, y que halló la expresión matemática de la entropía desde el punto de vista de la probabilidad (la relación entre estados macroscópicos y microscópicos).”
En una de sus primeras publicaciones, Boltzmann obtuvo en 1866 una expresión de la entropía, que había sido definida un año antes por Clausius, basado en conceptos mecánicos. Las limitaciones de este trabajo eran que su aplicación se restringía al estudio de los gases y que el sistema era periódico en el tiempo. Además, Boltzmann no pudo deducir de su definición de entropía la irreversibilidad del segundo principio de la termodinámica de Clausius. En 1868, basándose en las ideas probabilísticas de Maxwell, obtuvo la distribución de equilibrio de un gas de partículas puntuales bajo la acción de una fuerza que deriva de un potencial (distribución de Maxwell-Boltzmann).

En el Universo, considerado como sistema cerrado, la entropía crece y…
En 1.872 publicó la denominada ecuación de Boltzmann para cuya deducción se basó, aparentemente, en ideas mecánicas. Esta ecuación contiene, sin embargo, una hipótesis no mecánica (estadística) o hipótesis del caos molecular, que Boltzmann no apreció como tal, y cuya mayor consecuencia es que, cualquiera que sea la distribución inicial de velocidad de un gas homogéneo diluido fuera del equilibrio, ésta evoluciona irreversiblemente hacia la distribución de velocidad de Maxwell. A raíz de las críticas de Loschmidt (paradoja de la reversibilidad) y Zermelo (paradoja de la recurrencia), Boltzmann acabó reconociendo el carácter estadístico de su hipótesis, y en 1877 propuso una relación entre la entropía S de un sistema de energía constante y el número de estados dinámicos W accesibles al sistema en su espacio de fases; esto es, la conocida ecuación S = kB ln W, donde kB es la constante de Boltzmann. En esta nota, se hace una breve descripción de la ecuación de Boltzmann y de la hipótesis del caos molecular.

El comportamiento de los gases siempre dio a los físicos en qué pensar
La ecuación de Boltzmann describe la evolución temporal de un gas diluido de N partículas puntuales de masa m contenidas en un volumen V que interaccionan a través de un potencial de par central repulsivo V(r) de corto alcance a. Como simplificación adicional, considérese que sobre las partículas no actúan campos externos. Si f1(r,v,t) indica la densidad de partículas que en el tiempo t tienen un vector de posición r y velocidad v, que está normalizada en forma:
∫dr ∫dvƒ1(r,v,t) = N
Su evolución temporal es la suma de dos contribuciones. En ausencia de interacción, las partículas que en el tiempo t tienen vector de posición r y velocidad v se encuentran, después de un intervalo de tiempo Δt, en r + v Δt y tiene la misma velocidad. Como
f1(r + vΔt,v,t + Δt) = f1(r,v,t)
en el límite Δt → 0 (2) se escribe:
∂1 f1(r,v,t) = – v∂r f1(r,v,t)
Que es una ecuación invariante bajo el cambio t → – t y v → – v. La evolución es, por tanto, mecánica.
Se cumplieron más de cien años desde la muerte de Boltzmann y su trabajo sigue siendo recordado. No pienso que Boltzmann creyera en la existencia real de los átomos, pero sí en su utilidad e incluso en su necesidad para comprender las leyes macroscópicas y la evolución irreversible de los fenómenos macroscópicos desde una base más fundamental que el nivel fenomenológico. Pero había quien (con autoridad) no creía ni en la existencia ni en su utilidad. Este debate no era ajeno a las tendencias ideológicas, religiosas y usos sociales de aquella época porque, en general, la ciencia es parte de la cultura y depende del momento histórico que viven los científicos, al fin y al cabo, seres humanos como los demás, influenciables por su entorno en una gran medida.
Por el siglo XIX, e incluso antes, ya se hablaba de “átomos”* y una rudimentaria teoría cinética de los gases gozaba de aceptación y utilidad científica (recordemos los trabajos de Benoulli, Dalton, Laplace, Poisson, Cauchy, Clausius, Krönig… y Maxwell). Pero fue Boltzmann quien definitivamente profundizó en la cuestión, para el estudio del equilibrio y, sobre todo, intentando explicar mecánicamente (mecano-estadísticamente) la evolución termodinámica irreversible y la descripción de los procesos de transporte ligados a ella. Y, nuevamente (por su enorme importancia) no podemos dejar de mencionar la muy singular labor que hicieron Gibbs, Einstein, Planck, Fermi y otros. Sin la motivación ideológica de Boltzmann, Gibbs elaboró una bellísima, útil y hoy dominante formulación (cuerpo de doctrina) de la termodinámica y física estadística.
Lorentz
Fue Lorentz quien primero utilizó la ecuación de Boltzmann y lo hizo para describir la corriente eléctrica en sólidos dando un paso significativo por encima del pionero Drude. Lorentz introdujo un modelo opuesto al browniano donde partículas ligeras como viento (electrones) se mueven chocando entre sí y con árboles gordos (tales como iones en una red cristalina); un modelo del que se han hecho estudios de interés tanto físico como matemático.
S = k log W
Enskog (inspirándose en Hilbert) y Chapman (inspirándose en Maxwell) enseñaron cómo integrar la ecuación de Boltzmann, abriendo vías a otras diversas aplicaciones (hidrodinámica, propagación del sonido, difusión másica, calor, fricción viscosa, termoelectricidad, etc.). Recordemos que Boltzmann encontró como solución de equilibrio de su ecuación una distribución de velocidades antes descubierta por Maxwell (hoy, como reseñé anteriormente, de Maxwell-Boltzmann), por lo que concluyó que así daba base microscópica mecánica (teorema H mecano-estadístico) al segundo principio de la termodinámica (estrictamente, evolución de un sistema aislado hacia su “desorden” máximo).
El físico austríaco Ludwig Boltzmann sentó las bases estadísticas de la entropía, su trabajo fue tan importante que el gran físico Max Planck sugirió que su versión de la fórmula de Boltzmann fuera grabada en la lápida de Boltzmann de Viena.
Está claro que ningún físico que se precie de serlo puede visitar Viena sin visitar el parque Zentralfriedhof para ver la tumba de Boltzmann. Yo sí me pasé por allí. Me senté junto a la tumba; el lugar estaba desierto, y cerrando los ojos traté de conectar con la conciencia del genio. La sensación, extraña y agradable, seguramente fue creada por mi imaginación, pero creo que charlé con él en el interior de mi mente –la fuerza más potente del universo está ahí– y aquellos sentimientos, aquel momento, compensaron el esfuerzo del viaje.
En la tumba, sobre una gran lápida de mármol de color blanco con los nombres Ludwig Boltzmann y de los familiares enterrados con él, sobre el busto de Boltzmann, se puede leer la inscripción, a modo de epitafio:
En esta breve ecuación se encierra la conexión entre el micro-mundo y el macro-mundo, y por ella se reconoce a Boltzmann como el padre de la rama de la física conocida como mecánica estadística. Esta sencilla ecuación es la mayor aportación de Boltzmann y una de las ecuaciones más importantes de la física. El significado de las tres letras que aparecen (aparte la notación del logaritmo) es el siguiente:
- S es la entropía de un sistema.
- W es el número de microestados posibles de sus partículas elementales.
- k es una constante de proporcionalidad que hoy recibe el nombre de Constante de Boltzmann, de valor 1’3805 × 10-23 J/K (si el logaritmo se toma en la base natural).
En definitiva, la ecuación describe la estrecha relación entre la entropía (S) y las miles de formas de partículas que en un sistema se pueden arreglar (k log W). La última parte es difícil. K es la constante de Boltzmann y W es el número de elementos microscópicos de un sistema (por ejemplo, el impulso y la posición de los átomos individuales de gas) en un sistema macroscópico en un estado de equilibrio (por ejemplo, el gas de sellado en una botella). Parece que la naturaleza ama el caos cuando empuja a los sistemas hacia el desequilibrio y Boltzmann le llamó entropía a este fenómeno.

El Cerebro como una inmensa Galaxia de Estrellas
Cuando profundizamos un poco en lo que el cerebro humano ha sido capaz de generar, los pensamientos que ha llegado a generar bien sea en forma de ecuaciones matemáticas o expresados con palabras, no podemos dejar de sorprendernos y maravillarnos al ver que, ¡todo el universo parece estar dentro de nuestras mentes! ¿Qué secretos se encierran allí? ¿Cómo nos lleva a estos pensamientos tan profundos?
Como todas las ecuaciones sencilla de gran trascendencia en la física (como la famosa E = mc2), hay un antes y un después de su formulación: sus consecuencias son de un calado tan profundo que cambiaron la forma de entender el mundo, y en particular, de hacer física a partir de ellas. De hecho, la sutileza de la ecuación es tal que hoy, cien años después de la muerte de su creador, se siguen investigando sus nada triviales consecuencias. Creo que lo mismo ocurrirá con α = 2πe2/ħc que, en tan reducido espacio y con tan pocos símbolos, encierra los misterios del electromagnetismo (el electrón), de la constante de Planck (la mecánica cuántica), y de la luz (la relatividad de Einstein), todo ello enterrado profundamente en las entrañas de un número: 137.
Bueno, a pesar de todo lo anterior, Schrödinger nos decía:
“La actitud científica ha de ser reconstruida, la ciencia ha de rehacerse de nuevo”

¡Lo grande y lo pequeño! ¡Son tantos los secretos de la Naturaleza!
Siempre hemos tenido consciencia de que en física, había que buscar nuevos paradigmas, nuevos caminos que nos llevaran más lejos. Es bien conocida la anécdota de que a finales del siglo XIX un destacado físico de la época William Thomson (1824-1907) conocido como Lord Kelvin, se atrevió a decir que solo dos pequeñas “nubecillas” arrojaban sombras sobre el majestuoso panorama de conocimiento que había construido la física clásica desde Galileo y Newton hasta ese momento: el resultado del experimento de Michelson-Morley, el cual había fallado en detectar la existencia del supuesto éter luminífero; y la radiación del cuerpo negro, i.e la incapacidad de la teoría electromagnética clásica de predecir la distribución de la energía radiante emitida a diferentes frecuencias emitidas por un radiador idealizado llamado cuerpo negro. Lo que Lord Kelvin no puedo predecir es que al tratar de disipar esas dos “nubecillas”, la física se vería irremediablemente arrastrada a una nueva física: la física moderna fundada sobre dos revoluciones en ciernes: la revolución relativista y la revolución cuántica con dos científicos como protagonistas: Planck y Albert Einstein. Sin embargo, ha pasado un siglo y seguimos con esas dos únicas guías para continuar el camino y, resultan insuficientes para llegar a la meta que… ¡Está tan lejos!
emilio silvera















 Totales: 74.956.688
Totales: 74.956.688 Conectados: 54
Conectados: 54























