Ene
15
¿El núcleo del átomo? ¡Una maravilla de la Naturaleza!
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física Cuántica ~
Clasificado en Física Cuántica ~
 Comments (0)
Comments (0)

Las partículas del núcleo atómico. Protón y neutrón.
En 1920 (Rutherford) descdubrió las partículas positivas que forman los átomos, los protones.

Por lo tanto en los núcleos de los átomos hay unas partículas positivas que se llaman protones. En el hidrógeno solo hay una partícula ya que recordemos su masa era casi la misma.

Se comprobó que el número de protones es una característica especial de cada elemento químico, ya que todos los átomos del mismo elemento tienen el mismo número de protones. Se llama número atómico (Z) al número de protones que tienen los átomos de un elemento químico. A cada elemento químico le corresponde un número atómico desde 1 hasta 106.
Todavía tenemos que buscar otras partículas en el núcleo atómico. La masa de los protones de un núcleo es mucho menor que la masa del núcleo.

Cada elemento químico se caracteriza por el número de protones de su núcleo, que se denomina número atómico (Z). Así, el hidrógeno ( 1H) tiene un protón, el carbono ( 6C) tiene 6 protones y el oxígeno ( 8O) tiene 8 protones en el núcleo.
El número de neutrones del núcleo puede variar. Casi siempre hay tantos o más neutrones que protones. La masa atómica(A) se obtiene sumando el número de protones y de neutrones de un núcleo determinado.
Un mismo elemento químico puede estar constituído por átomos diferentes, es decir, sus números atómicos son iguales, pero el número de neutrones es distinto. Estos átomos se denominan isótopos del elemento en cuestión. Isótopos significa “mismo lugar“, es decir, que como todos los isótopos de un elemento tienen el mismo número atómico, ocupan el mismo lugar en la Tabla Periódica.
isótopos del Hidrógeno

Isótopos del Carbono

Desde 1918 estaba probado que existían los isótopos. Estos, eran átomos que tenían propiedades químicas iguales (parecían elementos iguales, por tanto), tenían el mismo número atómico, pero sus masas atómicas eran diferentes. En el núcleo debían existir partículas neutras que contribuyeran a la masa pero no tuvieran carga eléctrica.



La curiosidad acerca del tamaño y masa del átomo atrajo a cientos de científicos durante un largo período en el que la falta de instrumentos y técnicas apropiadas impidió lograr respuestas satisfactorias. Con posterioridad se diseñaron numerosos experimentos ingeniosos para determinar el tamaño y peso de los diferentes átomos.
El átomo más ligero, el de hidrógeno, tiene un diámetro de aproximadamente 10-10 m (0,0000000001 m) y una masa alrededor de 1,7 x 10-27 kg (la fracción de un kilogramo representada por 17 precedido de 26 ceros y una coma decimal).
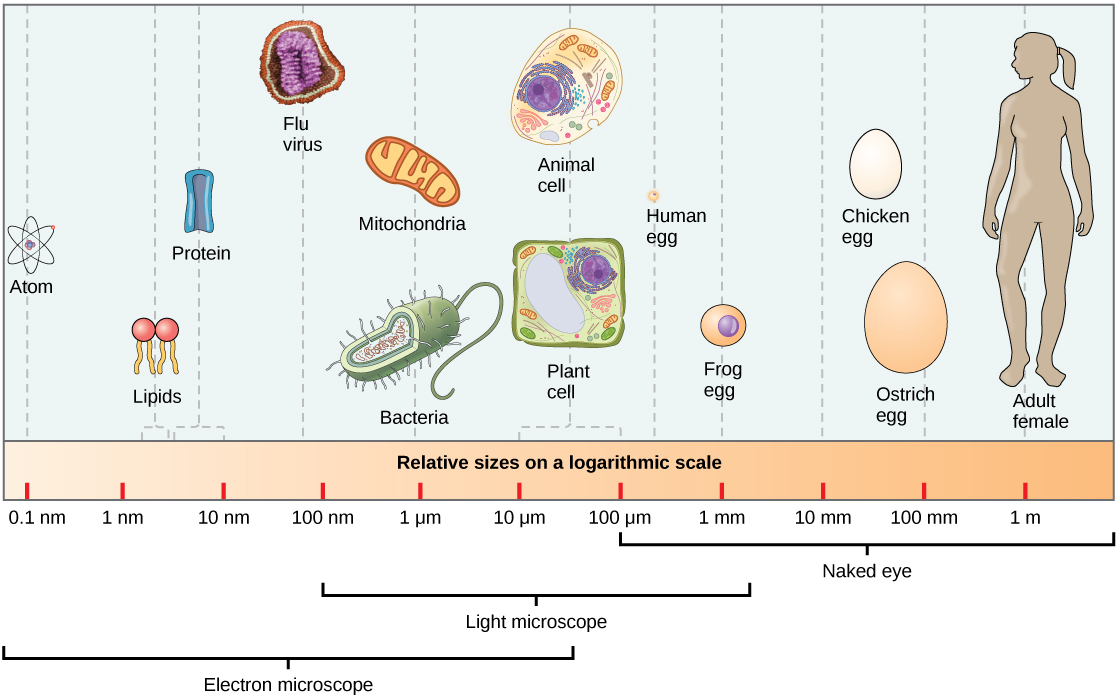


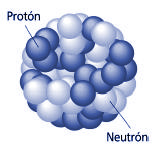
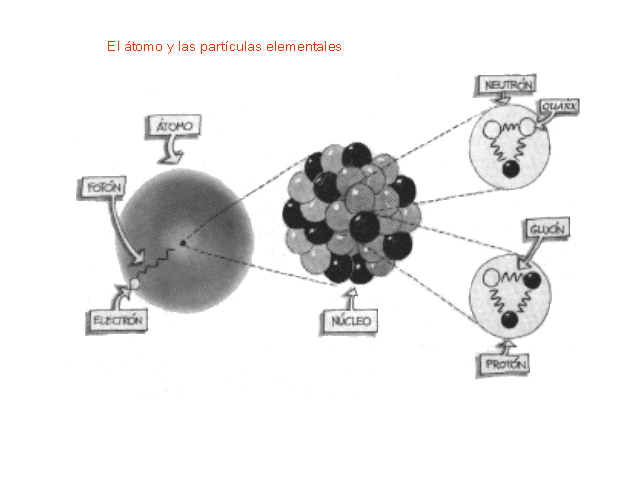
Como no es el objeto del trabao, no hablaremos hoy de los Quarks, y, simplemente diremos que en la naturaleza no se encuentran quarks aislados. Estos siempre se encuentran en grupos, llamados Hadrones. de dos o tres quarks, conocidos como mesones y bariones respectivamente. Esto es una consecuencia directa del confinamiento de color. En el año 2003 se encontró evidencia experimental de una nueva asociación de cinco quarks, los Pentaquarks, cuya evidencia, en principio controvertida , fue demostrada gracias al Colisionador de Partículas LHC en el pasado Julio de 2.015.

Pero sigamos con lo que nos ocupa y veámos que los Quarks están confinados dentro de los nucleones (protones y neutrones) donde la fuerza fuerte les retiene y nos los deja que se vayan alejando más de lo debido como se explica en el cuadro de arriba.
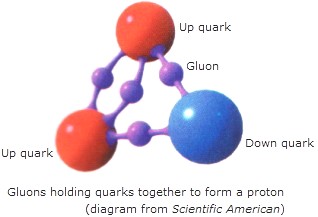
Dentro del nucleo se desatan las fuerzas de la Naturaleza, la que conocemos como fuerza nuclear fuerte, la más potente de las cuatro fuerzas fundamentales que, intermediada por otras partículas de la familia de los Bosones, los Gluones, no dejan que los Quarks se alejen y son retenidos allí, dentro de los nucleones donde tienen su función de conformar los hadrones másicos del núcleo que le aporta la materia al átomo.
Los Gluones, son las partículas intermediarias de la fuerza fuerte, y, de la misma manera, existen otros Bosones encargados de mediar en las otras fuerzas conocidas de la Naturaleza: El Fotón para los fenómenos electromagnéticos, el Gravitón (no encontrado aún) para la fuerza de Gravedad, y, los W+, W–y Zº para la fuerza nuclear débil.

Este acontecimiento se está dando continuamente en el interior de estrellas como el Sol, y es de esperar que se pueda reproducir algún día cercano para obtener energía barata y limpia mediante fusión nuclear.

El protón y el neutrón son Hadrones de la rama bariónica, y, el electrón, es un Leptón. Todos están presentes en el átomo, los primeros en el núcleo y el segundo formando la parte electrónica de espacios magnéticos que forman en su deambular a su alrededor.
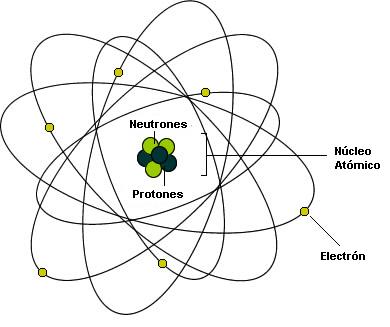
Lo cierto es que, el núcleo atómico está cargado positivamente y, tal carga, hace la llamada para que, un enjambre de electrones, con cargas negativas, vengan a rodear el núcleo atómico y, de esa manera, queda estabilidado el átomo, ese pequeño objeto que conforma todas las cosas hechas de materia.
Así, los electrones que rodea el núcleo, con su carga eléctrica negativa que complementa la positiva de los protones y hace estable al átomo; una masa de solamente 1/1.836 de la del núcleo más ligero (el del hidrógeno). Y, sin embargo, la importancia del electrón es vital en el universo.
Repasando todo esto, no puedo dejar de recordar aquellas palabras que el físico Freeman Dyson escribió:
“Cuando miramos en el universo e identificamos los muchos accidentes de la física y la astronomía que han colaborado en nuestro beneficio, casi parece que el universo debe haber sabido, en cierto sentido, que nosotros íbamos a venir“.
α es la constante de estructura fina, si variara con el paso del tiempo… … la vida no podría existir. Esas constantes hacen posible nuestra presencia aquí.
Fijaros en el hecho cierto de que, si la carga del electrón, o, la masa del protón, variaran aunque sólo fuese una diezmillonésima parte… ¡La vida no podría existir en el Universo! Estamos hechos de átomos y, con tal cambio, éstos nunca se habrían podido conformar.
emilio silvera.
















 Totales: 75.199.627
Totales: 75.199.627 Conectados: 49
Conectados: 49
























