Ago
11
Desde bien pequeños dicen lo que quieren ser en la vida
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (4)
Comments (4)
https://www.youtube.com/watch?
|
Niña sigue el ritmo de la música y disfruta de cada pasaje
|
Ago
1
Sobre el número áureo
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)



¿Sabéis qué relaciona la manzana de Apple con la proporción áurea?, ¿Y con la distribución de los pétalos en una flor?, ¿Y con las proporciones de nuestro cuerpo?. Esta proporción ha fascinado desde hace siglos al ser humano, que lo ha considerado un indicador de la perfección y la estética. En el Renacimiento, muchos artistas y arquitectos compusieron sus trabajos con la intención de aproximarse a la proporción áurea, convencidos de que esta relación atribuía a las obras un carácter estético especial.
Veamos el Reportaje de prensa:
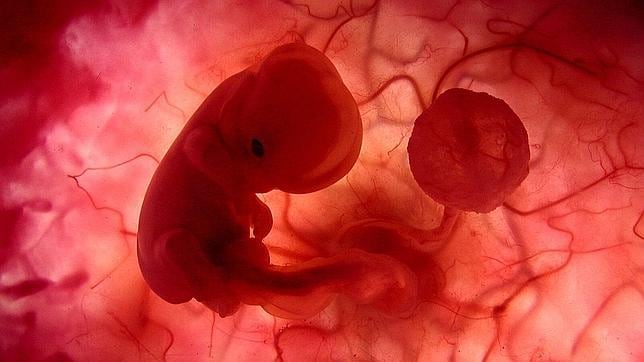
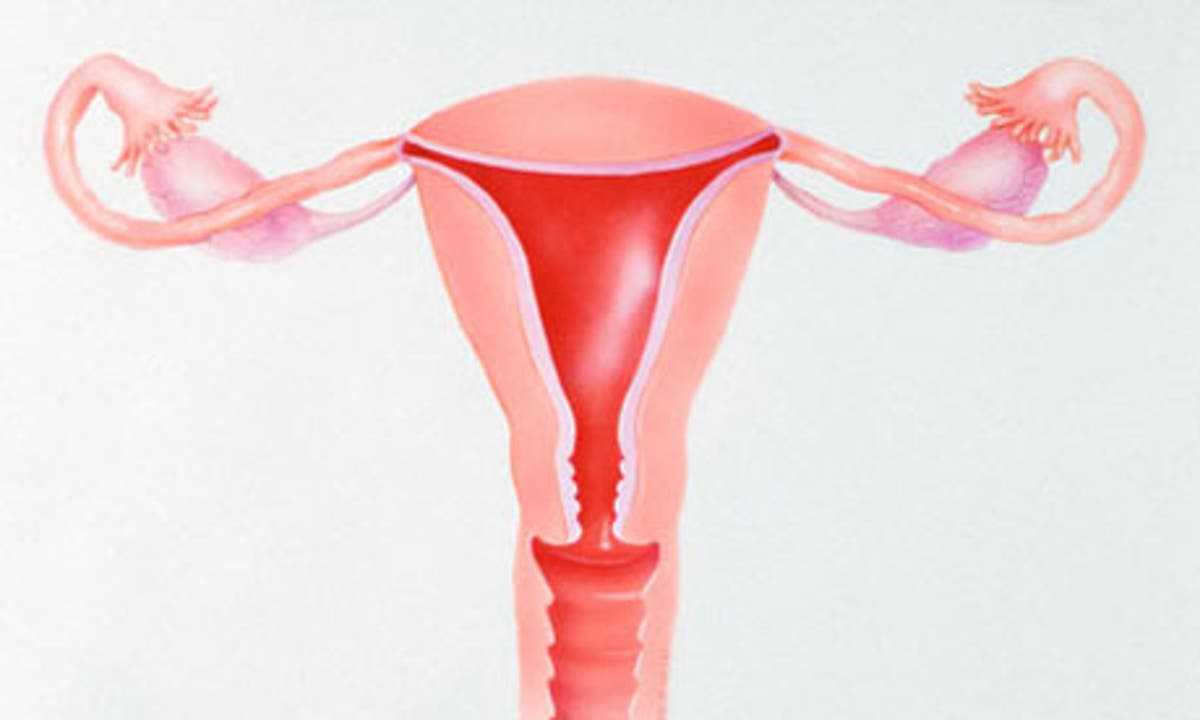
El número mágico de la fertilidad femenina
El Número áureo descubierto en el útero.
En su momento pudimos leer, en el apartado de Ciencia del Diario ABC, el siguiente reportaje:
“Un ginecólogo belga encuentra por primera vez la «divina proporción» en las entrañas de las mujeres que están en su edad más fértil
1,618. Ese es el número áureo o relación dorada, una proporción de las cosas descubierta en la antigüedad a la que se le atribuye un carácter estético y que puede encontrarse no solo en el mundo del arte, sino también en la naturaleza. Y resulta que también en el útero de las mujeres. El ginecólogo Jasper Vergtus, de la Universidad de Leuven en Bélgica, asegura que existe una relación entre ese número considerado por algunos casi místico y el sexo femenino. El investigador sugiere que cuando las mujeres son más fértiles, entre los 16 y los 20 años, las dimensiones del útero se acercan a 1,6, una aproximación muy cercana al número áureo, según publica el diario británico The Guardian en su edición online.
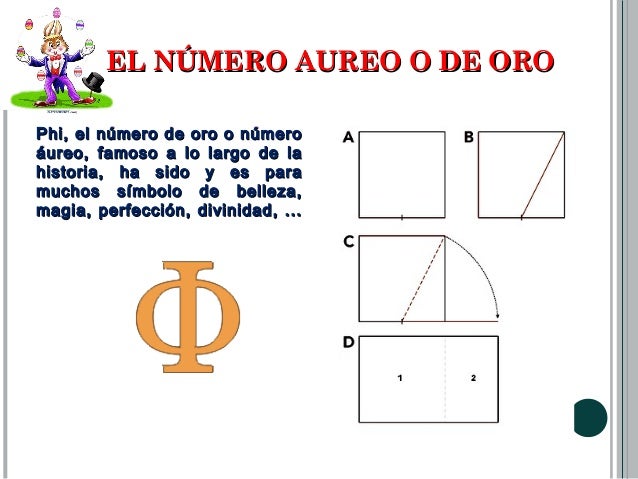
El número áureo -a menudo llamado número dorado, razón áurea, razón dorada, proporción áurea o divina proporción- fue formulado por primera vez por Euclides, unos tres siglos antes de Cristo, como un número irracional y con infinitos decimales, cuyo su valor aproximado es 1,6180339887498… Casi 2000 años más tarde Alberto Durero describía cómo trazar con regla y compás la espiral basada en la sección áurea. Unas décadas después, el astrónomo Johannes Kepler desarrolló su modelo del Sistema Solar, en el que tenía en cuenta estas proporciones mágicas.
El número áureo también está «emparentado» con la serie de Fibonacci. Si llamamos Fn al enésimo número de Fibonacci y Fn+1 al siguiente, podemos ver que a medida que n se hace más grande, la razón entre Fn+1 y Fn oscila, siendo alternativamente menor y mayor que la razón áurea. Esto se relaciona de una forma muy especial con la naturaleza, por ejemplo, con la disposición de los pétalos de las flores.
De Da Vinci a las entrañas
![Proporción Áurea: Explicación Sencilla [Con Ejemplos] | Blog del Fotógrafo](https://www.blogdelfotografo.com/wp-content/uploads/2022/02/Vitruvian_Man_by_Leonardo_da_Vinci-2.webp)

La divina proporción ha sido empleada hasta la saciedad en el arte -buen ejemplo de ello es el magnífico Hombre de Vitruvio de Leonardo Da Vinci- pero se encuentra en los lugares más dispares de la naturaleza. Según The Guardian, el doctor Verguts ha medido los úteros de 5.000 mujeres utilizando ultrasonidos y ha dibujado una tabla con las proporciones según la longitud y la anchura para las diferentes franjas de edad. El número resultante es 2 tras el nacimiento y decrece a 1,46 cuando la mujer envejece. Lo más sorprendente es que cuando las mujeres están en su etapa más fértil, entre los 16 y los 20 años, las dimensiones del útero son de 1,6, una estupenda aproximación al número áureo. Es la primera vez que alguien se ha dado cuenta.

Probablemente, el asunto tiene un escaso valor científico o médico, pero resulta más que curioso que este número presente en el arte, la arquitectura y la naturaleza -hasta en los cuasicristales del último Nobel de Química– aparezca también en las entrañas femeninas. Ya sabemos lo que el Partenón, una tarjeta de crédito, el rostro de la Mona Lisa y un útero tienen en común. Y todas, de una u otra forma, son cosas atractivas.”
Si queréis saber más sobre estos interesantes temas, os recomiendo leer:
La fórmula de Euler, una ecuación en la 4ª dimensión de Ricard Jiménez García que, en su Mundo aureo ofrece una serie de obras fascinantes y que son reveladoras de profundos pensamientos, y, sin dudarlo, os pueden transportar en un viaje sin fin, en el que podeis visitar mundos maravillosos del pensamiento humano que, ligado al Universo con los hilos invisibles de las ideas… ¡Os dará que pensar!
Jul
25
De materiales y radiaciones (El ingenio humano)
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)

Uranio 238
Al pensar en la desintegración me ha traído a la memoria otros materiales que también se desintegran de manera natural y que son materiales fértiles, o que sin serlo, se pueden transformar en otros que sí lo son.
Al hablar de material fértil me estoy refiriendo a núclidos que pueden absorber neutrones para formar material fisible. El uranio-238, por ejemplo, absorbe un neutrón para formar uranio-239, que se desintegra en plutonio-239. Este es el tipo de conversión que la imaginación del hombre hace que ocurra en un reactor reproductor.
Isaac Asimov lo explicaba así::


El uranio-235 es un combustible práctico, es decir, los neutrones lentos son capaces de hacer que el uranio-235 se fisione, o lo que es lo mismo, se rompan sus átomos en dos, produciendo neutrones lentos, que a su vez inducen otras fisiones atómicas. El uranio-233 y el plutonio-239 son también combustibles nucleares prácticos por las mismas razones.
Desgraciadamente, el uranio-233 y el plutonio-239 no existen en estado natural sino en trazas mínimas, y el uranio-235, aunque existe en cantidades apreciables, no deja de ser raro. En cualquier muestra de uranio natural, sólo siete de cada mil átomos son de uranio-235, el resto es uranio-238.

Científicos chinos han logrado extraer uranio y plutonio de combustible gastado tras la obtención de energía nuclear, un avance que según los expertos podría multiplicar por 60 la duración de estas fuentes de energía atómica,

El uranio-238, la variedad común de uranio, no es un combustible nuclear práctico. Así que, el uranio que más abunda en la naturaleza no sirve como combustible nuclear. Podemos conseguir que se fisione, pero sólo con neutrones rápidos. Los átomos de uranio-238 que se rompen en dos, producen neutrones lentos, que no bastan para producir o inducir nuevas fisiones. El uranio-238 cabría compararlo a la madera húmeda: es posible hacer que arda, pero acabará por apagarse.
Supongamos, sin embargo, que se separa el uranio-235 del uranio-238 (trabajo más bien difícil) y que se utiliza aquel para hacer funcionar un reactor nuclear. Los átomos de uranio-235 que forman el combustible del reactor se fisionan y esparcen miríadas de neutrones lentos en todas direcciones. Si el reactor está rodeado por una capa de uranio ordinario (que en su mayor parte es uranio-238), los neutrones que van a parar allí son absorbidos por el uranio-238 y, aunque no pueden hacer que el uranio-238 se fisione, sí pueden provocar otros cambios que finalmente, producirán plutonio-239. Separando este plutonio-239 del uranio (tarea muy fácil), puede ser utilizado como combustible nuclear practico para la fisión.
De esta manera, el reactor nuclear genera nuevo combustible a partir de un material (uranio-238) que no lo es. Este es el motivo de que al reactor nuclear que hace posible la transformación se le llame “reactor generador”.
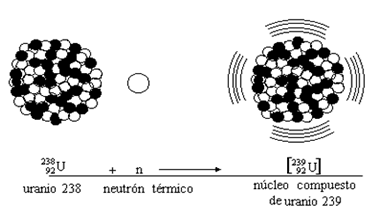
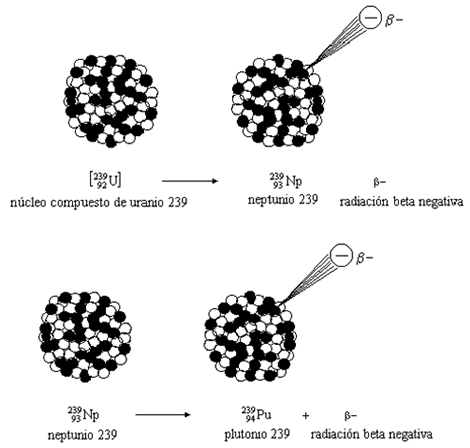
El Reactor Generador TR10 permite convertir uranio-238 en plutonio-239 dentro de su mismo núcleo
Un reactor generador bien diseñado puede producir más plutonio-239 que el uranio-234 consumido para ello. De este modo, las reservas totales de uranio de la Tierra (y no sólo las de uranio-235) se convierten en potenciales de combustible nuclear.
El torio, tal como se da en la naturaleza, consiste todo él en torio-232, que al igual que el uranio-238, no es un combustible nuclear práctico, porque requiere neutrones rápidos para fisionarse. Pero si se coloca torio-232 alrededor de un reactor nuclear, sus átomos absorberán los neutrones y, sin experimentar fisión alguna, se convertirán en átomos de uranio-233. Como el uranio-233 es un combustible práctico que se puede separar fácilmente del torio, el resultado es otra variedad del reactor generador, que convierte las reservas de torio en un combustible nuclear en potencia.

El torio es un elemento naturalmente radiactivo de símbolo Th y número atómico 90. Descubierto en noruega por el minerólogo Thrane Esmark e identificado y nombrado por el químico sueco Jons Berzelius en 1828. El Torio fue nombrado en honor al dios nordico del trueno Thor.
Se encuentra en 13 lugares más arriba en la lista de elementos más abundantes de la tierra que todos los isótopos del uranio. Esto se debe a que cierto isótopo del torio, el 232Th decae más lentamente que el uranio, de hecho lo hace tan lento que su vida media es comparable con la edad del universo.
La cantidad total de uranio y de torio que hay en la Tierra es unas 800 veces mayor que las reservas de uranio-235, lo que significa que el buen uso de los reactores generadores podría multiplicar por 800 la oferta potencia de energía extraída de plantas de fisión nuclear.
En este punto, sin dejar de elogiar la inteligencia del hombre que ha sabido encontrar la manera de transformar una materia inservible en otra practica, hay que decir que la energía de fisión nuclear genera también muchos problemas.

Como estará comprobando al lector de este trabajo, el autor ha querido esta vez diversificar los temas y plasmar una variedad múltiple que facilite el conocimiento de distintas cosas que ocurren en la naturaleza, o que la mano del hombre hace que ocurran, y todas estas cuestiones tratadas aquí van encaminadas a resolver preguntas que en alguna ocasión nos hemos podido hacer, tales como:
¿Por qué al calentar un metal se pone primero rojo, luego naranja, después amarillo, pero a continuación blanco en lugar de seguir el espectro y ponerse verde?
Cualquier objeto, a cualquier energía superior al cero absoluto, radia ondas electromagnéticas. Si su temperatura es muy baja, emite sólo ondas de radio largas, muy pobres en energías. Al aumentar la temperatura, radia una cantidad mayor de ondas, pero también empieza a radiar ondas de radio más cortas (y más energéticas). Si la temperatura sigue subiendo, empiezan a radiarse microondas aún más energéticas y después radiaciones infrarrojas.

Esto no quiere decir que a una temperatura dada sólo se emitan ondas de radio largas, un poco más arriba sólo ondas de radio cortas, luego sólo microondas y después sólo infrarrojos. En realidad, se emite toda la gama de radiaciones, pero siempre hay una radiación máxima, es decir, una gama de longitudes de onda que son las más radiadas, flanqueadas por cantidades menores en el lado de las energías bajas y por cantidades todavía más pequeñas en el de las altas.
Cuando un objeto alcanza la temperatura del cuerpo humano (37°C), el máximo de radiación se encuentra en los infrarrojos largos. El cuerpo humano también radia ondas de radio, pero las longitudes de ondas más cortas y más energéticas son siempre las más fáciles de detectar por ser los más potentes.
Cuando la temperatura alcanza aproximadamente los 600°C, el máximo de radiación se halla en el infrarrojo corto. Pero a estas alturas la pequeña cantidad de radiación que se halla en el lado de las energías altas adquiere una importancia especial, porque entra ya en la región de la luz visible roja. El objeto reluce entonces con un rojo intenso.
Este rojo constituye sólo un pequeño porcentaje de la radiación total, pero como da la casualidad de que nuestro ojo lo percibe, le otorgamos toda nuestra atención y decimos que el objeto está al “rojo vivo”.
Si la temperatura sigue subiendo, el máximo de radiación continúa desplazándose hacia las longitudes de ondas cortas y cada vez se emite más luz visible de longitudes cada vez menores. Aunque el objeto radia más luz roja, se van agregando poco a poco luz anaranjada y luz amarilla en cantidades menores pero significativas. Al llegar a los 1.000°C la mezcla de colores la percibimos como naranja, y a los 2.000°C como amarilla. Lo cual no significa que a los 1.000°C sólo se radie luz naranja y a los 2.000°C sólo se radie luz amarilla, porque si fuese así, habría efectivamente que esperar que lo siguiente fuese “color verde”. Lo que en realidad vemos son mezclas de colores.

Al llegar a los 6.000°C (la temperatura superficial del Sol), el máximo de radiación está en el amarillo visible y lo que llega a nuestros ojos son grandes cantidades de luz visible, desde el violeta hasta el rojo. La incidencia simultánea de toda la gama de luz visible sobre nuestra retina nos da la sensación de blanco, y de ahí el color del Sol.
Los objetos más calientes aún que el Sol radian todas las longitudes de ondas de luz visible y en cantidades todavía mayores, pero el máximo de radiación se desplaza al azul, de modo que la mezcla se desequilibra y el blanco adquiere un tinte azulado.
Toda esta travesía se produce para objetos calientes que emiten “espectros continuos”, es decir, que radian luz en la forma de una ancha banda de longitudes de ondas. Ciertas sustancias en condiciones adecuadas, radian sólo luz de determinadas longitudes de onda. El nitrato de bario radia luz verde cuando se calienta, y con ese fin se lo utiliza en los fuegos de artificio, “calor verde”, podríamos decir.
¡Qué bonito es saber!

Tubos de descarga conteniendo gases nobles, excitados eléctricamente, mostrando la luz emitida.
En alguna ocasión todos hemos oído mencionar la palabra “gases nobles”, y sin embargo no siempre sabemos lo que son y el por qué le llaman así.
Los elementos que reaccionan difícilmente o que no reaccionan en absoluto con otros elementos se denominan “inertes”. El nitrógeno y el platino son ejemplos de elementos inertes.
En la última década del siglo pasado se descubrieron en la atmósfera una serie de gases que no parecían intervenir en ninguna reacción química. Estos nuevos gases (helio, neón, argón, kripton, xenón y radón) son más inertes que cualquier otro elemento y se agrupan bajo el nombre de gases inertes.
Los elementos inertes reciben a veces el calificativo de “nobles” porque esa resistencia a reaccionar con otros elementos recordaba un poco a la altanería de la aristocracia. El oro y el platino son ejemplos de “metales nobles”, y por la misma razón se llaman a veces “gases nobles” a los gases inertes. Hasta 1.962, el nombre más común era el de gases inertes, quizá porque lo de nobles parecía poco apropiados en sociedades democráticas.

La razón de que los gases inertes sean inertes es que el conjunto de electrones de cada uno de sus átomos está distribuido en capas especialmente estables. La más exterior, en concreto, tiene 8 electrones. Así la distribución electrónica del neón es (2,8) y la del argón (2,8,8). Como la adición o sustracción de electrones rompe esta distribución estable, no pueden producirse cambios electrónicos. Lo cual significa que no pueden producirse reacciones químicas y que estos elementos son inertes.
Ahora bien, el grado de inercia depende de la fuerza con que el núcleo, cargado positivamente y situado en el centro del átomo sujeta a los 8 electrones de la capa exterior. Cuantas más capas electrónicas haya entre la exterior y el centro, más débil será la atracción del núcleo central sobre los electrones de esa última capa de electrones.

Quiere esto decir que el gas inerte más complejo es también el menos inerte. El gas inerte de estructura atómica más complicada es el radón. Sus átomos tienen una distribución electrónica de (2,8,18,32,18,8). El radón, sin embargo está sólo constituido por isótopos radiactivos y es un elemento con el que difícilmente se pueden hacer experimentos químicos. El siguiente en orden de complejidad es el xenón, que es estable. Sus átomos tienen una distribución electrónica de (2,8,18,18,8).
Los electrones más exteriores de los átomos de xenón y radón están bastante alejados del núcleo y, por consiguiente, muy sueltos. En presencia de átomos que tienen una gran apetencia de electrones, son cedidos rápidamente. El átomo con mayor apetencia de electrones es el flúor, y así fue como en 1.962 el químico canadiense Neil Bartlett consiguió formar compuestos de xenón y flúor.
Desde entonces se han conseguido formar también compuestos de radón y kriptón. Por eso los químicos rehúyen el nombre de gases inertes, porque a fin de cuentas, esos gases no son completamente inertes. Hoy día se ha impuesto la denominación de “gases nobles”, y existe toda una rama de la química que se ocupa de los “compuestos de gases nobles”.
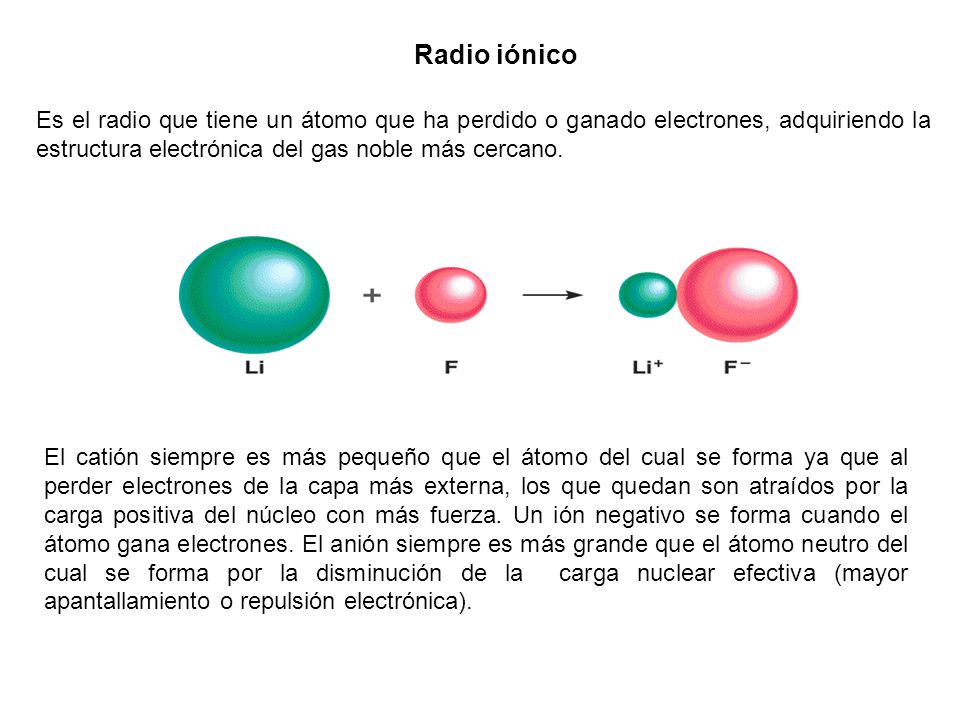
Naturalmente, cuanto más pequeño es el átomo de un gas noble, más inerte es, y no se ha encontrado nada que sea capaz de arrancarles algún electrón. El argón, cuya distribución electrónica es de 2,8,8 y el neón, con 2,8 electrones respectivamente, sigue siendo completamente inerte. Y el más inerte de todos es el helio, cuyos átomos contienen una sola capa electrónica con dos electrones (que es lo máximo que puede alojar esta primera capa) que al estar en la primera linea cerca del núcleo positivo, están fuertemente atraídos al tener su carga eléctrica el signo negativo.
Para finalizar diré que los gases nobles (gases inertes, gases raros) están clasificados en el grupo 18 (antiguamente 0) de la tabla periódica de dos elementos y se definen por símbolos que responden a: helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe) y radón (Rn).

Ya se dijo antes la configuración electrónica de cada uno de ellos y todas las capas internas están completamente ocupadas, lo que hace que estos elementos, por tanto, constituyan la terminación de un periodo y posean configuración de capa completa, por lo que sus energías de ionización son muy elevadas y su reactividad química escasa.
Como son monoatómicos, las moléculas de los gases nobles poseen simetría esférica, y las fuerzas intermoleculares son muy débiles, por lo que sus entalpías de vaporización son muy bajas.
Con todo lo anteriormente expuesto sobre los gases nobles, espero que el lector del trabajo aquí reflejado pueda tener una idea más amplia y un conocimiento más certero sobre lo que en realidad son los denominados como “gases nobles”.
En comparación con la inmensidad del universo, nos queda aún muchísimo que aprender. Si nos limitamos a nuestro entorno más cercano, la Tierra, ¿cómo hemos podido llegar tan lejos?
¡La curiosidad! y ¡La necesidad! ¡El Instinto!
Fuente: Isaac Asimov
Publica: emilio silvera
Jul
21
¡La Curiosidad! La madre del saber
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)

¡Qué bonito sería si las piedras pudieran hablar! ¿Qué nos contarían éstas? ¿De qué escenas habrán sido testigos? Por aquí paseó Colón con los frailes franciscanos de La Rábida en Huelva

Hoy día no se construyen basílicas como esta de Santa María del Mar, en el barrio de la Ribera (Barcelona)
Todos los asiduos a este lugar, sabéis de mi curiosidad insaciable por las cosas, por lo que pasó, por las Civilizaciones antiguas, por los misterios que la materia encierra, y, en fin, por el Universo y las historias de las criaturas que lo pueblan y que, en la antigüedad, estuvieron aquí.
Existen lugares en los que, se han conservado más vivos y realistas los recuerdos del pasado y, en la India, donde al contrario que en la China, no cruzan el cielo los Dragones, serpientes o Aves monstruosas, nos dicen que fueron máquinas, las que, para el asombro de todos, cruzaban el cielo.

James Churchward, el desconcertante estudioso inglés cuyas investigaciones no son nada desdeñables, siempre y cuando no se aproximan a las especulaciones teosofistas, nos habla de un manuscrito que contiene la descripción de una nave aérea de hace 20.000 años.
“La energía” –detalla en una obra redactada varios lustros antes de que se hablara de astronaves y satélites artificiales- se obtiene de la atmósfera de manera simple y poco costosa. En la obra daba una amplia explicación del motor y sus compartimentos y cámaras y de las increíbles propiedades que la nave tenía que, incluso, podía quedar estática en el aire, o, salir disparada como un rayo hacia lo más alto del cielo hasta desaparecer de la vista.
¿Fantasías? Escuchemos un relato de la Academia Internacional de Investigaciones sánscritas de Mysore: “Los manuscritos cuya traducción del sánscrito presentamos, describen varios tipos de “vimana” (naves que se mueven por sí mismas), capaces de viajar por su propio impulso por tierra, agua y aire, y, asimismo, de planeta a planeta. Parece que los vehículos aéreos podían detenerse en el cielo hasta quedar inmóviles, y que estaban dotados de instrumentos capaces de señalar, incluso a distancia, la presencia de aparatos enemigos.
(El relato fue publicado en la India por el especialista Maharshi Bharadaja con el título Aeronáutica del pasado prehistórico.)
Numerosísimos testimonios nos vienen a confirman ampliamente lo anterior. Por ejemplo tenemos una amplia muestra en el Samaranganasutradhara que narra la historia de vuelos fantásticos realizados por el mundo, y hacia el Sol y las estrellas. Un documento de época pre-cristiana nos suministra una detallada descripción del carro celeste de Rama. La narración nos dice: “…el carro se movía por sí solo y era grande y estaba bien pintado; tenía dos pisos, muchas habitaciones y ventanas…”, cuyas hazañas, canta Valmiki el Herodoto indio: “El carro celeste, que posee una fuerza admirable, alada de velocidad, dorado en su forma y en su esplendor… El carro celeste ascendió por encima de la colina y del valle boscoso…alado como el rayo, dardo de Indra, fatal como el relámpago del cielo, envuelto en humo y destellos flameantes, rápida proa circular” (del Ramayana, que narra la epopeya de Rama).

Centenares y centenares de historias semejantes nos podemos encontrar a lo largo de las tradiciones hundúes: “ahí va la divina Maya volando en un carro de oro circular, que mide 12.000 codos de circunferencia, capaz de alcanzar las estrellas”, y, hete aquí el “caballo metálico del cielo” del rey Satrugit y el “carruaje del aire” del rey Pururavas. También el siglo IV de nuestra era encontramos a un héroe aeronauta, el monje budista Gunarvarman, quien se va desde Ceylán a Java en un aparato similar a los antiguos, sacado quién sabe de dónde.
Según se deduce de estos antiquísimos manuscritos en sánscrito, aquellos hindúes prehistóricos (o lo que realmente pudieran ser), no utilizaban aquellos ingenios voladores para excursiones de placer, sino que, según nos cuentan los relatos, las acciones bélicas eran también cotidianas que describen terribles batallas.
Un bajorrelieve en Angkor Wat (Camboya) representa a Rávana peleando en la batalla de Lanka, el clímax del Ramaiana.
Rávana, el rey de los demonios de Ceylán, enemigo mortal de Rama, “voló sobre los adversarios (según nos narra un manuscrito del año 500 a, de C.) haciendo caer ingenios que causaron grandes destrucciones. Finalmente, fue capturado y muerto, y su máquina celeste cayó en manos del capitán hindú Ram Chandra, quién, sirviéndose de ella, voló a la capital, Adjhudia…”
Y esto no son más que bagatelas. “El Bhisma Parva –recuerda Drake- menciona armas como la “verga de Brahma” y el “Rayo de Indra”, cuyos efectos se parecen a los producidos por la energía nuclear. El Drona Parva nos habla del “señor Mahadeva” y de sus terribles lanzas volantes (¿misiles?) capaces de destruir ciudades enteras fortificadas…, y describe las fantásticas armas de Agni, que aniquilaron ejércitos completos y devastaron la Tierra como bombas de Hidrógeno.”
¿Es posible que no se hayan conservado trazas de estos alucinantes conflictos? Los restos existen, y numerosísimos –responden los investigadores-. Basta que nos tomemos la molestia de ir en su busca. No es una empresa fácil, desde luego, puesto que, desde hace milenios la jungla se ha espesado sobre las ruinas, pero si consiguiéramos localizar todas las “ciudades muertas” de la gran península, constelaríamos el mapa de la India de tantos puntos como los que, en un Atlas, nos indican los centros de población actuales.

De vez en cuando aparecen descripciones a este respecto que nos dejan perplejos. El explorador De Camp, por ejemplo, refirió haber visto, en la zona que se extiende entre el Ganges y los montes Rajmahal, ruinas carbonizadas por algo que no podía ser un simple incendio, por violento que éste fuera. Algunas piedras gigantescas aparecían fundidas y desenterradas en varios puntos, “como bloques de estaño afectados por la salpicadura de una colada de acero”.
Más al Sur, el oficial británico J. Campbell se topó, en los años veinte, con ruinas similares, y quedó sorprendido por un extrañísimo detalle: en el pavimento semivitrificado de lo que debió de ser un patio interior, parecían haber sido impresas, por una fuerza desconocida, formas de cuerpos humanos.

Otros viajeros refieren haber descubierto en el corazón de los bosques indios ruinas de edificios nunca vistos, con paredes “semejantes a gruesas losas de cristal” asimismo perforadas, resquebrajadas y corroídas por agentes desconocidos. Y habiendo penetrado en una de estas construcciones, parecida a una cúpula baja, el explorador y cazador H. J. Hamilton se encontró con la mayor sorpresa de su vida.ç
“En una parte –recuerda-, el suelo cedió bajo mis pies con un extraño crujido. Me puse a seguro y, luego, ensanché con la culata del fusil el boquete que se había abierto, y me introduje en él. Me encontré en una estancia larga y estrecha que recibía luz por una grieta de la bóveda. Al fondo, vi una especie de mesa y un asiento del mismo “cristal” de que estaban hechas las paredes.

En el asiento, se enroscaba una forma extraña, de contornos vagamente humanos. Observándola de cerca, me pareció, al principio, que se trataba de una estatua deteriorada por la acción del tiempo, pero, luego, descubrí algo que me llenó de horror: bajo el “vidrio” que revestía aquella estatua, ¡se podían distinguir claramente los detalles del esqueleto!”.
Muros, muebles y seres humanos vitrificados… ¿Qué tremendos secretos se esconden entre las líneas del Mahabrata y del Drona Parva?
emilio silvera
Ene
14
Fenómenos inexplicables
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (24)
Comments (24)

Podemos explicar el Gran Cañón, y cómo está así constituido
Sin embargo, hay cosas que la razón no puede explicar, y, lo que está ocurriendo en esta página, es, sin duda, una de las cosas más extrañas que jamás contarse puedan. Se trata de lo siguiente: Esos números que abajo podéis contemplar, son los contadores de las visitas recibidas en los últimos días hasta ayer, en este Blog. Como podeis ver, rondan más de treinta mil al día de media.
Estamos en este mismo momento alcanzando los 36 millones de visitas.

Sí, es cierto, yo puedo explicar algunas cosas pero, la falta de comentarios en el Blog… es algo incomprensible para mí. No puedo imaginar que, aunque sean sólo unos pocos, no tengan la necesidad de plantear alguna pregunta, señalar un fallo cometido por mí, expresar el asombro que le produce tal o cual fenómeno, y, en fín, dejar constancia de que estuvo por aquí. Precisamente sabemos siempre de lo que pasó por las huellas dejadas por los que estuvieron allí.

No siempre, podemos dar una explicación satisfactoria a nuestros comportamientos. Se hacen cosas, o, se toman decisiones que, ni son lógicas ni están en consonancia con la realidad que, de alguna manera, indica procederes distintos a los que realmente se han ejecutado.
En el caso de los pocos comentaristas en este Blog, se podrían pensar muchas cosas que, serían el motivo del por qué, tan pocos aparecen para expresar lo que les parece o piensan del trabajo expuesto. Nadie está obligado a decir nada sobre lo que aquí tratamos. Sin embargo, es lógico pensar que, alguna vez, tenga la necesidad o el impulso, de decir alguna cosa que, por nimia que esta pueda ser, aquí quedará dicha.
Cuando en alguna ocasión me he quejado de este proceder, se alega que no todos están preparados para entablar un diálogo en este tipo de complejidades. Lo cierto es que, por mi parte, procuro explicarlo todo de manera sencilla y que todos lo puedan entender, evito las ecuaciaones y, de esa manera facilito que se puedan hacer preguntas, comentarios e incluso, criticar el trabajo.

Por mi parte, siempre me lo he tomado como el caso de un grupo de amigos que van al campo a pasarlo bien, han echado el día disfrutando de la Naturaleza y en paz, no pretendían otra cosa. Y, de la misma manera, deben pensar aquellos -la mayoría silenciosa- que, pasan por Blog para pasarlo bien, leen aquellos trabajos de los expuestos que más les puedan interesar y, sin más pretensiones, se quedan a la espera del siguiente día, en el que volverán a mirar si viene algo que les pueda despertar la curiosidad. Por sus mentes, nunca pasó la idea de comentar nada.

Unas simples palabras que son siempre bien acogidas
Claro que, por mi parte, expreso, simplemente, mi gran extrañeza que, de ninguna manera es desilución o frustración que, han quedado anuladas, ambas, por el número de visitantes que nos pagan el esfuerzo con su “presencia” que, aunque silenciosas, presencias son.
Como decía aquel sabio:
“Nuestra recompensa se encuentra en el esfuerzo y no en el resultado, un esfuerzo total es una victoria completa.”
En ese sentido, amigos míos, salimos victoriosos porque, darlo todo, a cambio de nada, es, ¡una alegría!
emilio silvera
PD
El que quiera decir algo es muy libre y, también es libre el que escoja callar. Sin embargo, se agradece el comentario que deja el visitante como muestra de que le gustó el tema aquí expuesto y, comentarlo con él/ellos, será siempre para mí, una gran satisfacción. Comentad anigos, al fin y al cabo es un pequeño pago por lo que yo os doy.
















 Totales: 75.650.125
Totales: 75.650.125 Conectados: 42
Conectados: 42



















:quality(70)/cloudfront-us-east-1.images.arcpublishing.com/metroworldnews/NHNPQ3MPWJHLVKK5HOVL4WSRWI.jpg)







