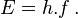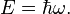Sep
8
El placer de Descubrir: Aventurarse por nuevos caminos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)

La molécula de agua es polar en virtud principalmente de su geometría angular.
¡Ah! ¿Pero sabemos?
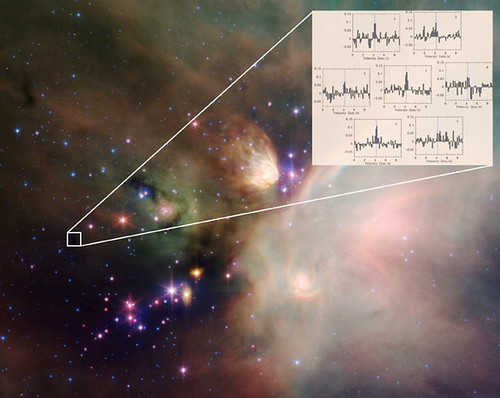
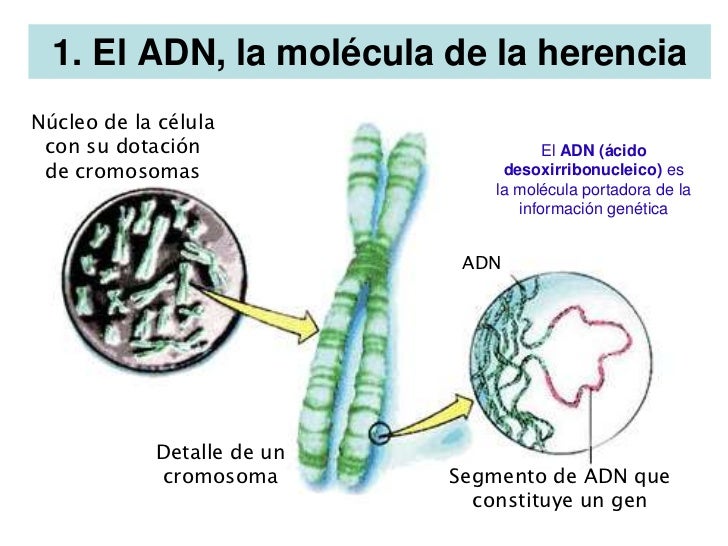
Los organismos vivos somos sistemas extremadamente complejos, formados por un elevado número de elementos interrelacionados que deben mantener sus características a lo largo del tiempo, de una generación a otra. Esto supone que debe existir algún mecanismo para que cada elemento de los organismos se elabore de acuerdo a un “plan”, a un modelo de organización establecido, y que ese modelo pueda ser transmitido de una célula a sus descendientes. Esta necesidad de los seres vivos nos acerca a la noción de información genética.
“Quien ha visto las cosas presentes ha visto todo, todo lo ocurrido desde la eternidad y todo lo que ocurrirá en el tiempo sin fin; pues todas las cosas son de la misma clase y la misma ”.
Marco Aurelio
Claro que él, quería significar que todo, desde el comienzo del mundo, ha sido igual, sigue unos patrones que se repiten una y otra vez a lo largo del transcurso de los tiempos: el día y la noche, las estaciones, el frío y el calor, el río muerto por la sequía o aquel que, cantarino y rumoroso ve correr sus aguas cristalinas hasta que desembocan en el océano. La Bondad y la maldad… Y, también, el Hombre y la Mujer. Así ha sido desde que podemos recordar y, así continuará siendo.


Para fugarnos de la tierra
un libro es el mejor bajel;
y se viaja mejor en el poema
que en más brioso corcel.
Whitman
Todas ellas pasaron por esas transformaciones
“Todo presente de una sustancia simple es naturalmente una consecuencia de su estado anterior, de modo que su presente está cargado de su futuro.”
Leibniz
Niels Bohr, citando a Gohete preguntaba: ¿Cuál es el camino? No hay ningún camino. Está claro el mensaje que tal pregunta y tal respuesta nos quiere hacer llegar, el camino, tendremos que hacerlo nosotros mediante la exploración hacia el futuro en el que está lo que deseamos encontrar. Hay que explorar y arriesgarse para tenemos que ir más allá de las regiones habituales y conocidas que nos tienen estancados siempre en el mismo lugar. A veces, para conseguir alguna cosa… ¡Hay que tomar riesgos!

Homero nos contó como Ulises de Ítaca se arriesgó a oír el canto de las sirenas amarrado al palo de la vela mayor de su embarcación. Él no que´ria ser atraído por aquellas fuerzas malignas pero quería sentir los efectos de aquella llamada en lugar seguro. Eso nos lleva a pensar que hay un mensaje en el pasaje de Homero: Arriesgarse… ¡Sí! Pero con las precauciones necesarias. Así que, cuidado con los Robots, con los experimentos científicos de todo tipo, y, sobre todo, no debemos creer que lo sabemos todo. Tenemos que ser conscientes de que, el peligro nos acecha por todas partes.
Pero, no cabe duda alguna de que, el acto de exploración modifica la perspectiva del explorador; Ulises, Marco Polo y Colón habían cambiado cuando volvieron a sus lugares de partida . Lo mismo ha sucedido en la investigación científica de los extremos en las escalas, desde la grandiosa extensión del espacio cosmológico hasta el mundo minúsculo y enloquecido de las partículas subatómicas.

La galaxia conocida por el nombre de Bella Durmiente
Una bella galaxia espiral de cien mil años-luz de diámetro que podemos comparar con…¡Un átomo! El tema de las medidas es relativo y todo se supedita a su ámbito natural, cada cosa tiene la medida que requiere su funciòn en el Universo, desde un átomo hasta una galaxia.

En ambos “universos” existe una descomunal diferencia en los extremos de las escalas. Sin embargo, la inmensa galaxia de arriba no sería posible sin la existencia de infinitesimal átomo de abajo. ¡Todo lo grande está hecho de cosas pequeñas!
Así que, cuando hacemos esos viajes, irremediablemente nos cambian, y, desde luego, desafían muchas de las concepciones científicas y filosóficas que, hasta ese momento, más valorábamos. Algunas tienen que ser desechadas, como el bagaje que se deja atrás en una larga travesía por el desierto. Otras tienen que ser modificadas y reconstruidas hasta quedar casi irreconocibles, ya que, lo que hemos podido ver en esos viajes, lo que hemos descubierto, nos han cambiado por completo el concepto y la perspectiva que del mundo teníamos, conocemos y sabemos.
La exploración del ámbito de las galaxias extendió el alcance de la visión humana en un factor de 1026veces mayor que la escala humana, y produjo la revolución que identificamos con la relatividad, la cual reveló que la concepción newtoniana del mundo sólo era un parroquianismo en un universo más vasto donde el espacio es curvo y el tiempo se hace flexible.

La exploración del dominio subatómico nos llevó lejos en el ámbito de lo muy pequeño, a 10-15 de la escala humana, y también significó una revolución. fue la Física cuántica que, transformó todo lo que abordó.
La teoría cuántica nació en 1900, Max Planck comprendió que sólo podía explicar lo que llamaba la curva del cuerpo negro -el espectro de energía que genera un objeto de radiación perfecta- si abandonaba el supuesto clásico de que la emisión de energía es continua, y lo reemplazó por la hipótesis sin precedentes de que la energía se emite en unidades discretas. Planck llamó cuantos a estas unidades.


1) Figura animada que representa un rayo de luz incidiendo sobre un cuerpo negro hasta su total absorción. 2) En la gráfica se representa la intensidad de la radiación emitida por el cuerpo negro en función de la longitud de onda a diferentes temperaturas. El máximo de la curva aumenta al ir hacia menores longitudes de onda (Ley de Wien). Se compara con el modelo clásico de Rayleigh-Jeans a altas temperaturas (5000 K) comprobándose la llamada catástrofe del ultravioleta
La constante de Planck es una constante física que desempeña un papel central en la teoría de la mecánica cuántica y recibe su nombre de su descubridor, Max Plancc, uno de los padres de dicha teoría. Denotada como 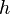 , es la constante que frecuentemente se define como el cuanto elemental de acción.Planck la denominaría precisamente «cuanto de acción»
, es la constante que frecuentemente se define como el cuanto elemental de acción.Planck la denominaría precisamente «cuanto de acción»
Fue inicialmente propuesta como la constante de proporcionalidad entre la energía 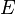 de un fotón y la frecuencia
de un fotón y la frecuencia 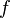 de su onda electromagnética asociada. Esta relación entre la energía y la frecuencia se denomina «relación de Planck»:
de su onda electromagnética asociada. Esta relación entre la energía y la frecuencia se denomina «relación de Planck»:
Dado que la frecuencia 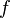 , la longitud de onda
, la longitud de onda 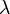 lambda” />, y la velocidad de la luz
lambda” />, y la velocidad de la luz  cumplen
cumplen  lambda . f = c ” />, la relación de Planck se puede expresar como:
lambda . f = c ” />, la relación de Planck se puede expresar como:
Otra ecuación fundamental en la que interviene la constante de Planck es la que relaciona el momento lineal 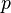 de una partícula con la longitud de onda de De Broglie λ de la misma:
de una partícula con la longitud de onda de De Broglie λ de la misma:
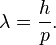 lambda =
lambda =
En aplicaciones donde la frecuencia viene expresada en términos de radianes por segundo o frecuencia angular, es útil incluir el factor 1/2 dentro de la constante de Planck. La constante resultante, «constante de Planck reducida» o «constante de Dirac», se expresa como ħ (“h barra“):
De esta forma la energía de un fotón con frecuencia angular  omega” />, donde
omega” />, donde 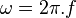 omega = 2 \pi . f” />, se podrá expresar como
omega = 2 \pi . f” />, se podrá expresar como
Por otro lado, la constante de Planck reducida es el cuanto del momento angular en mecánica cuántica.
Planck definió a “sus” cuantos en términos del “cuanto de acción”, simbolizado por la letra h que ahora, se ha convertido en el símbolo de una constante, la constante de Planck, h. Planck no era ningún revolucionario – a la edad de cuarenta y dos años era un viejo, juzgado por patrones de la ciencia matemática y, además, un pilar de la elevada cultura alemana del siglo XIX-, pero se percató fácilmente de que el principio cuántico echaría abajo buena de la física clásica a la que había dedicado la mayor parte de su carrera. “Cuanto mayores sean las dificultades -escribió-…tanto más importante será finalmente para la ampliación y profundización de nuestros conocimientos en la física.”
Sus palabras fueron proféticas: cambiando y desarrollándose constantemente, modificando su coloración de manera tan impredecible como una reflexión en una burbuja de , la física cuántica pronto se expandió practicamente a todo el ámbito de la física, y el cuanto de acción de Planck, h llegó a ser considerado una constante de la Naturaleza tan fundamental como la velocidad de la luz, c, de Einstein.

Dos buenos amigos, dos genios
Max Planck es uno de los científicos a los que más veces se le han reconocido sus méritos y, su , está por todas partes: La Constante de Planck, las Unidades de Planck, El cuanto de Planck, la Radiación de Planck, El Tiempo de Planck, la masa de Planck, la Energía de Planck, la Longitud de Planck… ¡Todo merecido!

Confinados en nuestro pequeño mundo, una mota de polvo en la inmensidad de una Galaxia grandiosa que, a su vez, forma parte de un universo “infinito”, hemos podido darnos traza para poder saber, a pesar de las enormes distancias, sobre lo que existe en regiones remotas del Universo. Un Universo formado por Supercúmulos de galaxias que formadas en grupos conforman la materia visible, y, dentro de cada una de esas galaxias, como si de universos se tratara, se reproducen todos los objetos y fenómenos que en el Universo son.
The Scale of the Universe 2 – HTwins.net
Sigamos con la escala del Universo conocido y hagamos un pequeño esquema que lo refleje: El Universo Observable, la mayor escala que abarca más de 100 mil trillones de kilómetros (según nos cuenta Timothy Ferris:
Radio en metros Objetos característicos
1026 Universo observable
1024 Supercúmulos de Galaxias
1023 Cúmulos de Galaxias
1022 Grupo de Galaxias (por ejemplo el Grupo Local)
1021 Galaxia La Vía Láctea
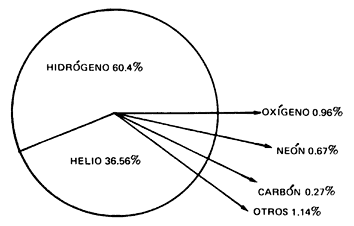
Nube Molecular gigante muy masiva, de gas y polvo compuesta fundamentalmente de moléculas con diámetro típico de 100 a.l. Tienen masa de diez millones de masas solares (moléculas de Hidrógeno (H2) el 73% en masa), átomos de Helio (He, 25%), partículas de polvo (1%), Hidrógeno atómico neutro (H I, del 1%) y, un rico cóctel de moléculas interestelares. En nuestra galaxia existen al menos unas 3000 Nubes Moleculares Gigantes, estando las más masivas situadas cerca de la radio-fuente Sagitario B en el centro Galáctico.
1018 Nebulosas Gigantes, Nubes Moleculares
1012 Sistema Solar
1011 Atmósfera externa de las Gigantes rojas

Aunque a una Unidad Astronómica de distancia (150 millones de Kilómetros de la Tierra), el Sol caliente el planeta y nos da la vida
109 El Sol
108 Planetas Gigantes Júpiter
107 Estrellas enanas, planetas similares a la Tierra
105 Asteroides, núcleos de cometas
104 Estrellas de Neutrones
Los seres humanos son parte del Universo que queremos descubrir.
1 Seres Humanos
10-2 Molécula de ADN (eje largo)
10-5 Células vivas
Células vivas
10-9 Molécula de ADN (eje corto)
10-10 Átomos
10-14 Núcleos de átomos pesados
10-15 Protones y Neutrones
10-35 Longitud de Planck: cuanto de espacio; radio de partículas sin dimensiones = la cuerda.

Es la escala de longitud a la que la descripción clásica de la Gravedad cesa de ser válida y debe ser tenida en la mecánica cuántica. Está dada por la ecuación de arriba, donde G es la constante gravitacional, ħ es la constante de Planck racionalizada y c es la velocidad de la luz. El valor de la longitud de Planck es del orden de 10-35 m (veinte órdenes de magnitud menor que el tamaño del protón 10-15 m).
Me llama la atención y me fascina la indeterminación que está inmersa en el mundo cuántico. La indeterminación cuántica no depende del aparato experimental empleado investigar el mundo subatómico. Se trata, en la medida de nuestro conocimiento, de una limitación absoluta, que los más destacados sabios de una civilización extraterrestre avanzada compartirían con los más humildes físicos de la Tierra.

Por muy avanzados que pudieran estar, ellos también estarían supeditados al Principio de Incertidumbre o Indeterminación cuántica, y, como nosotros, cuando trataran de encontrar (sea cual fuese las matemáticas o sistemas que emplearan para hallarlo) el resultado de la constante de estructura fina, la respuesta sería la misma: 137, puro y adimensional.
Todo esto nos ha llevado a la más firme convicción definir la visión del mundo de la física que nos revelaba que no sólo la materia y la energía sino que también el conocimiento están cuantizados. Cuando un fotónchoca con un átomo, haciendo saltar un electrón a una órbita más elevada, el electrón se mueve de la órbita inferior a la superior instantáneamente, sin tener que atravesar el espacio intermedio. Los mismos radios orbitales están cuantizados, y el electrón simplemente deja de existir en un punto para aparecer simultáneamente en otro. Este es el famoso “salto cuántico” que tanto desconcierta, y no es un mero problema filosófico, es una realidad que, de , no hemos llegado a comprender.

No, esto no es un salto cuántico. Simplemente le tocó la Lotería
Pero, ¿quién sabe? Quizás un día lejano aún en el tiempo, cuando descubramos el secreto que salto cuántico nos esconde, podremos aprovechar la misma técnica que emplea la Naturaleza con los electrones hacer posible que se transporten de un lugar a otro sin tener que recorrer las distancias que separan ambos destinos.

Estaría bien poder trasladarse las estrellas por ese medio
Bueno, pongamos los pies en el suelo, volvamos a la realidad. La revolución cuántica ha sido penosa, pero podemos agradecerle que, nos haya librado de muchas ilusiones que afectaban a la visión clásica del mundo. Una de ellas era que el hombre es un ser aparte, separado de la naturaleza a la que en realidad, no es que esté supeditado, sino que es, ella. ¡Somos Naturaleza!
Está claro, como nos decía Immanuel Kant que:
“La infinitud de la creación es suficientemente grande como para que un mundo, o una Vía Láctea de mundos, parezca, en comparación con ella, lo que una flor o un insecto en comparación con la Tierra.”

Algún día podríamos desaparecer en una especie de plasma como ese de la imagen y salir al “otro lado” que bien (¡Por qué no) podría ser otra galaxias lejana. Creo que la imaginación se nos ha dado para algo y, si todo lo que podemos imaginar se realizar, la conclusión lógica es que sólo necesitamos ¡Tiempo!
Sí, amigos míos, la Naturaleza vive en constante movimiento, y, nosotros, que formamos parte de ella…También vivimos en una constante evolución física y del conocimiento. Tenemos que llegar a conocerla.
Existen muchos mundos con dos soles, ¿cómo será vivir en uno de ellos?
En tiempos y lugares totalmente inciertos,
Los átomos dejaron su camino celeste,
Y mediante abrazos fortuitos,
Engendraron todo lo que existe.
Maxwell
Doy las gracias a Timothy Ferris de cuyo libro, La Aventura del Universo, he podido obtener bellos pasajes que aquí, quedan incluídos.
emilio silvera
Feb
9
Viajar desde el núcleo atómico hasta las galaxias
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (2)
Comments (2)
Interacciones fundamentales
El propio Rutherford empezó a vislumbrar la respuesta a la que arriba hacemos. Entre 1.906 y 1.908 (hace más de un siglo) realizó constantes experimentos disparando partículas alfa contra una lámina sutil de metal (como oro o platino), para analizar sus átomos. La parte de los proyectiles atravesaron la barrera sin desviarse (como balas a través de las hojas de un árbol), pero no todos.
En la placa fotográfica que le sirvió de blanco tras el metal, Rutherford descubrió varios impactos dispersos e insospechados alrededor del punto central. Comprobó que algunas partículas habían rebotado. Era como si en vez de atravesar las hojas, algunos proyectiles hubiesen chocado contra algo más sólido. Rutherford supuso que aquella “balas” habían chocado contra una especie de núcleo denso, que ocupaba sólo una parte mínima del volumen atómico y ese núcleo de intensa densidad desviaban los proyectiles que acertaban a chocar contra él. Ello ocurría en muy raras ocasiones, lo cual demostraba que los núcleos atómicos debían ser realmente ínfimos, porque un proyectil había de por fuerza muchos millones de átomos al atravesar la lámina metálica

Era lógico , pues, que los protones constituían ese núcleo duro. Rutherford representó los protones atómicos como elementos apiñados alrededor de un minúsculo “núcleo atómico” que servía de centro (después de todo eso, hemos podido que el diámetro de ese núcleo equivale a algo más de una cienmilésima del volumen total del átomo).
En 1.908 se concedió a Rutherford el premio Nobel de Química por su extraordinaria labor de investigación sobre la naturaleza de la materia. Él fue el de importantes descubrimientos que permitieron conocer la estructura de los átomos en esa primera avanzadilla.
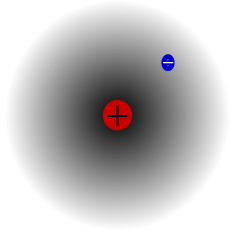
Átomo de hidrógeno, núcleo y electrón.
Desde entonces se pueden describir con términos más concretos los átomos específicos y sus diversos comportamientos. Por ejemplo, el átomo de hidrógeno posee un solo electrón. Si se elimina, el protón restante se asocia inmediatamente a alguna molécula vecina; y cuando el núcleo desnudo de hidrógeno no encuentra por este medio un electrón que participe, actúa como un protón (es decir, una partícula subatómica), lo cual le permite penetrar en la materia y reaccionar con otros núcleos si conserva la suficiente energía.

El helio, que posee dos electrones, no cede uno con tanta facilidad. Sus dos electrones un caparazón hermético, por lo cual el átomo es inerte. No obstante, si se despoja al helio de ambos electrones, se convierte en una partícula alfa, es , una partícula subatómica portadora de dos unidades de carga positiva.

Hay un tercer elemento, el litio, cuyo átomo tiene electrones. Si se despoja de uno o dos, se transforma en ión, y si pierde los tres, queda reducida a un núcleo desnudo, con una carga positiva de tres unidades.
Las unidades de carga positiva en el núcleo atómico deben ser numéricamente idénticas a los electrones que contiene por norma, pues el átomo suele ser un cuerpo neutro, y esta igualdad de lo positivo con lo negativo es el equilibrio. De hecho, los números atómicos de sus elementos se basan en sus unidades de carga positiva, no en las de carga negativa, porque resulta fácil hacer variar el de electrones atómicos dentro de la iónica, pero en cambio se encuentran grandes dificultades si se desea alterar el número de sus protones.

Apenas esbozado este esquema de la construcción atómica, surgieron nuevos enigmas. El de unidades con carga positiva en un núcleo no equilibró, en ningún caso, el peso nuclear ni la masa, exceptuando el caso del átomo de hidrógeno. Para citar un ejemplo, se averiguó que el núcleo de helio tenía una carga positiva dos veces mayor que la del núcleo de hidrógeno; pero como ya se sabía, su masa era cuatro veces mayor que la de este último. Y la situación empeoró progresivamente a medida que se descendía por la tabla de elementos, e incluso cuando se alcanzó el uranio, se encontró un núcleo con una masa igual a 238 protones, pero una carga que equivalía sólo a 92.
¿Cómo era posible que un núcleo que contenía cuatro protones (según se suponía el núcleo de helio) tuviera sólo dos unidades de carga positiva? Según la más y primera conjetura emitida, la presencia en el núcleo de partículas cargadas negativamente y con peso despreciable neutralizaba dos unidades de carga. Como es natural, se pensó también en el electrón. Se podría componer el rompecabezas si se suponía que en núcleo de helio estaba integrado por cuatro protones y dos electrones neutralizadores, lo cual deja libre una carga positiva neta de dos, y así sucesivamente, hasta llegar al uranio, cuyo núcleo tendría, pues, 238 protones y 146 electrones, con 92 unidades libres de carga positiva. El hecho de que los núcleos radiactivos emitieran electrones (según se había comprobado ya, por ejemplo, en el caso de las partículas beta), reforzó esta idea . Dicha teoría prevaleció durante más de una década, hasta que por caminos indirectos, llegó una respuesta mejor como resultado de otras investigaciones.
Pero entre tanto se habían presentado algunas objeciones rigurosas contra dicha hipótesis. Por lo , si el núcleo estaba constituido esencialmente de protones, mientras que los ligeros electrones no aportaban prácticamente ninguna contribución a la masa, ¿cómo se explicaba que las masas relativas de varios núcleos no estuvieran representadas por enteros? Según los pesos atómicos conocidos, el núcleo del átomo cloro, por ejemplo, tenía una masa 35’5 veces mayor que la del núcleo de hidrógeno. ¿Acaso significaba esto que contenía 35’5 protones? Ningún científico (ni entonces ni ahora) podía aceptar la existencia de medio protón.
Este singular interrogante encontró una respuesta incluso antes de solventar el problema , y ello dio lugar a una interesante historia.

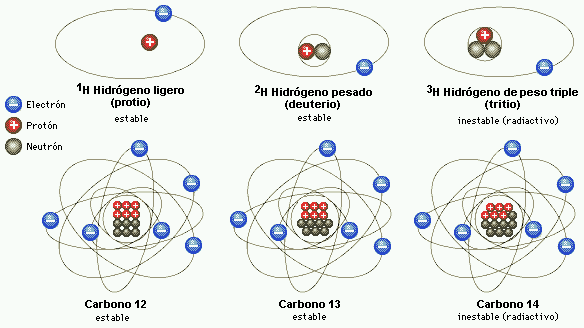
Los tres isótopos naturales del carbono: carbono-12 (6 protones y 6 neutrones), carbono-13 (6 protones y 7 neutrones) y carbono-14 (6 protones y 8 neutrones). En los tres casos es carbono, tiene el aspecto de carbono y se comporta químicamente como carbono, por tener seis protones (y forma parte de nuestro organismo, por ejemplo). Sin embargo, sus propiedades físicas varían. Por ejemplo, mientras que el carbono-12 y el carbono-13 son estables, el carbono-14 es inestable y radioactivo: emite radiación beta, uno de sus neutrones “extras” se transforma así en un protón y el núcleo se convierte en nitrógeno-14 (que tiene 7 protones y 7 neutrones), con el aspecto y las propiedades del nitrógeno (por tener 7 protones). Dado que la mitad de la masa del carbono-14 pasa a ser nitrógeno-14 cada 5.730 años aproximadamente (más o menos lo que llevamos de civilización humana), la presencia de este isótopo natural resulta especialmente útil para la datación precisa de objetos históricos.
Isótopos; construcción de bloques uniformes
Allá por 1.816, el físico inglés William Prout había insinuado ya que el átomo de hidrógeno debía en la constitución de todos los átomos. Con el tiempo se fueron desvelando los pesos atómicos, y la teoría de Prout quedó arrinconada, pues se comprobó que muchos elementos tenían pesos fraccionarios (para lo cual se tomó el oxígeno, tipificado al 16). El cloro, según dije antes, tiene un peso atómico aproximado de 35’5, o para ser exactos, 35’457. otros ejemplos son el antimonio, con un peso atómico de 121’75, el galio con 137’34, el boro con 10’811 y el cadmio con 112’40.

El Uranio 235 que es el único que de manera natural es apto para la fisión nuclear, es escaso, sólo el 7 por 1.000 es uranio 235, el , es uranio 238 que, no es combustible nuclear y, como la madera mojada, no arde. Sin embargo, si se bombardea con neutrones lentos del uranio 235, resulta que se convierte en Plutonio 239 que sí, es combustible nuclear válido. ¡Qué no idearemos para los objetivos!
El Uranio es muy radiactivo y si está enriquecido… ¡Ya sabemos las consecuencias!
Hacia principios de siglo se hizo una de observaciones desconcertantes, que condujeron al esclarecimiento. El inglés William Crookes (el del tubo Crookes) logró disociar del uranio una sustancia cuya ínfima cantidad resultó ser mucho más radiactiva que el propio uranio. Apoyándose en su experimento, afirmó que el uranio no tenía radiactividad, y que ésta procedía exclusivamente de dicha impureza, que él denominó uranio X. Por otra parte, Henri Becquerel descubrió que el uranio purificado y ligeramente radiactivo adquiría mayor radiactividad con el tiempo, por causas desconocidas. Si se deja reposar durante algún tiempo, se extraer de él repetidas veces uranio activo X. Para decirlo de otra manera, por su propia radiactividad, el uranio se convertía en el uranio X, más radiactivo aún.
Por entonces, Rutherford, a su vez, separó del torio un torio X muy radiactivo, y comprobó también que el torio seguía produciendo más torio X. Hacia aquellas fechas se sabía ya que el más famoso de los elementos radiactivos, el , emitía un gas radiactivo, denominado radón. Por tanto, Rutherford y su ayudante, el químico Frederick Soddy, dedujeron que durante la emisión de sus partículas los átomos radiactivos se transformaron en otras variedades de átomos radiactivos.
El Radón, uno de los llamados gases nobles, es incoloro, inodoro e insípido, además de –para nuestro mal- radioactivo. Suele presentarse según el tipo de suelos de determinadas zonas y con la descomposición de uranio, concentrándose en la superficie y siendo “arrastrado” en y por el aire que respiramos, y es en grandes cantidades es un gas perjudicial para la salud… y que anticipa terremotos.


químicos que investigaron tales transformaciones lograron obtener un surtido muy variado de nuevas sustancias, a las que dieron nombres tales como A, B, mesotorio I, mesotorio II y actinio C. Luego los agruparon todos en tres series, de acuerdo con sus historiales atómicos. Una serie se originó del uranio disociado; otra del torio, y la tercera del actinio (si bien más tarde se encontró un predecesor del actinio, llamado protactinio).
En total se identificaron unos cuarenta miembros de esas series, y cada uno se distinguió por su peculiar esquema de radiación. Pero los finales de las tres series fueron idénticos: en último término, todas las cadenas de sustancias conducían al mismo elemento, el plomo.
Ahora bien, esas cuarenta sustancias no podían ser, sin excepción, elementos disociados. Entre el uranio (92) y el plomo (82) había sólo diez lugares en la tabla periódica, y todos ellos, salvo dos, pertenecían a elementos conocidos.
En realidad, los químicos descubrieron que aunque las sustancias diferían entre sí por su radiactividad, algunas tenían propiedades químicas idénticas. Por ejemplo, ya en 1.907 los químicos americanos Herbert Newby McCoy y W. H. Ross descubrieron que el radiotorio (uno entre los varios de la desintegración del torio) mostraba el mismo comportamiento químico que el torio, y el D, el mismo que el plomo, tanto que a veces era llamado radioplomo. De todo lo cual se infirió que tales sustancias eran en realidad variedades de mismo elemento: el radiotorio, una forma de torio; el radioplomo, un miembro de una familia de plomos; y así sucesivamente.
En 1.913, Soddy esclareció esta idea y le dio más amplitud. Demostró que cuando un átomo emitía una partícula alfa, se transformaba en un elemento que ocupaba dos lugares más abajo en la lista de elementos, y que cuando emitía una partícula beta, ocupaba, después de su transformación, el lugar inmediatamente . Con arreglo a tal norma, el radiotorio descendía en la tabla hasta el lugar del torio, y lo mismo ocurría con las sustancias denominadas uranio X y uranio Y, es decir, que los tres serían variedades del elemento 90. Así mismo, el radio D, el radio B, el torio B y el actinio B compartirían el lugar del plomo como variedades del elemento 82.
Soddy dio el de isótopos (del griego iso y topos, “el mismo lugar”) a todos los miembros de una familia de sustancias que ocupaban el mismo lugar en la tabla periódica. En 1.921 se le concedió el premio Nobel de Química.
El modelo protón–electrón del núcleo concordó perfectamente con la teoría de Soddy sobre los isótopos. Al retirar una partícula alfa de un núcleo, se reducía en dos unidades la carga positiva de dicho núcleo, exactamente lo que necesitaba para bajar dos lugares en la tabla periódica. Por otra parte, cuando el núcleo expulsaba un electrón (partícula beta), quedaba sin neutralizar un protón adicional, y ello incrementaba en una unidad la carga positiva del núcleo, lo cual era como agregar una unidad al atómico, y por tanto, el elemento pasaba a ocupar la posición inmediatamente superior en la tabla periódica de los elementos. ¡Maravilloso!
¿Cómo se explica que cuando el torio se descompone en radiotorio después de sufrir no una, sino tres desintegraciones, el producto siga siendo torio? Pues bien, en este proceso el átomo de torio pierde una partícula alfa, luego una partícula beta, y más tarde una segunda partícula beta. Si aceptamos la teoría sobre el bloque constitutivo de los protones, ello significa que el átomo ha perdido cuatro electrones (dos de ellos contenidos presuntamente en la partícula alfa) y cuatro protones. (La situación actual difiere bastante de este , aunque en cierto modo, esto no afecta al resultado).
El núcleo de torio constaba inicialmente (según se suponía) de 232 protones y 142 electrones. Al haber perdido cuatro protones y otros cuatro electrones, quedaba reducido a 228 protones y 138 electrones. No obstante, conservaba todavía el atómico 90, es decir, el mismo de antes.
Así pues, el radiotorio, a semejanza del torio, posee 90 electrones planetarios, que giran alrededor del núcleo. Puesto que las propiedades químicas de un átomo están sujetas al de sus electrones planetarios, el torio y el radiotorio tienen el mismo comportamiento químico, sea cual fuere su diferencia en peso atómico (232 y 228 respectivamente).
Los isótopos de un elemento se identifican por su peso atómico, o número másico. Así, el torio corriente se denomina torio 232, y el radiotorio, torio 228. Los isótopos radiactivos del plomo se distinguen también por estas denominaciones: plomo 210 (radio D), plomo 214 (radio B), plomo 212 (torio B) y plomo 211 (actinio B).

Se descubrió que la noción de isótopo podía aplicarse indistintamente tanto a los elementos estables como a los radiactivos. Por ejemplo, se comprobó que las tres series radiactivas anteriormente mencionadas terminaban en tres formas distintas de plomo. La serie del uranio acababa en plomo 206, la del torio en plomo 208 y la del actinio en plomo 207. cada uno de estos era un isótopo estable y corriente del plomo, pero los tres plomos diferían por su peso atómico.
Mediante un dispositivo inventado por cierto ayudante de J. J. Thomson, llamado Francis William Aston, se demostró la existencia de los isótopos estables. En 1.919, Thomson, empleando la versión primitiva de aquel artilugio, demostró que el neón estaba constituido por dos variedades de átomos: una cuyo de masa era 20, y otra con 22. El neón 20 era el isótopo común; el neón 22 lo acompañaba en la proporción de un átomo cada diez. Más tarde se descubrió un tercer isótopo, el neón 21, cuyo porcentaje en el neón atmosférico era de un átomo por cada 400.
Entonces fue posible, al fin, razonar el peso atómico fraccionario de los elementos. El peso atómico del neón (20, 183) representaba el peso conjunto de los tres isótopos, de pesos diferentes, que integraban el elemento en su estado natural. Cada átomo individual tenía un másico entero, pero el promedio de sus masas (el peso atómico) era un número fraccionario.
Aston procedió a que varios elementos estables comunes eran, en realidad, mezclas de isótopos. Descubrió que el cloro, con un peso atómico fraccionario de 35’453, estaba constituido por el cloro 35 y el cloro 37, en la proporción de cuatro a uno. En 1.922 se le otorgó el premio Nobel de Química.

Sabiendo todo lo anteriormente explicado, hemos llegado a comprender cómo parte de la Astronomía que estudia las características físicas y químicas de los cuerpos celestes, la astrofísica es la parte más de la astronomía en la actualidad debido a que, al avanzar la física moderna: Efecto Doppler-Fizeau, el efecto Zeeman, las teorías cuánticas y las reacciones termonucleares aplicadas al estudio de los cuerpos celestes han permitido descubrir que el magnético solar, el estudio de las radiaciones estelares y sus procesos de fusión nuclear, y determinar la velocidad radial de las estrellas, etc. La radiación electromagnética de los cuerpos celestes permite realizar análisis de los espectros que nos dicen de qué están hechas las estrellas y los demás cuerpos del espacio interestelar y, de esa manera, hemos ido conociendo la materia y sus secretos que cada vez, van siendo menos.
emilio silvera
Jul
2
Dilvurgar la Cienca siempre será positivo
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)

Historia F+Q
Enseñando física y química a través de su historia. Un blog colaborativo de los alumnos del Master de Secundaria


Tal y como comentan Vollhardt y Schore (2007),

En 1985, Curl, Kroto y Smalley efectuaron un sorprendente descubrimiento, que les valió el premio Nobel de Química en 1996: el buckminsterfullereno, de fórmula molecular C60, una nueva forma alotrópica de carbono, de estructura semejante a una pelota de fútbol. Concretamente, observaron que la evaporación del grafito por acción del láser originaba diversos agregados de carbono en fase vapor, entre los que abundaban especies de 60 átomos. La estructura que mejor explica este agregado y que respeta la tetravalencia de carbono es la que forman 20 anillos de benceno fusionados, combándose sobre sí mismos hasta adoptar una disposición esférica con las valencias “sobrantes” definiendo 12 pentágonos: una especie de icosaedro truncado de 60 vértices equivalentes. La molécula fue bautizada como buckminsterfullereno, en honor a Buckminster Fuller, ya que su forma recuerda a las bóvedas geodésicas que él diseñaba(Bellapart, 2016). (…)

El enorme interés que suscitó el hallazgo del C60 condujo rápidamente a varios descubrimientos interesantes y al desarrollo de numerosas aplicaciones, de entre las que destacan, por su potencial utilidad, los nanotubos (Silvera, 2017), moléculas cilíndricas basadas en el motivo estructural de los fullereno.> (p. 680)
Pero este acercamiento a los alótropos del Carbono por parte del mundo del arte, representado en este caso por la arquitectura, no es, ni mucho menos, el primero del que se tiene constancia. De hecho, no hay más que recordar cómo Supermán, con solo la fuerza de su puño, era capaz de convertir el carbón en diamante. (Salkind, Salkind y Lester, R., 1983)…

¿Cómo es posible que algo tan pequeño como el Carbono esconda tantas posibilidades? La respuesta la sabíais antes de que os preguntase… ¡Gracias a la química!:)
A partir de este texto y del clip de vídeo, la actividad que se le plantearía a los alumnos sería un trabajo por grupos de 4 personas. El trabajo duraría tres días: en el primero se repartiría el texto y se empezarían a trabajar las cuestiones más prácticas. En el segundo juntarían y cribarían la información recabada en su casa, y prepararían la exposición de los apartados, uno de los cuales (elegido al azar por la profesora) tendrían que presentar al resto de la clase al día siguiente.
Las cuestiones que se les plantearían en el trabajo serían las siguientes:
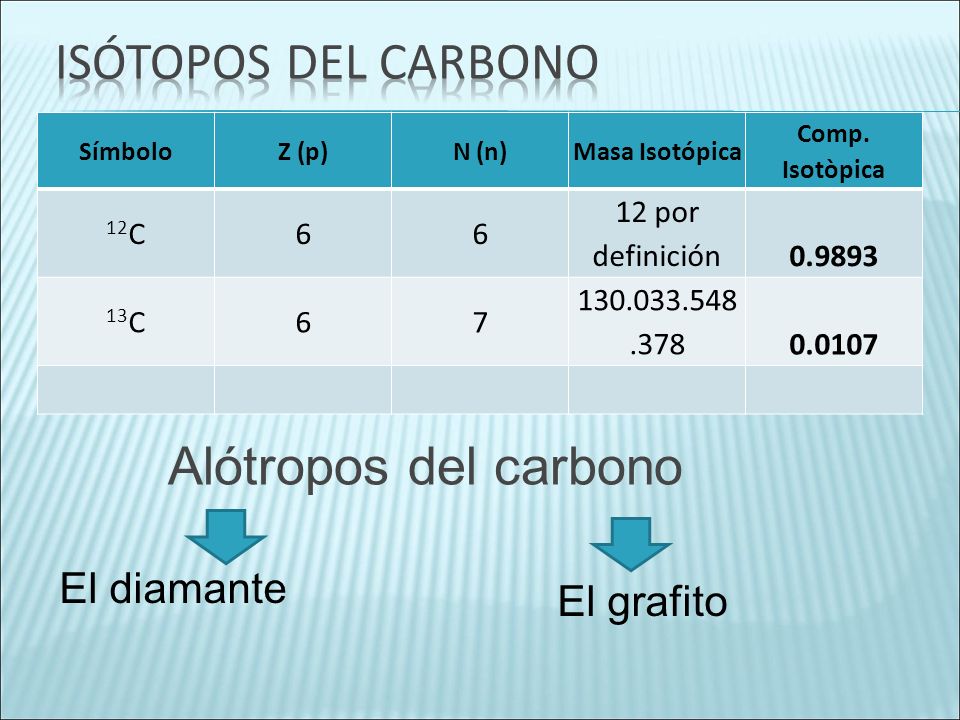
A) El año pasado estudiasteis el concepto de alótropo. Definidlo y nombrad al menos tres alótropos más de los más significativos para el Carbono (hay más de 40).
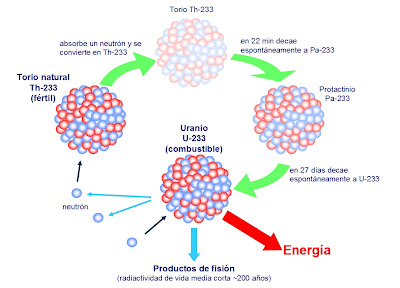
B) Si sumamos la os conocimientos del año pasado lo que habéis recordado que hacía Supermán, podréis completarsin problemas los recuadros del siguiente diagrama extraído de Nóguez (2013).
Si os fijáis, debajo del diagrama aparece el valor de la energía libre de la reacción para el paso de diamante a grafito. ¿Qué os sugiere este dato? ¿Cómo lo explicaríais, sabiendo que viene dado a temperatura y presión ambientales? ¿Qué consecuencias tiene y cómo lo justificaríais, considerando vuestra experiencia.
C) Justificad y esquematizad, según la teoría de enlace de valencia y de los orbitales híbridos, los enlaces covalentes existentes entre los átomos de los dos alótropos del Carbono mencionados en el texto, diamante y fullereno, así como de al menos otro del que conozcáis las características estructurales.
D) En vuestra casa, buscad información acerca de las aplicaciones potenciales del fullereno, y de su relevancia tecnológica. Además, buscad al menos otro ejemplo representativo de elemento con formas alotrópicas cuyas propiedades sean muy diferentes entre sí.

Objetivos de la actividad:
-Recordar y ampliar el concepto de alótropo, ya visto en Física y Química de 1º de Bachillerato.
-Entender el diagrama de fases que relaciona los alótropos cristalinos del carbono, así como sus distintas propiedades y aplicaciones.
-Recordar y aplicar el concepto de variación de entalpía, variación de entropía y Energía Libre de Gibbs en una reacción química, que se verá en mayor detalle en el siguiente bloque.
-Afianzar la teoría de enlace de valencia y la teoría de orbitales híbridos, que se habría explicado los días previos en clase. Aplicar dicha teoría correctamente al ejemplo de los alótropos del carbono.
-Familiarizarse con la búsqueda de información científica.
-Desarrollar las competencias de trabajo en equipo y de comunicación y expresión oral.
![]()
Un nuevo alótropo del silicio promete revolucionar la industria fotovoltaica
Criterios de evaluación:
-Entiende y define adecuadamente el concepto de alotropía química. Está ampliamente familiarizado con el ejemplo del Carbono: conoce y nombra a sus alótropos más significativos, sabe cómo se relacionan en el diagrama de fases, qué estructura tiene cada uno y cuáles son sus propiedades y aplicaciones más relevantes. (30%)
-Es capaz explicar el enlace covalente y la geometría de distintas moléculas sencillas empleando la teoría de hibridación. (40%)
-Recuerda el concepto de Energía Libre de Gibbs, Es capaz de justificar la espontaneidad de una reacción química considerando tanto sus factores entálpicos como entrópicos. (5%)
-Encuentra información adecuada, que evalúa e integra crítica y justificadamente en el contexto que se le pide. (5%)
-Trabaja en equipo de forma cooperativa. (5%)
-Expone de forma clara y crítica sus resultados al resto de la clase, al igual que escucha y participa en los expuestos por sus compañeros. (15%)
Referencias
-Bellapart (2016). Magic Badalona Mall. Bellapart. Recuperado en : http://www.bellapart.com/en/projects/estructura-prueba/magic-badalona-mall.html
-Nóguez, Á. (2013). Elementos no metálicos y sus compuestos. Slide Share. Recuperado de: https://es.slideshare.net/Angelnoguez/elementos-no-metlicos-y-suscompuestos.
-Salkind, Salkind (productores) y Lester, R. (director). (1983). Superman III [Cinta cinematográfica]. EU.: Warner Bros Pictures.
-Silvera, V. (2017) El grafeno es uno de los materiales del futuro. España: Blog de Emilio Silvera V. Dedicado al Universo, la Mente y la Ciencia en general. Recuperado de: http://www.emiliosilveravazquez.com/blog/2017/03/19/%C2%A1la-fisica-%C2%BFhasta-donde-nos-llevara-5/-Villatoro, F. R. (2014) Supermán y la cristalografía en el cine. La ciencia de la Mula Francis. Recuperado de: http://francis.naukas.com/2014/06/16/superman-y-la-cristalografia-en-el-cine/
-Vollhardt, K. P., Schore, N. E., (2007) Química Orgánica, Estructura y función (Martínez, D.A., trad.). Universidad de California , E.U.: Ediciones Omega.
Jun
9
Moléculas, sustancias, cuerpos…
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)
Es allí, en las estrellas, en sus hornos nucleares y en las explosiones de supernovas, donde a miles de millones de grados de temperatura, se crean los elementos más complejos que el hidrógeno y el helio. Aparece el litio, el carbono, el silicio o el nitrógeno y el hierro.

De estos materiales estamos nosotros hechos, y, lógicamente, se fabricaron en las estrellas.
En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es:
H, He, (Li, Be, B) C, N, O…… Fe
¿Apreciáis la maravilla? Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del Universo y…. de la vida inteligente.

El telescopio VLT (Very Large Telescope) de ESO ha obtenido imágenes de una fascinante región de formación de estrellas en la Gran Nube de Magallanes — una de las galaxias satélite de la Vía Láctea. Esta precisa imagen revela dos peculiares y brillantes nubes de gas: la rojiza NGC 2014 y su vecina azulada NGC 2020. Pese a que son muy diferentes, ambas fueron esculpidas por potentes vientos estelares procedentes de estrellas recién nacidas extremadamente calientes que también irradian el gas, provocando que brille de forma intensa. (para verla entera hay que pasar la rgla hacia la derehca).

Pero está claro que, todo el proceso estelar evolutivo inorgánico nos condujo desde el simple gas y polvo cósmico a la formación de estrellas y nebulosas solares hasta los planetas, la Tierra en particular, en cuyo medio ígneo describimos la formación de las estructuras de los silicatos, desplegándose con ello una enorme diversidad de composiciones, formas y colores, asistiéndose, por primera vez en la historia de la materia, a unas manifestaciones que contrastan con las que hemos mencionado en relación al proceso de las estrellas.
Desde el punto de vista del orden es la primera vez que nos encontramos con objetos de tamaño comparables al nuestro, en los que la ordenación de sus constituyentes es el rasgo más característico.
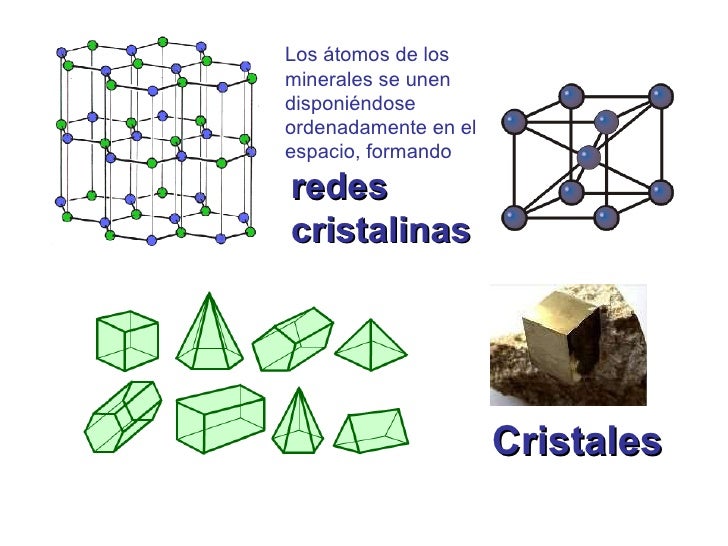
Al mismo tiempo nos ha parecido reconocer que esos objetos, es decir, sus redes cristalinas “reales”, almacenan información (memoria) que se nos muestra muy diversa y que puede cobrar interés en ciertos casos, como el de los microcristales de arcilla, en los que, según Cairos-Swith, puede incluso llegar a transmitirse.
Porque ¿qué sabemos en realidad de lo que llamamos materia inerte? Lo único que sabemos de ella son los datos referidos a sus condiciones físicas de dureza, composición, etc., en otros aspectos, ni sabemos si pueden existir otras propiedades distintas a las meramente-físicas.
¿No os hace pensar que nosotros estemos hechos, precisamente, de lo que llamamos materia inerte?

Pero el mundo inorgánico es sólo una parte del inmenso mundo molecular. El resto lo constituye el mundo orgánico, que es el de las moléculas que contienen carbono y otros átomos y del que quedan excluidos, por convenio y características especiales, los carbonatos, bicarbonatos y carburos metálicos, los cuales se incluyen en el mundo inorgánico.
Según decía en páginas anteriores, los quarks u y d se hallan en el seno de los nucleones (protones y neutrones) y, por tanto, en los núcleos atómicos. Hoy día, estos se consideran como una subclase de los hadrones.
La composición de los núcleos (lo que en Química se llama análisis cualitativo) es extraordinariamente sencilla ya que, como es sabido, constan de neutrones y protones que se pueden considerar como unidades que, dentro del núcleo, mantienen su identidad. Tal simplicidad cualitativa recuerda, por ejemplo, el caso de las series orgánicas, siendo la de los hidrocarburos saturados la más conocida. Recordad que su fórmula general es , lo que significa que una molécula de hidrocarburo contiene n átomos de carbono (símbolo C) y (2n+2) átomos de hidrógeno (símbolo H).
Protones y de neutrones determinan el elemento
El número de protones y neutrones determina al elemento, desde el hidrógeno (el más simple), al Uranio (el más complejo), siempre referido a elementos naturales que son 92, el resto, son artificiales, los conocidos transuránicos en cuyo grupo están el Einstenio o el Plutonio, artificiales todos ellos.
Los núcleos, como sistemas dinámicos de nucleones, pertenecen obviamente a la microfísica y, por consiguiente, para su descripción es necesario acudir a la mecánica cuántica. La materia, en general, aunque presumimos de conocerla, en realidad, nos queda mucho por aprender de ella.
Hablemos un poco de moléculas.

El papel primordial del agua en el metabolismo de los seres vivos se debe sus propiedades físicas y químicas, derivadas de la estructura molecular.
El número de especimenes atómicos es finito, existiendo ciertas razones para suponer que hacia el número atómico 173 los correspondientes núcleos serían inestables, no por razones intrínsecas de inestabilidad “radiactiva” nuclear, sino por razones relativistas. Ya antes me referiría a las especies atómicas, naturales y artificiales que son de unos pocos millares; en cambio; el número de moléculas conocidas hasta ahora comprende varios millones de especimenes, aumentando continuamente el número de ellas gracias a las síntesis que se llevan a cabo en numerosos laboratorios repartidos por todo el mundo.
Una molécula es una estructura, con individualidad propia, constituida por núcleos y electrones. Obviamente, en una molécula las interacciones deben tener lugar entre núcleos y electrones, núcleos y núcleos y electrones y electrones, siendo del tipo electromagnético.

Proteína supresora de tumores p53 encajada a una secuencia de ADN
Debido al confinamiento de los núcleos, el papel que desempeñan, aparte del de proporcionar la casi totalidad de la masa de la molécula, es poco relevante, a no ser que se trate de moléculas livianas, como la del hidrógeno. De una manera gráfica podríamos decir que los núcleos en una molécula constituyen el armazón de la misma, el esqueleto, cuya misión sería proporcionar el soporte del edificio. El papel más relevante lo proporcionan los electrones y en particular los llamados de valencia, que son los que de modo mayoritario intervienen en los enlaces, debido a que su energía es comparativamente inferior a la de los demás, lo que desempeña muy importante papel en la evolución.

Desde las moléculas más sencilla, como la del hidrógeno, con un total de 2 electrones, hasta las más complejas, como las de las proteínas, con muchos miles de ellos, existe toda una gama, según decía, de varios millones. Esta extraordinaria variedad de especies moleculares contrasta con la de las especies nucleares e incluso atómicas.
Sin entrar en las posibles diferencias interpretativas de estas notables divergencias, señalaré que, desde el punto de vista de la información, las especies moleculares la poseen en mucho mayor grado que los nucleares y atómicas.
Dejando aparte los núcleos, la información que soportan los átomos se podría atribuir a la distribución de su carga eléctrica, y en particular a la de los electrones más débilmente ligados. Concretando un poco se podría admitir que la citada información la soportan los orbitales atómicos, pues son precisamente estos orbitales las que introducen diferencias “geométricas” entre los diferentes electrones corticales.
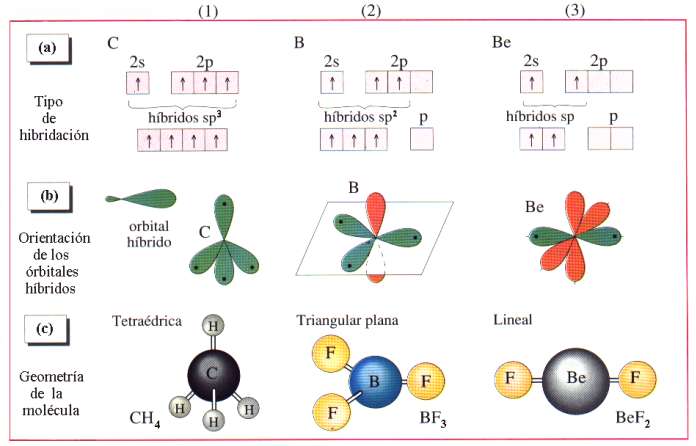
Justamente esa información es la que va a determinar las capacidades de unión de unos átomos con otros, previo el “reconocimiento” entre los orbitales correspondientes. De acuerdo con la mecánica cuántica el número de orbitales se reduce a unos pocos. Se individualizan por unas letras hablándose de orbitales, s, p, d, f, g, h. Este pequeño número nos proporciona una gran diversidad.
La llamada hibridación (una especie de mezcla) de orbitales es un modo de aumentar el número de mensajes, esto es, la información, bien entendido que esta hibridación ocurre en tanto y en cuanto dos átomos se preparan para enlazarse y formar una molécula. En las moléculas, la información, obviamente, debe de abarcar a todo el edificio, por lo que en principio parece que debería ser más rica que en los átomos. La ganancia de información equivale a una disminución de entropía; por esta razón, a la información se la llama también negantropía.
En términos electrónicos, la información se podría considerar proporcionada por un campo de densidad eléctrica, con valles, cimas, collados, etc., es decir, curvas isoelectrónicas, equivalentes formalmente a las de nivel en topografía. Parece razonable suponer que cuanto más diverso sean los átomos de una molécula, más rica y variada podrá ser su información, la información que pueda soportar.
La enorme variedad de formas, colores, comportamientos, etc., que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetravalencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.
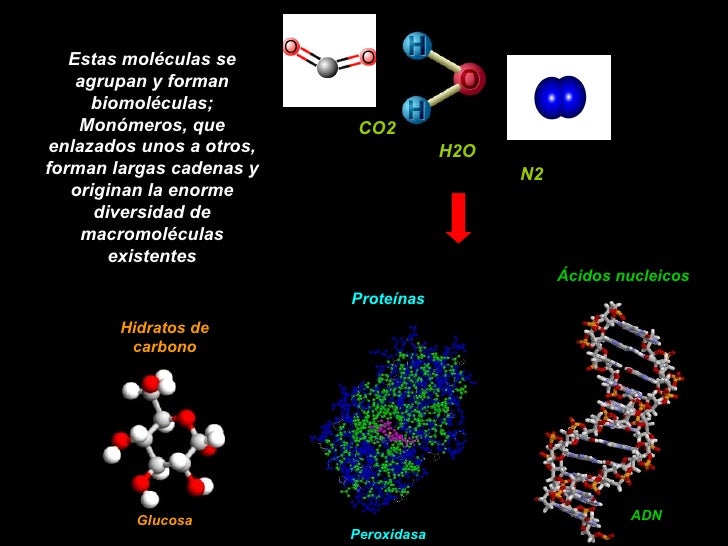
Estas moléculas se agrupan y forman biomoléculas; Monómeros, que enlazados unos a otros, forman largas cadenas y originan la enorme diversidad de macromoléculas existentes CO2 H2O N2 Hidratos de carbono Glucosa Peroxidasa.
El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor.
Refiriéndonos al silicio, que para nosotros es el más importante, señalaremos que las “moléculas” que dicho átomo forma con el oxígeno y otros átomos, generalmente metálicos, poseyendo gran nivel de información, difieren, en varios aspectos, de las moléculas orgánicas, es decir, de las que poseen un esqueleto de átomos de carbono.

El mundo de los silicatos es de una gran diversidad, existiendo centenares de especies minerológicas. Esas diferencias se refieren, fundamentalmente, a que el enlace químico en el caso de las moléculas orgánicas es covalente, y cuando se forma la sustancia correspondiente (cuatrillones de moléculas) o es un líquido, como es el caso de los aceites, o bien un sólido que funde fácilmente. Entre las moléculas que lo forman se ejercen unas fuerzas, llamadas de van der Waals, que, pueden considerarse como residuales de las fuerzas electromagnéticas, algo más débiles que éstas. En cambio, en los silicatos sólidos (como en el caso del topacio) el enlace covalente o iónico no se limita a una molécula, sino que se extiende en el espacio ocupado por el sólido, resultando un entramado particularmente fuerte.
Al igual que para los cristales de hielo, en la mayoría de los silicatos la información que soportan es pequeña, aunque conviene matizar este punto. Para un cristal ideal así sería en efecto, pero ocurre que en la realidad el cristal ideal es una abstracción, ya que en el cristal real existen aquí y allá los llamados defectos puntuales que trastocan la periodicidad espacial propia de las redes ideales. Precisamente esos defectos puntuales podían proporcionar una mayor información.

Las moléculas orgánicas con enlaces dobles ó triples tienen también formas características.
Si prescindimos de las orgánicas, el resto de las moléculas que resultan de la combinación entre los diferentes átomos no llega a 100.000, frente a los varios millones de las primeras. Resulta ranozable suponer que toda la enorme variedad de moléculas existentes, principalmente en los planetas rocosos, se haya formado por evolución de los átomos, como corresponde a un proceso evolutivo. La molécula poseería mayor orden que los átomos de donde procede, esto es, menor entropía. En su formación, el ambiente se habría desordenado al ganar entropía en una cierta cantidad tal, que arrojarse un balance total positivo.
No puedo, dejar pasar la oportunidad, aunque sea de pasada, remencionar las sustancias.
Tipos de energía que se almacena en moléculas orgánicas
Las así llamadas, son cuerpos formados por moléculas idénticas, entra las cuales pueden o no existir enlaces químicos. Veremos varios ejemplos. Las sustancias como el oxígeno, cloro, metano, amoníaco, etc., se presentan en estado gaseoso en condiciones ordinarias de presión y temperatura. Para su confinamiento se embotellan, aunque existen casos en que se encuentran mezcladas en el aire (os podéis dar una vueltecita por el Polo químico de Huelva).
En cualquier caso, un gas como los citados consiste en un enjambre de las moléculas correspondientes. Entre ellas no se ejercen fuerzas, salvo cuando colisionan, lo que hacen con una frecuencia que depende de la concentración, es decir, del número de ellas que están concentradas en la unidad de volumen; número que podemos calcular conociendo la presión y temperatura de la masa de gas confinada en un volumen conocido.

Decía que no existen fuerzas entre las moléculas de un gas. En realidad, es más exacto que el valor de esas fuerzas es insignificante porque las fuerzas residuales de las electromagnéticas, a las que antes me referí, disminuyen más rápidamente con la distancia que las fuerzas de Coulomb; y esta distancia es ordinariamente de varios diámetros moleculares.
Podemos conseguir que la intensidad de esas fuerzas aumente tratando de disminuir la distancia media entre las moléculas. Esto se puede lograr haciendo descender la temperatura, aumentando la presión o ambas cosas. Alcanzada una determinada temperatura, las moléculas comienzan a sentir las fuerzas de Van der Waals y aparece el estado líquido; si se sigue enfriando aparece el sólido. El orden crece desde el gas al líquido, siendo el sólido el más ordenado. Se trata de una red tridimensional en la que los nudos o vértices del entramado están ocupados por moléculas.
Todas las sustancias conocidas pueden presentarse en cualquiera de los tres estados de la materia (estados ordinarios y cotidianos en nuestras vidas del día a día).
Si las temperaturas reinantes, como decíamos en páginas anteriores, es de miles de millones de grados, el estado de la materia es el plasma, el material más común del Universo, el de las estrellas (aparte de la materia oscura, que no sabemos ni lo que es, ni donde está, ni que “estado” es el suyo).
En condiciones ordinarias de presión, la temperatura por debajo de la cual existe el líquido y/o sólido depende del tipo de sustancia. Se denomina temperatura de ebullición o fusión la que corresponde a los sucesivos equilibrios(a presión dada) de fases: vapor <-> líquido <-> sólido. Estas temperaturas son muy variadas. Por ejemplo, para los gases nobles son muy bajas; también para el oxígeno (O2) e hidrógeno (H2). En cambio, la mayoría de las sustancias son sólidos en condiciones ordinarias (grasas, ceras, etc.)
Las sustancias pueden ser simples y compuestas, según que la molécula correspondiente tenga átomos iguales o diferentes. El número de las primeras es enormemente inferior al de las segundas.

El concepto de molécula, como individuo-físico y químico, pierde su significado en ciertas sustancias que no hemos considerado aun. Entre ellas figuran las llamadas sales, el paradigma de las cuales es la sal de cocina. Se trata de cloruro de sodio, por lo que cualquier estudiante de E.G.B. escribiría sin titubear, su fórmula: Cl Na. Sin embargo, le podríamos poner en un aprieto si le preguntásemos donde se puede encontrar aisladamente individuos moleculares que respondan a esa composición. Le podemos orientar diciéndole que en el gas Cl H o en el vapor de agua existen moléculas como individualidades. En realidad y salvo casos especiales, por ejemplo, a temperaturas elevadas, no existen moléculas aisladas de sal, sino una especie de molécula gigante que se extiende por todo el cristal. Este edificio de cristal de sal consiste en una red o entramado, como un tablero de ajedrez de tres dimensiones, en cuyos nudos o vértices se encuentran, alternativamente, las constituyentes, que no son los átomos de Cl y Na sino los iones Cl– y Na+. El primero es un átomo de Cl que ha ganado un electrón, completándose todos los orbitales de valencia; el segundo, un átomo de Na que ha perdido el electrón del orbital s.

Cuando los átomos de Cl y Na interaccionan por aproximarse suficientemente sus nubes electrónicas, existe un reajuste de cargas, porque el núcleo de Cl atrae con más fuerza los electrones que el de Na, así uno pierde un electrón que gana el otro. El resultado es que, la colectividad de átomos se transforma en colectividad de iones, positivos los de Na y negativos los de Cl. Las fuerzas electromagnéticas entre esos iones determinan su ordenación en un cristal, el ClNa. Por consiguiente, en los nudos de la red existen, de manera alternativa, iones de Na e iones de Cl, resultando una red mucho más fuerte que en el caso de que las fuerzas actuantes fueran de Van der Waals. Por ello, las sales poseen puntos de fusión elevados en relación con los de las redes moleculares.
Hablemos de cuerpos.

Me referiré en primer lugar a los que constituyen nuestro entorno ordinario, que sería todo el entorno que abarca nuestro planeta. En segundo lugar considerare los demás cuerpos y objetos del Universo. El análisis de muestras de esos diversos cuerpos ha puesto de manifiesto que, en función de la composición, los cuerpos pueden ser simples y compuestos. Los primeros son, precisamente, los llamados elementos químicos, a las que el insigne Lavoisier (conocido como padre de la Química), consideró como el último término a que se llega mediante la aplicación del análisis químico.
Hoy sabemos que son colectividades de átomos isotópicos.
La mayoría de ellos son sólidos y se encuentran en la Naturaleza (nuestro entorno terráqueo) en estado libre o en combinación química con otros elementos, formando los diversos minerales.
La ordenación de los iones en las redes se manifiesta externamente en multitud de formas y colores. No obstante, debo señalar que, aun siendo abundante esta variedad, no es tan rica como la que corresponde a los cuerpos vivos, tanto animales como vegetales. La explicación se basa en que el número de especimenes moleculares y su complejidad son mucho mayores que en el reino inorgánico.
 Mandemos nuestra mejor energía
Mandemos nuestra mejor energía
.
#medioambiente #latierra #naturaleza #conexion #union #buenas #energias #terapiasnaturales #terapiasenergeticas #terapiamanual #reiki #hoponopono #masajemetamorfico #relajacion #meditacion #vida #divida #terapias #fluir #masajes #madrid #españa
Ago
12
Moléculas, sustancias, cuerpos…
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)
Es allí, en las estrellas, en sus hornos nucleares y en las explosiones de supernovas, donde a miles de millones de grados de temperatura, se crean los elementos más complejos que el hidrógeno y el helio. Aparece el litio, el carbono, el silicio o el nitrógeno y el hierro.

De estos materiales estamos nosotros hechos, y, lógicamente, se fabricaron en las estrellas.
En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es:
H, He, (Li, Be, B) C, N, O…… Fe
¿Apreciáis la maravilla? Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del Universo y…. de la vida inteligente.

El telescopio VLT (Very Large Telescope) de ESO ha obtenido imágenes de una fascinante región de formación de estrellas en la Gran Nube de Magallanes — una de las galaxias satélite de la Vía Láctea. Esta precisa imagen revela dos peculiares y brillantes nubes de gas: la rojiza NGC 2014 y su vecina azulada NGC 2020. Pese a que son muy diferentes, ambas fueron esculpidas por potentes vientos estelares procedentes de estrellas recién nacidas extremadamente calientes que también irradian el gas, provocando que brille de forma intensa. (para verla entera hay que pasar la rgla hacia la derehca).
Pero está claro que, todo el proceso estelar evolutivo inorgánico nos condujo desde el simple gas y polvo cósmico a la formación de estrellas y nebulosas solares hasta los planetas, la Tierra en particular, en cuyo medio ígneo describimos la formación de las estructuras de los silicatos, desplegándose con ello una enorme diversidad de composiciones, formas y colores, asistiéndose, por primera vez en la historia de la materia, a unas manifestaciones que contrastan con las que hemos mencionado en relación al proceso de las estrellas.
Desde el punto de vista del orden es la primera vez que nos encontramos con objetos de tamaño comparables al nuestro, en los que la ordenación de sus constituyentes es el rasgo más característico.

Al mismo tiempo nos ha parecido reconocer que esos objetos, es decir, sus redes cristalinas “reales”, almacenan información (memoria) que se nos muestra muy diversa y que puede cobrar interés en ciertos casos, como el de los microcristales de arcilla, en los que, según Cairos-Swith, puede incluso llegar a transmitirse.
Porque ¿qué sabemos en realidad de lo que llamamos materia inerte? Lo único que sabemos de ella son los datos referidos a sus condiciones físicas de dureza, composición, etc., en otros aspectos, ni sabemos si pueden existir otras propiedades distintas a las meramente-físicas.
¿No os hace pensar que nosotros estemos hechos, precisamente, de lo que llamamos materia inerte?

Pero el mundo inorgánico es sólo una parte del inmenso mundo molecular. El resto lo constituye el mundo orgánico, que es el de las moléculas que contienen carbono y otros átomos y del que quedan excluidos, por convenio y características especiales, los carbonatos, bicarbonatos y carburos metálicos, los cuales se incluyen en el mundo inorgánico.
Según decía en páginas anteriores, los quarks u y d se hallan en el seno de los nucleones (protones y neutrones) y, por tanto, en los núcleos atómicos. Hoy día, estos se consideran como una subclase de los hadrones.
La composición de los núcleos (lo que en Química se llama análisis cualitativo) es extraordinariamente sencilla ya que, como es sabido, constan de neutrones y protones que se pueden considerar como unidades que, dentro del núcleo, mantienen su identidad. Tal simplicidad cualitativa recuerda, por ejemplo, el caso de las series orgánicas, siendo la de los hidrocarburos saturados la más conocida. Recordad que su fórmula general es , lo que significa que una molécula de hidrocarburo contiene n átomos de carbono (símbolo C) y (2n+2) átomos de hidrógeno (símbolo H).
Protones y de neutrones determinan el elemento
El número de protones y neutrones determina al elemento, desde el hidrógeno (el más simple), al Uranio (el más complejo), siempre referido a elementos naturales que son 92, el resto, son artificiales, los conocidos transuránicos en cuyo grupo están el Einstenio o el Plutonio, artificiales todos ellos.
Los núcleos, como sistemas dinámicos de nucleones, pertenecen obviamente a la microfísica y, por consiguiente, para su descripción es necesario acudir a la mecánica cuántica. La materia, en general, aunque presumimos de conocerla, en realidad, nos queda mucho por aprender de ella.
Hablemos un poco de moléculas.

El papel primordial del agua en el metabolismo de los seres vivos se debe sus propiedades físicas y químicas, derivadas de la estructura molecular.
El número de especimenes atómicos es finito, existiendo ciertas razones para suponer que hacia el número atómico 173 los correspondientes núcleos serían inestables, no por razones intrínsecas de inestabilidad “radiactiva” nuclear, sino por razones relativistas. Ya antes me referiría a las especies atómicas, naturales y artificiales que son de unos pocos millares; en cambio; el número de moléculas conocidas hasta ahora comprende varios millones de especimenes, aumentando continuamente el número de ellas gracias a las síntesis que se llevan a cabo en numerosos laboratorios repartidos por todo el mundo.
Una molécula es una estructura, con individualidad propia, constituida por núcleos y electrones. Obviamente, en una molécula las interacciones deben tener lugar entre núcleos y electrones, núcleos y núcleos y electrones y electrones, siendo del tipo electromagnético.

Proteina supresora de tumores p53 encajada a una secuencia de ADN
Debido al confinamiento de los núcleos, el papel que desempeñan, aparte del de proporcionar la casi totalidad de la masa de la molécula, es poco relevante, a no ser que se trate de moléculas livianas, como la del hidrógeno. De una manera gráfica podríamos decir que los núcleos en una molécula constituyen el armazón de la misma, el esqueleto, cuya misión sería proporcionar el soporte del edificio. El papel más relevante lo proporcionan los electrones y en particular los llamados de valencia, que son los que de modo mayoritario intervienen en los enlaces, debido a que su energía es comparativamente inferior a la de los demás, lo que desempeña muy importante papel en la evolución.

Desde las moléculas más sencilla, como la del hidrógeno, con un total de 2 electrones, hasta las más complejas, como las de las proteínas, con muchos miles de ellos, existe toda una gama, según decía, de varios millones. Esta extraordinaria variedad de especies moleculares contrasta con la de las especies nucleares e incluso atómicas.
Sin entrar en las posibles diferencias interpretativas de estas notables divergencias, señalaré que, desde el punto de vista de la información, las especies moleculares la poseen en mucho mayor grado que los nucleares y atómicas.
Dejando aparte los núcleos, la información que soportan los átomos se podría atribuir a la distribución de su carga eléctrica, y en particular a la de los electrones más débilmente ligados. Concretando un poco se podría admitir que la citada información la soportan los orbitales atómicos, pues son precisamente estos orbitales las que introducen diferencias “geométricas” entre los diferentes electrones corticales.

Justamente esa información es la que va a determinar las capacidades de unión de unos átomos con otros, previo el “reconocimiento” entre los orbitales correspondientes. De acuerdo con la mecánica cuántica el número de orbitales se reduce a unos pocos. Se individualizan por unas letras hablándose de orbitales, s, p, d, f, g, h. Este pequeño número nos proporciona una gran diversidad.
La llamada hibridación (una especie de mezcla) de orbitales es un modo de aumentar el número de mensajes, esto es, la información, bien entendido que esta hibridación ocurre en tanto y en cuanto dos átomos se preparan para enlazarse y formar una molécula. En las moléculas, la información, obviamente, debe de abarcar a todo el edificio, por lo que en principio parece que debería ser más rica que en los átomos. La ganancia de información equivale a una disminución de entropía; por esta razón, a la información se la llama también negantropía.

En términos electrónicos, la información se podría considerar proporcionada por un campo de densidad eléctrica, con valles, cimas, collados, etc., es decir, curvas isoelectrónicas, equivalentes formalmente a las de nivel en topografía. Parece razonable suponer que cuanto más diverso sean los átomos de una molécula, más rica y variada podrá ser su información, la información que pueda soportar.
La enorme variedad de formas, colores, comportamientos, etc., que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetravalencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.

Estas moléculas se agrupan y forman biomoléculas; Monómeros, que enlazados unos a otros, forman largas cadenas y originan la enorme diversidad de macromoléculas existentes CO2 H2O N2 Hidratos de carbono Glucosa Peroxidasa.
El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor.
Refiriéndonos al silicio, que para nosotros es el más importante, señalaremos que las “moléculas” que dicho átomo forma con el oxígeno y otros átomos, generalmente metálicos, poseyendo gran nivel de información, difieren, en varios aspectos, de las moléculas orgánicas, es decir, de las que poseen un esqueleto de átomos de carbono.

El mundo de los silicatos es de una gran diversidad, existiendo centenares de especies minerológicas. Esas diferencias se refieren, fundamentalmente, a que el enlace químico en el caso de las moléculas orgánicas es covalente, y cuando se forma la sustancia correspondiente (cuatrillones de moléculas) o es un líquido, como es el caso de los aceites, o bien un sólido que funde fácilmente. Entre las moléculas que lo forman se ejercen unas fuerzas, llamadas de van der Waals, que, pueden considerarse como residuales de las fuerzas electromagnéticas, algo más débiles que éstas. En cambio, en los silicatos sólidos (como en el caso del topacio) el enlace covalente o iónico no se limita a una molécula, sino que se extiende en el espacio ocupado por el sólido, resultando un entramado particularmente fuerte.
Al igual que para los cristales de hielo, en la mayoría de los silicatos la información que soportan es pequeña, aunque conviene matizar este punto. Para un cristal ideal así sería en efecto, pero ocurre que en la realidad el cristal ideal es una abstracción, ya que en el cristal real existen aquí y allá los llamados defectos puntuales que trastocan la periodicidad espacial propia de las redes ideales. Precisamente esos defectos puntuales podían proporcionar una mayor información.

Las moléculas orgánicas con enlaces dobles ó triples tienen también formas características.
Si prescindimos de las orgánicas, el resto de las moléculas que resultan de la combinación entre los diferentes átomos no llega a 100.000, frente a los varios millones de las primeras. Resulta ranozable suponer que toda la enorme variedad de moléculas existentes, principalmente en los planetas rocosos, se haya formado por evolución de los átomos, como corresponde a un proceso evolutivo. La molécula poseería mayor orden que los átomos de donde procede, esto es, menor entropía. En su formación, el ambiente se habría desordenado al ganar entropía en una cierta cantidad tal, que arrojarse un balance total positivo.
No puedo, dejar pasar la oportunidad, aunque sea de pasada, remencionar las sustancias.
Tipos de energía que se almacena en moléculas orgánicas
Las así llamadas, son cuerpos formados por moléculas idénticas, entra las cuales pueden o no existir enlaces químicos. Veremos varios ejemplos. Las sustancias como el oxígeno, cloro, metano, amoníaco, etc., se presentan en estado gaseoso en condiciones ordinarias de presión y temperatura. Para su confinamiento se embotellan, aunque existen casos en que se encuentran mezcladas en el aire (os podéis dar una vueltecita por el Polo químico de Huelva).
En cualquier caso, un gas como los citados consiste en un enjambre de las moléculas correspondientes. Entre ellas no se ejercen fuerzas, salvo cuando colisionan, lo que hacen con una frecuencia que depende de la concentración, es decir, del número de ellas que están concentradas en la unidad de volumen; número que podemos calcular conociendo la presión y temperatura de la masa de gas confinada en un volumen conocido.

Decía que no existen fuerzas entre las moléculas de un gas. En realidad, es más exacto que el valor de esas fuerzas es insignificante porque las fuerzas residuales de las electromagnéticas, a las que antes me referí, disminuyen más rápidamente con la distancia que las fuerzas de Coulomb; y esta distancia es ordinariamente de varios diámetros moleculares.
Podemos conseguir que la intensidad de esas fuerzas aumente tratando de disminuir la distancia media entre las moléculas. Esto se puede lograr haciendo descender la temperatura, aumentando la presión o ambas cosas. Alcanzada una determinada temperatura, las moléculas comienzan a sentir las fuerzas de Van der Waals y aparece el estado líquido; si se sigue enfriando aparece el sólido. El orden crece desde el gas al líquido, siendo el sólido el más ordenado. Se trata de una red tridimensional en la que los nudos o vértices del entramado están ocupados por moléculas.
Todas las sustancias conocidas pueden presentarse en cualquiera de los tres estados de la materia (estados ordinarios y cotidianos en nuestras vidas del día a día).
Si las temperaturas reinantes, como decíamos en páginas anteriores, es de miles de millones de grados, el estado de la materia es el plasma, el material más común del Universo, el de las estrellas (aparte de la materia oscura, que no sabemos ni lo que es, ni donde está, ni que “estado” es el suyo).
En condiciones ordinarias de presión, la temperatura por debajo de la cual existe el líquido y/o sólido depende del tipo de sustancia. Se denomina temperatura de ebullición o fusión la que corresponde a los sucesivos equilibrios(a presión dada) de fases: vapor <-> líquido <-> sólido. Estas temperaturas son muy variadas. Por ejemplo, para los gases nobles son muy bajas; también para el oxígeno (O2) e hidrógeno (H2). En cambio, la mayoría de las sustancias son sólidos en condiciones ordinarias (grasas, ceras, etc.)
Las sustancias pueden ser simples y compuestas, según que la molécula correspondiente tenga átomos iguales o diferentes. El número de las primeras es enormemente inferior al de las segundas.

El concepto de molécula, como individuo-físico y químico, pierde su significado en ciertas sustancias que no hemos considerado aun. Entre ellas figuran las llamadas sales, el paradigma de las cuales es la sal de cocina. Se trata de cloruro de sodio, por lo que cualquier estudiante de E.G.B. escribiría sin titubear, su fórmula: Cl Na. Sin embargo, le podríamos poner en un aprieto si le preguntásemos donde se puede encontrar aisladamente individuos moleculares que respondan a esa composición. Le podemos orientar diciéndole que en el gas Cl H o en el vapor de agua existen moléculas como individualidades. En realidad y salvo casos especiales, por ejemplo, a temperaturas elevadas, no existen moléculas aisladas de sal, sino una especie de molécula gigante que se extiende por todo el cristal. Este edificio de cristal de sal consiste en una red o entramado, como un tablero de ajedrez de tres dimensiones, en cuyos nudos o vértices se encuentran, alternativamente, las constituyentes, que no son los átomos de Cl y Na sino los iones Cl– y Na+. El primero es un átomo de Cl que ha ganado un electrón, completándose todos los orbitales de valencia; el segundo, un átomo de Na que ha perdido el electrón del orbital s.

Cuando los átomos de Cl y Na interaccionan por aproximarse suficientemente sus nubes electrónicas, existe un reajuste de cargas, porque el núcleo de Cl atrae con más fuerza los electrones que el de Na, así uno pierde un electrón que gana el otro. El resultado es que, la colectividad de átomos se transforma en colectividad de iones, positivos los de Na y negativos los de Cl. Las fuerzas electromagnéticas entre esos iones determinan su ordenación en un cristal, el ClNa. Por consiguiente, en los nudos de la red existen, de manera alternativa, iones de Na e iones de Cl, resultando una red mucho más fuerte que en el caso de que las fuerzas actuantes fueran de Van der Waals. Por ello, las sales poseen puntos de fusión elevados en relación con los de las redes moleculares.
Hablemos de cuerpos.

Me referiré en primer lugar a los que constituyen nuestro entorno ordinario, que sería todo el entorno que abarca nuestro planeta. En segundo lugar considerare los demás cuerpos y objetos del Universo. El análisis de muestras de esos diversos cuerpos ha puesto de manifiesto que, en función de la composición, los cuerpos pueden ser simples y compuestos. Los primeros son, precisamente, los llamados elementos químicos, a las que el insigne Lavoisier (conocido como padre de la Química), consideró como el último término a que se llega mediante la aplicación del análisis químico.

Hoy sabemos que son colectividades de átomos isotópicos.
La mayoría de ellos son sólidos y se encuentran en la Naturaleza (nuestro entorno terráqueo) en estado libre o en combinación química con otros elementos, formando los diversos minerales.
La ordenación de los iones en las redes se manifiesta externamente en multitud de formas y colores. No obstante, debo señalar que, aun siendo abundante esta variedad, no es tan rica como la que corresponde a los cuerpos vivos, tanto animales como vegetales. La explicación se basa en que el número de especimenes moleculares y su complejidad son mucho mayores que en el reino inorgánico.
Sería conveniente, salir al paso de una posible interpretación errónea. Me refiero a que pudiera pensarse que los reinos que acabamos de mencionar constituyen clases disyuntas, esto es, sin conexión mutua. Y no lo digo porque esté considerando el hecho de que el carbono forma compuestos inorgánicos y orgánicos (lo que también hace el silicio), sino porque haya existido, y aún pueda existir, una conclusión, mejor conexión evolutiva del mundo inorgánico y el viviente que no se puede descartar, de hecho, yo particularmente, estoy seguro de ello. Estamos totalmente conectados con los ríos, las montañas y los valles, con la tierra que pisamos, el aire que respiramos y con todo el resto del Universo del que formamos parte.

La teoría de Cairos Swith considera que el eslabón entre ambos mundos se halla localizado en los microcristales de arcilla. Mi teoría particular es que no hay eslabón perdido en dicha conexión, sino que es el tiempo el que pone, en cada momento, una u otra materia en uno u otro lugar. Ahora, nos ha tocado estar aquí como ser complejo, pensante y sensitivo. El eón que viene nos puede colocar formando parte de un enorme árbol, de un monte, o, simplemente estar reposando como fina arena en el lecho de un río. Sin dudarlo, J. M. y P. formarán parte de un hermoso jardín perfumado y lleno de aromas que la brisa regalará a los que pasen cerca de allí.
El granito, por ejemplo, consiste básicamente en una mezcla de tres cuerpos compuestos: cuarzo, mica y feldespato. ¿Quién puede decir hoy lo que seremos mañana?

En todos los cuerpos que hemos estado considerando hasta ahora, las moléculas, los átomos o los iones se hallan situados en los nudos de la correspondiente red, así que, los electrones de esos individuos se encuentran también localizados en el entorno inmediato de esos lugares. Podríamos decir que la densidad electrónica es una función periódica espacial, lo que significa que al recorrer la red siguiendo una determinada dirección irían apareciendo altibajos, es decir, crestas y valles de la densidad electrónica.
La estructura de los cuerpos metálicos, así como las aleaciones, merecen una consideración especial. La estructura de los metales y aleaciones difiere de la de los demás cuerpos en un aspecto muy importante que consideraré a continuación.

Supongamos, para fijar las ideas, que tenemos un trozo de plata metálica pura. En los nudos de la red correspondientes los átomos han perdido su electrón de …
Me refiero a que en los cuerpos metálicos existe una deslocalización de los electrones que están menos fuertemente enlazados en los correspondientes núcleos, es decir, de los electrones de valencia.
Vamos a precisar un poco. Supongamos, para fijar las ideas, que tenemos un trozo de plata metálica pura. En los nudos de la red correspondientes los átomos han perdido su electrón de valencia, pero ocurre que cada uno de estos electrones forma una colectividad que se halla desparramada o dispersa por todo el sólido. Una primera imagen de esta situación fue establecida por el gran físico italiano Enrico Fermi, por lo que se habla de un gas electrónico, llamado también de Fermi, que llenaría los espacios libres, es decir, no ocupados por los iones metálicos.
Este gas electrónico es el responsable de las propiedades metálicas, tales como el brillo, conductibilidades eléctrica y térmica, etc. La aplicación de la mecánica cuántica a la descripción del estado metálico conduce a la obtención del mapa de la densidad electrónica, o, como decía antes, a las características de la información correspondiente.
Sin entrar en detalles que desviarían nuestra atención hacia otros conceptos fuera de los límites de lo que ahora estoy pretendiendo, utilizaré el mismo lenguaje que para las estructuras de núcleos y átomos.

Recordemos que en la sociedad de los nucleones y electrones existen las relaciones verticales y las de estratificación, que se manifiestan en las capas y subcapas. En el caso de los metales tendríamos una colectividad de núcleos, arropados con sus capas cerradas, ocupando los nudos de la red; únicamente los electrones de valencia de cada átomo forman la colectividad del gas electrónico.
La pregunta que nos debemos hacer es: ¿estos electrones, en número igual, por lo menos, al de los átomos, se hallan estratificados? La respuesta es que sí. Existe una estratificación de estos electrones en las llamadas bandas. El concepto de banda energética resulta de la consideración simultánea de dos aspectos: la cuantización energética (o la estratificación de los niveles energéticos en los átomos) y el grandísimo número de electrones existentes. Este colectivo no podría ubicarse en un número finito y escaso de niveles. Esta dificultad queda soslayada si se admite que cada uno de esos niveles atómicos de los N átomos que forman el cuerpo se funde en otros tantos niveles de cierta anchura donde ya pueden alojarse los electrones disponibles.

Esa fusión de los niveles atómicos da lugar a las bandas. Esta imagen equivaldría a considerar un metal como un átomo gigante en el que los niveles energéticos poseyeran una anchura finita.
En cuanto a la información que puede soportar un metal, podríamos señalar que sería parecida a la del correspondiente átomo, pero mucha más extendida espacialmente. Una información puntual, la del átomo, daría paso a otra espacial, si bien vendría a ser una mera repetición periódica de aquella.
¿Y los cuerpos que pueblan el resto del Universo?
Cuando un cuerpo sobrepasa unas determinadas dimensiones, aparece algo que conocemos como fuerza gravitatoria y que se deja sentir en la forma que todos conocemos y, que da lugar, primeramente a la fusión de los diversos materiales que forman los cuerpos.
Así, por ejemplo, en el cuerpo que llamamos Tierra, la presión crece con la profundidad, por lo que, a partir de un determinado valor de ésta, aparece el estado líquido y con él una estratificación que trata de establecer el equilibrio hidrostático.
Dentro de nuestro sistema planetario se distinguen los planetas rocosos, hasta Marte y meteoritos inclusive, y el resto de ellos, desde Júpiter en adelante, incluido este. Estos últimos difieren esencialmente de los primeros en su composición. Recuérdese que la de Júpiter es mucho más simple que la de los planetas rocosos. Consta fundamentalmente de hidrógeno, helio, agua, amoniaco y metano, con un núcleo rocoso en su interior. El hidrógeno que rodea a este núcleo se encuentra en forma de hidrógeno atómico sólido.

También la composición del Sol (y todas las estrellas que brillan) es más simple que la de los planetas rocosos, su estado físico es el de plasma y su contenido está reducido (mayormente) a hidrógeno y helio. Mas variedad de materiales existe en las estrellas supernovas, donde el primitivo hidrógeno ha evolucionado de la manera que expliqué en otra parte de este trabajo.
En cuanto a los derechos de la evolución estelar, enanas blancas, estrellas de neutrones y agujeros negros, señalaré que la composición de la primera es sencilla en cuanto al numero de “elementos” constituyentes; la segunda ya lo indica su propio nombre, constan de nucleones, particularmente neutrones que están fuertemente empaquetados (muy juntos) por la gravedad. Una estrella de neutrones puede tener una densidad superior a la del agua, en millones de veces y del mismo orden que la de los núcleos atómicos. El agujero negro, es un fenómeno aparte, su inmensa fuerza gravitatoria es tal que, ni la luz puede escapar de ella, es decir, su velocidad de escape es superior a 300.000 km/s, y, como según la relatividad, nada es en nuestro Universo, superior en velocidad, a la luz, resulta que nada podrá escapar de un agujero negro.
Allí dentro, en el interior del agujero negro, no existen ni el tiempo ni el espacio, es como un objeto que estando en nuestro Universo (deja sentir su fuerza gravitatoria y engulle estrellas), al mismo tiempo, no está aquí. Son muchas las cosas que aún nos queda por dedcubrir.
emilio silvera
















 Totales: 75.283.684
Totales: 75.283.684 Conectados: 36
Conectados: 36