Oct
4
La Naturaleza y sus secretos que tratamos de desvelar
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (1)
Comments (1)

No, el Universo no es infinito pero… ¡Nos lo parece!

Hay que prestar atención a las coincidencias. Uno de los aspectos más sorprendentes en el estudio del Universo astronómico durante el siglo xx ha sido el papel desempeñado por la coincidencia: que existiera, que fuera despreciada y que fuera reconocida. Cuando los físicos empezaron a apreciar el papel de los constantes en el dominio cuántico y a explorar y explotar la nueva teoría de la Gravedad de Einstein para describir el Universo en conjunto, las circunstancias eran las adecuadas para que alguien tratara de unirlas.

En este “océano” de materia en el que están fraguándose el nacimiento de miles de estrellas y de mundos… ¿Qué moléculas y materiales estarán presentes? No es coincidencia de que en todas las Nebulosas ocurran los mismos procesos y esté presente una fuerte radiación que ioniza el material que circunda a las estrellas jóvenes masivas.
Entró en escena Arthur Eddington: un extraordinario científico que había sido el primero en descubrir cómo se alimentaban las estrellas a partir de reacciones nucleares. También hizo importantes contribuciones a nuestra comprensión de la galaxia, escribió la primera exposición sistemática de la teoría de la relatividad general de Einstein y fue el responsable de revificar, en una prueba decisiva, durante un eclipse de Sol, la veracidad de la teoría de Einstein en cuanto a que el campo gravitatorio del Sol debería desviar la luz estelar que venía hacia la Tierra en aproximadamente 1,75 segundos de arco cuando pasaba cerca de la superficie solar, y así resulto.
Einstein y Eddington en el jardín de la casa de éste último
Albert Einstein y Arthur Stanley Eddington, se conocieron y se hicieron amigos. Se conservan fotos de los dos juntos conversando sentados en un banco del jardín de Eddington en el año 1.939, don se fueron fotografiados por la hermana del dueño de la casa.
 Aunque Eddington era un hombre tímido con pocas dotes para hablar en público, sabía escribir de forma muy bella, y sus metáforas y analogías aún las utilizan los astrónomos que buscan explicaciones gráficas a ideas complicadas.
Aunque Eddington era un hombre tímido con pocas dotes para hablar en público, sabía escribir de forma muy bella, y sus metáforas y analogías aún las utilizan los astrónomos que buscan explicaciones gráficas a ideas complicadas.

En este mar de materiales relucientes por la radiación se forman increíbles imágenes y figuras arabescas impulsadas por los pinceles de los vientos estelares que empujan con fuerza esas “montañas” de gas y polvo hasta llevarlas hacia otras regiones donde, ayudadas por la Gravedad, se conforman en grumos que van creciendo para, finalmente, convertirse en proto-estrellas que, mucho tiempo más tarde, comienzan a brillar ¡ha nacido una estrella!
Eddington creía que a partir del pensamiento puro sería posible deducir leyes y constantes de la Naturaleza y predecir la existencia en el Universo de cosas como estrellas y Galaxias. ¡Se está saliendo con la suya! Entre los números de Eddington que él consideraba importante y que se denomino “numero de Eddington” (1079), que es igual al número de protones del Universo visible. Eddington calculó (a mano) este número enorme y de enorme precisión en un crucero trasatlántico (ya lo he contado otras veces), concluyendo con esta memorable afirmación:

“Creo que en el Universo hay
15.747.724.136.275.002.577.605.653.968.181.555.468.044.717.914.527.116.709.366.231.425.076.185.631.031.296 de protones y el mismo número de electrones.”
Este número enorme, normalmente escrito NEdd, es aproximadamente igual a 1080. Lo que atrajo la atención de Eddington hacia él era el hecho de que debe ser un número entero, y por eso en principio puede ser calculado exactamente. En el Universo existen grandes números que lo definen y la Ciencia ha sabido dar con ellos para poder comprender mejor.
Durante la década de 1.920, cuándo Eddington empezó su búsqueda para explicar las constantes de la Naturaleza, no se conocían bien las fuerzas débil y fuerte de la Naturaleza, y las únicas constantes dimensionales de la física que sí se conocían e interpretaban con confianza eran las que definían la Gravedad y las fuerzas electromagnéticas.
“El Número adimensional es un número que no tiene unidades físicas que lo definan y por lo tanto es un número puro. Los números adimensionales se definen como productos o cocientes de cantidades que sí tienen unidades de tal forma que todas éstas se simplifican. Dependiendo de su valor estos números tiene un significado físico que caracteriza unas determinadas propiedades para algunos sistemas.”
Eddington las dispuso en tres grupos o tres puros números adimensionales. Utilizando los valores experimentales de la época, tomó la razón entre las masas del protón y electrón:
mpr/me ≈ 1840
la inversa de la constante de estructura fina:
2phc/e2≈ 137
Y la razón entre la fuerza gravitatoria y la fuerza electromagnética entre un electrón y un protón;
22/Gmpr me ≈1040
A estas añadió su número cosmológico:
N Edd ≈ 1080
A estos cuatro números los llamó “las constantes últimas”, y la explicación de sus valores era el mayor desafió de la ciencia teórica: ¿Son estas cuatro constantes irreducibles, o una unificación posterior de la Física demostrará que alguna o todas ellas pueden ser prescindibles ? ¿Podrían haber sido diferentes de lo que realmente son?
De momento con certeza, nadie ha podido contestar a estas dos preguntas que, como tantas otras, están a la espera de esa Gran teoría Unificada del Todo que, por fín, nos brinde las respuestas tan esperadas y buscadas por todos los grandes físicos del mundo.

Según parece, el Tiempo que afecta a la vida de los seres vivos y de las cosas compuestas de materia -nada permanece y todo cambia-, están situadas en un plano distinto al que ocupan esas otras “cosas” que llamamos ¡constantes universales! y que son, las responsables de que nuestro mundo, nuestro universo, sea como es. Son aquellos parámetros que no cambian a lo largo del universo: La carga del electrón, la masa del protón, la velocidad de la luz en el vacío, la constante de Planck, la constante gravitacional y también la magnética, o, la constante de estructura fina. Se piensa que son todas ellas ejemplos de constantes fundamentales de la Naturaleza.
Poco a poco, los científicos llegaron a apreciar el misterio de la regularidad y lo predecible del mundo. Pese a la concatenación de movimientos caóticos e impredecibles de átomos y moléculas, nuestra experiencia cotidiana es la de un mundo que posee una profunda consistencia y continuidad. Nuestra búsqueda de la fuente de dicha consistencia atendía primero a las leyes de la Naturaleza que son las que gobiernan como cambian las cosas. Sin embargo, y al mismo tiempo, hemos llegado a identificar una colección de números misteriosos arraigados en la regularidad de la apariencia. Son las Constantes de la Naturaleza que, como las que antes hemos relacionado dan al Universo un carácter distintivo y lo singulariza de otros que podríamos imaginar. Todo esto, unifica de una vez nuestro máximo conocimiento y también, nuestra infinita ignorancia.


La fuerza de la Gravedad es una constante que se deja notar
¡Es todo tan complejo! ¡Sabemos tan poco!
¿Acaso es sencillo y no sabemos verlo? Seguramente, un poco de ambas cosas. Pudiera ser que, ni todo sea tan complejo y que, nuestras mentes, aún no están preparadas para ver la simple belleza que subyace en todas las cosas del Universo, de la Naturaleza que, cuando al fin las podemos comprender, a veces, incluso nos sorprendemos de la sencillez con la que el “mundo” se expresa. Una cosa es segura, la verdad está ahí, esperándonos.
Por ejemplo: Los campos magnéticos están presentes por todo el Universo. Hasta un diminuto (no por ello menos importante) electrón crea, con su oscilación, su propio campo magnético, y, aunque pequeño, se le supone un tamaño no nulo con un radio ro, llamado el radio clásico del electrón, dado por r0 = e2/(mc2) = 2,82 x 10-13 cm, donde e y m son la carga y la masa, respectivamente del electrón y c es la velocidad de la luz. Pudimos llegar a discernir eso y mucho más haciendo que la comprensión se abriera paso en nuestras mentes que, no por ello, dejaron de teorizar y de imaginar como sería el Universo y las reglas que lo rigen.
“La creciente distancia entre la imaginación del mundo físico y el mundo de los sentidos no significa otra cosa que una aproximación progresiva al mundo real.”
El mundo que nosotros percibimos es “nuestro mundo”, el verdadero es diferente, y, como nos dice Planck en la oración entrecomillada arriba, cada vez estamos más cerca de la realidad, a la que, aunque no nos pueden llevar nuestros sentidos, si no llevarán la intuición, la imaginación y el intelecto.
Está claro que la existencia de unas constantes de la Naturaleza nos dice que sí, que existe una realidad física completamente diferente a las realidades que la Mente Humana pueda imaginar. La existencia de esas constantes inmutables dejan en mal lugar a los filósofos positivistas que nos presentan la ciencia como una construcción enteramente humana: puntos precisos organizados de una forma conveniente por una teoría que con el tiempo será reemplazada por otra mejor, más precisa. Claro que, tales pensamientos quedan fuera de lugar cuando sabemos por haberlo descubierto que las constantes de la naturaleza han surgido sin que nosotros las hallamos invitado y ellas se muestran como entidades naturales que no han sido escogidas por conveniencia humana.

Físicos de la University of New Wales (UNSW) tienen una teoría cuando menos controvertida, y es la de que la constante de estructura fina, α (alpha), en realidad no es constante. Y estudian los alrededores de una enana blanca lejana, con una gravedad más de 30.000 veces mayor que la de la tierra, para comprobar su hipótesis.
En 1999 un equipo de físicos anunció la detección de variaciones en el valor de α. Ahora, otro grupo de la misma universidad están usando el Telescopio Espacial Hubble para observar una enana blanca con el objeto de medir α con gran precisión. El argumento es que se cree que los exóticos campos de energía escalar podrían alterar el valor de α en lugares donde existe un intenso campo gravitatorio. Estos campos de energía escalar son campos que aparecen en teorías que combinan el Modelo Estándar de la Fisica de Partículas, con la Teoría de la Relatividad General de Einstein.

Todos los procesos de la Naturaleza, requieren su tiempo. Todo pasa cuando tiene que pasar. Esta escala temporal está controlada por el hecho de que las constantes fundamentales de la naturaleza sean:
t(estrellas) ≈ (Gmp2 / hc)-1 h/mpc2 ≈ 1040 ×10-23 segundos ≈ 10.000 millones de años.
No esperaríamos estar observando el universo en tiempos significativamente mayores que t(estrellas), puesto que todas las estrellas estables se habrían expandido, enfriado y muerto. Tampoco seríamos capaces de ver el universo en tiempos mucho menores que t(estrellas) porque no podríamos existir; no había estrellas ni elementos pesados como el carbono. Parece que estamos amarrados por los hechos de la vida biológica para mirar el universo y desarrollar teorías cosmológicas una vez que haya transcurrido un tiempo t(estrellas) desde el Big Bang.

Porque eso es así es por lo que tenemos que pensar que posibles civilizaciones extraterrestres presentes en otros mundos, habrán llegado aquí (al universo), casi al mismo tiempo que nosotros y, seguramente, sus recorridos serán los mismos o muy parecidos a los nuestros desde que pudieron surgir a partir de la “materia inerte” y evolucionar para generar pensamientos adquiriendo la consciencia de Ser.
En la imagen de arriba de una Nebulosa planetaria, contemplamos la escena de una estrella moribunda que fue necesaria para que, los materiales biológicos que nos conformaron a los seres vivos, pudieran estar presentes en el Universo. Sin ese tiempo de t(estrellas) = a 10.000 millones de años, difícilmente podríamos estar ahora aquí tratando de estos temas.
Rodo esto ¿No desata tu imaginación?
Emilio Silvera V.
Oct
4
¿Un detalle insignificante? Pero podría cambiar el curso del Mundo
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (1)
Comments (1)
Edwin Schrödinger, autor de la ecuación con su función de onda, se disgustó con algunas de las interpretaciones de su ecuación. Para demostrar lo absurdo de la situación creada, Schrödinger colocó un gato imaginario en una caja cerrada. El gato estaba frente a un recipiente con veneno que al dejarlo salir se volatilizaba en gas mortífero, Un cuadrado de plomo podía caer y romper el recipiente al ser soltado por un mecanismo sensible conectado a un fragmento de uranio. El átomo de uranio es inestable y sufrirá una desintegración radiactiva. Si se desintegra un núcleo de uranio, será detectado por el contador Geiger que entonces soltaba pa pieza de plomo sobre el recipiente de cristal que dejaba salir el gas que matará al gato.

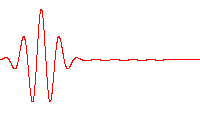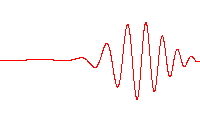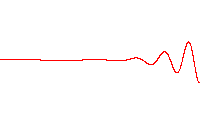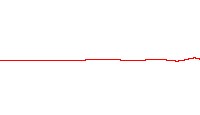
donde i es la unidad imaginaria, ħ es la «constante de Planck reducida» o «constante de Dirac» (constante de Planck dividida por 2π), el símbolo ∂∂t indica una derivada parcial con respecto al tiempo t, Ψ (la letra griega psi) es la función de onda del sistema cuántico, y Ĥ es el operador Hamiltoniano (el cual caracteriza la energía total de cualquier función de onda dada y tiene diferentes formas que dependen de la situación).
Una función de onda que satisface la ecuación no relativista de Schrödinger con V = 0. Es decir, corresponde a una partícula viajando libremente a través del espacio libre. Este gráfico es la parte real de la función de onda.”
Función de onda para una partícula bidimensional encerrada en una caja. Las líneas de nivel sobre el plano inferior están relacionadas con la probabilidad de presencia.”
Cada una de las tres filas es una función de onda que satisfacen la ecuación de Schrödinger dependiente del tiempo para un oscilador armónico cuántico. A la izquierda: La parte real (azul) y la parte imaginaria (rojo) de la función de onda. A la derecha: La distribución de probabilidad de hallar una partícula con esta función de onda en una posición determinada. Las dos filas de arriba son ejemplos de estados estacionarios, que corresponden a ondas estacionarias. La fila de abajo es un ejemplo de un estado que no es estacionario. La columna de la derecha ilustra por qué el estado puede llamarse “estacionario”.
Sep
27
¡La Mecánica Cuántica! con sus insondables secretos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física, Física Cuántica ~
Clasificado en Física, Física Cuántica ~
 Comments (22)
Comments (22)
Werner Heisenberg
Sí, el principio cuántico es muy extraño. Cuando en 1927, el joven físico alemán Werner Heisenberg llegó al Principio de Indeterminación, la física moderno rompió de manera decisiva con la física clásica, una nueva Era comenzaba con otra manera de mirar el mundo que nos rodea a través de la Física. Heisenberg descubrió que se puede conocer, o bien la posición exacta de una partícula determinada, o bien su trayectoria exacta, pero no ambas.
Sep
23
Los Quarks invisibles
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física Cuántica ~
Clasificado en Física Cuántica ~
 Comments (0)
Comments (0)
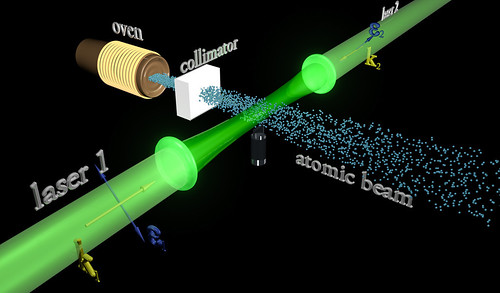
Una vez que se ha puesto orden entre las numerosas especies de partículas, se puede reconocer una pauta. Igual que Dimitri Ivanovich Mendeleev descubrió el sistema periódico de los elementos químicos en 1869, así también se hizo visible un sistema similar para las partículas. Esta pauta la encontraron independientemente el americano Murray Gell-Mann y el israelí Yuval Ne’eman. Ocho especies de mesones, todos con el mismo espín, u ocho especies de bariones, con el mismo espín, se podían reagrupar perfectamente en grupos que llamaremos multipletes. El esquema matemático correspondiente se llama SU(3). Grupletes de ocho elementos forman un octete “fundamental”. Por esta razón Gell-Mann llamó a esta teoría el “óctuplo camino”. Lo tomó prestado del budismo de acuerdo con el cual el camino hacia el nirvana es el camino óctuplo.
Pero las matemáticas SU(3) también admiten multipletes de diez miembros. Cuando se propuso este esquema se conocían nueve bariones con espín 3/2. Los esquemas SU(3) se obtienen al representar dos propiedades fundamentales de las partículas, la extrañeza S frente al iso-espín I₃ , en una gráfica.

La cámara de burbujas es un detector de partículas cargadas eléctricamente. La cámara la compone una cuba que contiene un fluido transparente, generalmente hidrógeno líquido, que está a una temperatura algo más baja que su temperatura de ebullición. Una partícula cargada deposita la energía necesaria para que el líquido comience a hervir a lo largo de su trayectoria, formando una línea de burbujas.
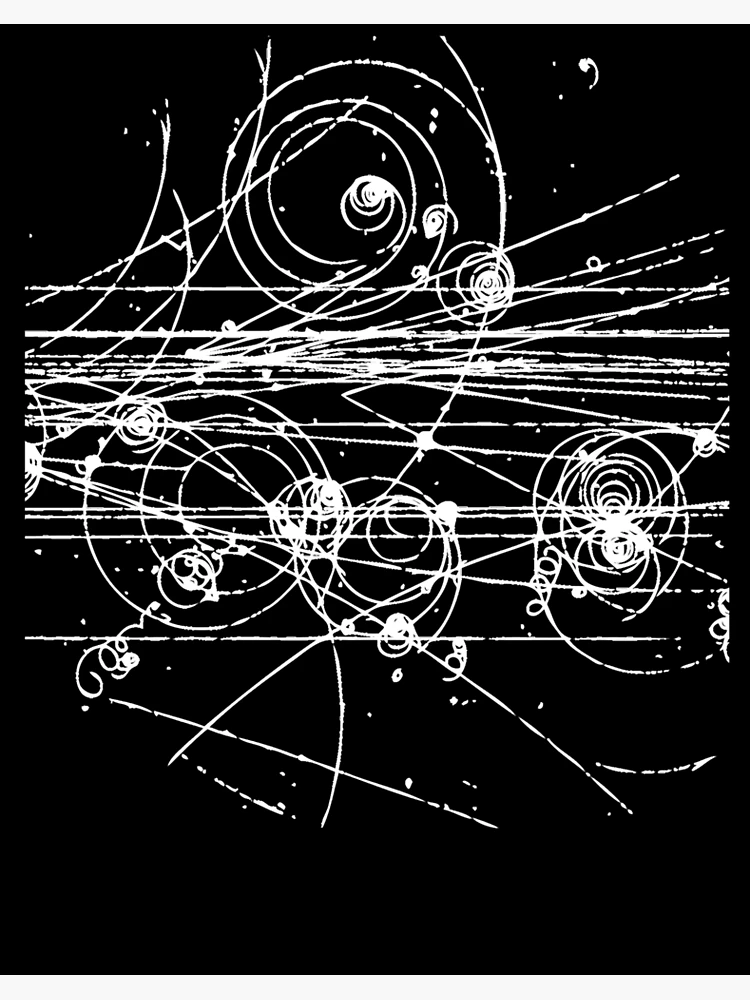

Las partículas cargadas van dejando una huella que se marca para poder comprobarla
Cuando las partículas entran en el compartimento, un pistón disminuye repentinamente la presión dentro del compartimiento. Esto causa que el líquido pase a un estado sobrecalentado, en el cual un efecto minúsculo, tal como el paso de una partícula cargada cerca de un átomo, es suficiente para originar la burbuja de líquido vaporizado. Esta traza puede fotografiarse, pues la cámara tiene en su parte superior una cámara fotográfica. La cámara se somete a un campo magnético constante, lo cual hace que las partículas cargadas viajen en trayectorias helicoidales cuyo radio queda determinado por el cociente entre la carga y la masa de la partícula. De esta manera se pueden obtener la masa y la carga de las partículas que entran en la cámara. Sin embargo, no hay manera de medir con eficacia su velocidad (con lo cual se podría determinar su energía cinética).
Imagen de trazas en la cámara de burbujas del primer evento observado incluyendo bariones Ω, en el Laboratorio Nacional Brookhaven. Dependiendo de su masa y tamaño las partículas producen distintos remolinos en la cámara de burbujas.
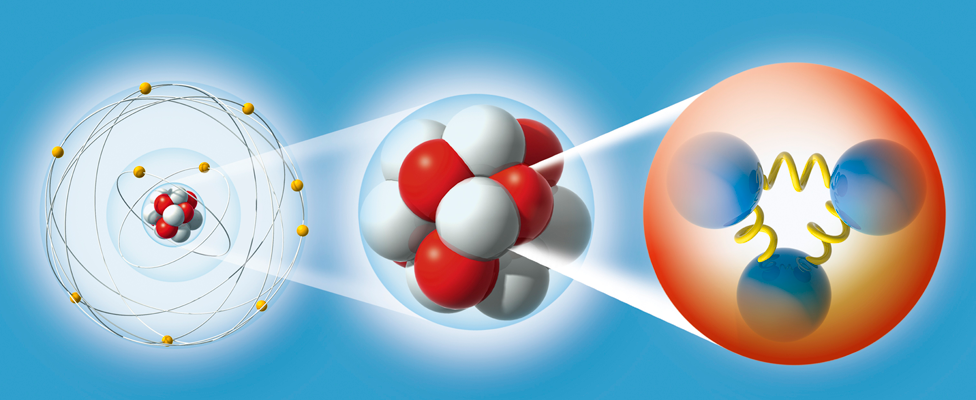
De esta manera, Gell-Mann predijo un décimo barión, el omega-menos (Ω–), y pudo estimar con bastante precisión su masa porque las masas de los otros nueve bariones variaban de una forma sistemática en el gráfico (también consiguió entender que las variaciones de la masa eran una consecuencia de una interacción simple). Sin embargo, estaba claro que la Ω-, con una extrañeza S = -3, no tenía ninguna partícula en la que desintegrarse que no estuviera prohibida por las leyes de conservación de la interacción fuerte. De modo que, la Ω- sólo podía ser de tan sólo 10¯²³ segundos como los demás miembros del multiplete, sino que tenía que ser del orden de 10¯¹⁰ segundos. Consecuentemente, esta partícula debería viajar varios centímetros antes de desintegrarse y esto la haría fácilmente detectable. La Ω¯ fue encontrada en 1964 con exactamente las mismas propiedades que había predicho Gell-Mann.
Se identificaron estructuras multipletes para la mayoría de los demás bariones y mesones y Gell-Mann también consiguió explicarlas. Sugirió que los mesones, igual que los bariones, debían estar formados por elementos constitutivos “más fundamentales aún”. Gell-Mann trabajaba en el Instituto de Tecnología de California en Pasadena (CalTech), donde conversaba a menudo con Richard Feynman. Eran ambos físicos famosos pero con personalidades muy diferentes. Gell-Mann, por ejemplo, es conocido como un entusiasta observador de Pájaros, familiarizado con las artes y la literatura y orgulloso de su conocimiento de lenguas extranjeras.
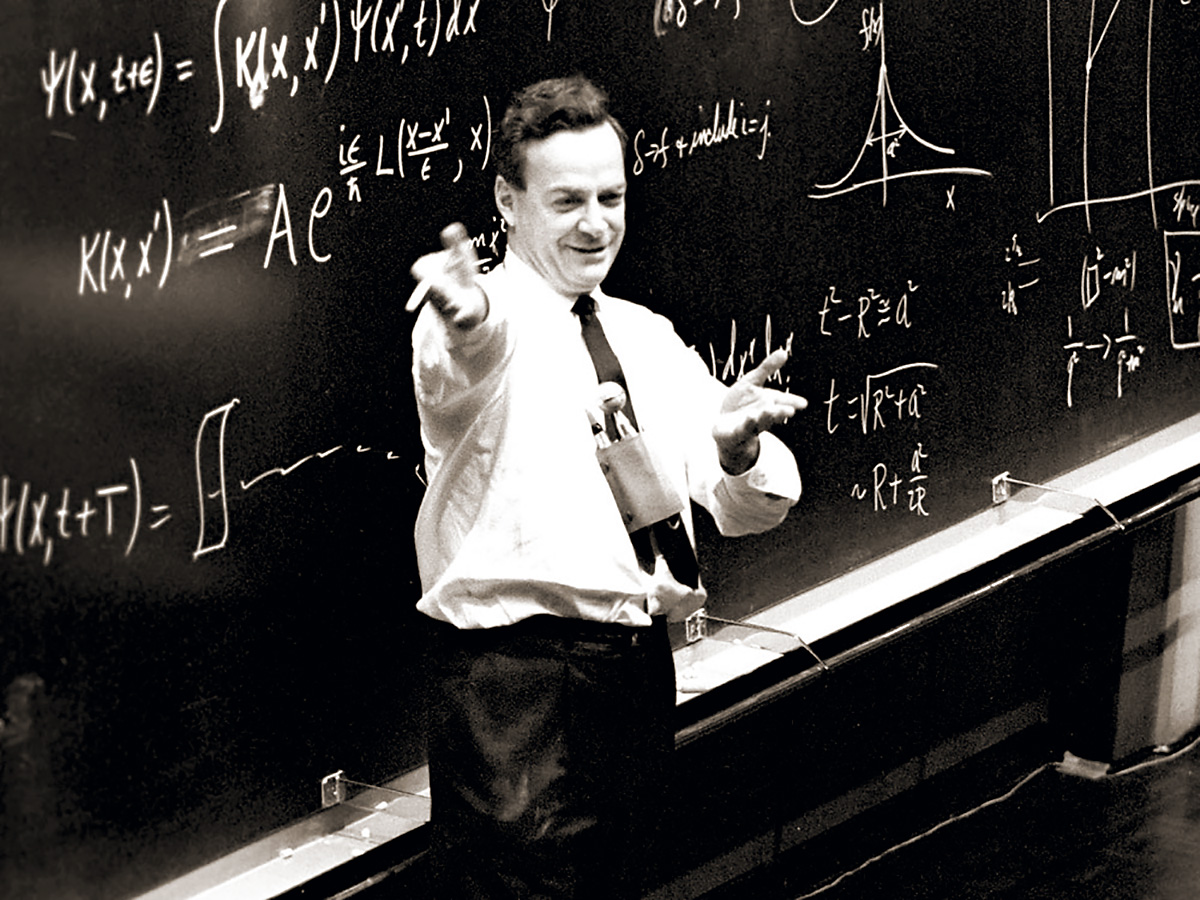
A comienzos de los años sesenta, un profesor del Instituto de Tecnología de California (Caltech) imparte un curso completo de física ante una cada día más numerosa. Su nombre: Richard Feynman
Feynman fue un hombre hecho a sí mismo, un analista riguroso que se reía de cualquier cosa que le recordara la autoridad establecida. Hay una anécdota que parece no ser cierta de hecho, pero que me parece tan buena que no puedo evitar el contarla; podía haber sucedido de esta forma. Gell-Mann le dijo a Feynman que tenía un problema, que estaba sugiriendo un nuevo tipo de ladrillos constitutivos de la materia y que no sabía qué nombre darles. Indudablemente debía haber de haber pensado en utilizar terminología latina o griega, como ha sido costumbre siempre en la nomenclatura científica. “Absurdo”, le dijo Feynman; “tú estás hablando de cosas en las que nunc ase había pensado antes. Todas esas preciosas pero anticuadas palabras están fuera de lugar. ¿Por qué no los llamas simplemente “shrumpfs”, “quacks” o algo así?”.

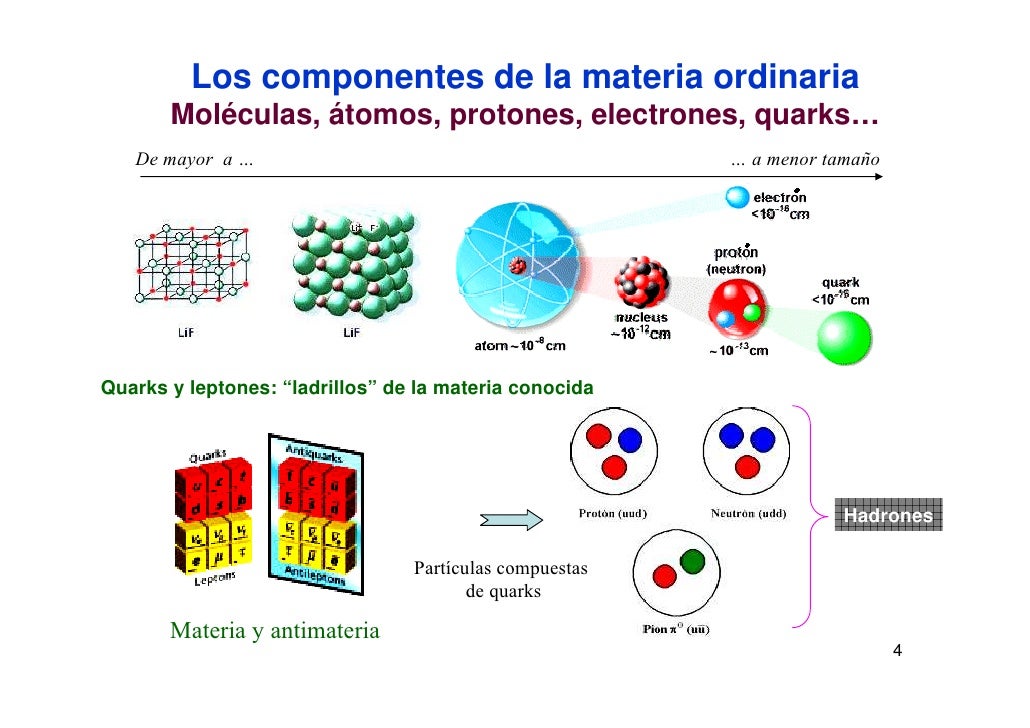
Los pequeños componentes de la materia ordinaria
Cuando algún tiempo después le pregunté a Gell-Mann, éste negó que tal conversación hubiera tenido lugar. Pero la palabra elegida fue quark, y la explicación de Gell-Mann fue que la palabra venía de una frase de Fynnegan’s Wake de James Joyce; “¡Tres quarks para Muster Mark!”. Y, efectivamente así es. A esas partículas les gusta estar las tres juntas. Todos los bariones están formados por tres quarks, mientras que los mesones están formados por un quark y un anti-quark.
Los propios quarks forman un grupo SU(3) aún más sencillo. Los llamaremos “arriba (u)”, “abajo” (d), y “extraño” (s). Las partículas “ordinarias” contienen solamente quarks u y d. Los hadrones “extraños” contienen uno o más quarks s (o antiquarks ŝ).
La composición de quarks de espín 3/2 se puede ver en cualquier tabla de física.. La razón por la que los bariones de espín ½ sólo forman un octete es más difícil de explicar. Está relacionada con el hecho de que en estos estados, al menos dos de los quarks tienen que ser diferentes unos de otros.
Junto con los descubrimientos de los Hadrones y de sus componentes, los Quarks, durante la primera mitad del sigo XX, se descubrieron otras partículas. Los Hadrones forman dos ramas, los mesones formados por dos qiuarks y los bariones por tres.
Realmente, la idea de que los hadrones estuvieran formados por ladrillos fundamentales sencillos había sido también sugerida por otros. George Zweig, también en el Cal Tech, en Pasadena, había tenido la misma idea. Él había llamado a los bloques constitutivos “ases!, pero es la palabra “quark” la que ha prevalecido. La razón por la que algunos nombres científicos tienen más éxito que otros es a veces difícil de comprender.
Pero en esta teoría había algunos aspectos raros. Aparentemente, los quarks (o ases) siempre existen en parejas o tríos y nunca se han visto solos. Los experimentadores habían intentado numerosas veces detectar un quark aislado en aparatos especialmente diseñados para ello, pero ninguno había tenido éxito.
Los Quarks no existen de forma aislada, solo se pueden observar dentro de partículas compuestas llamadas hadrones, que pueden ser bariones (como protones y neutrones, formados por tres quarks) o mesones (formados por un quark y un antiquark), debido a un fenómeno llamado confinamiento de color. Este confinamiento hace que los quarks solo sean estables cuando sus cargas de color se combinan para dar como resultado una combinación “incolora”, y esta propiedad se debe a la fuerza del campo de los gluones.
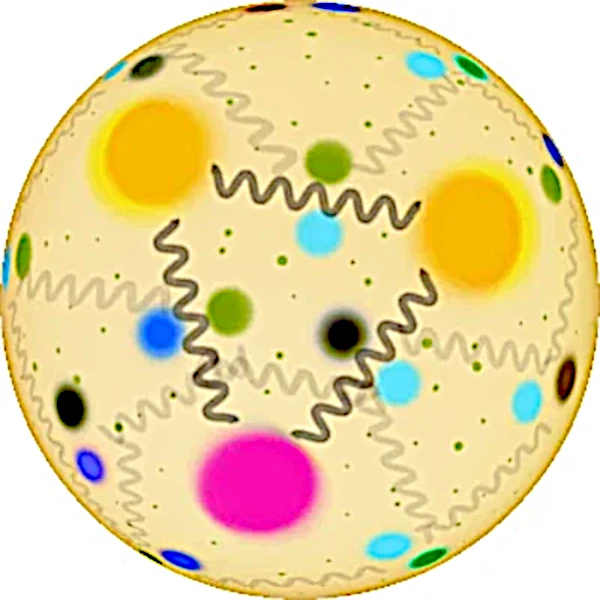
Loa quarks –si se pudieran aislar- tendrían propiedades incluso más extrañas. Por ejemplo, ¿Cuáles serían sus cargas eléctricas? Es razonable suponer que tanto los quarks u como los quarks s y d deban tener siempre la misma carga. La comparación de la tabla 5 con la tabla 2 sugiere claramente que los quarks d y s tienen carga eléctrica -1/3 y el quark u tiene carga +2/3. Pero nunca se han observado partículas que no tengan carga múltiplo de la del electrón o de la del protón. Si tales partículas existieran, sería posible detectarlas experimentalmente. Que esto haya sido imposible debe significar que las fuerzas que las mantienen unidas dentro del hadrón son necesariamente increíblemente eficientes.
Todos sabemos que los Leptones son: El elentrón, el Muón y la partícula Tau y, cada una de ellas tiene su tipo de neutrino: el electrónico, el muónico y el tauónico.
Aunque con la llegada de los quarks se ha clarificado algo más la flora y la fauna de las partículas subatómicas, todavía forman un conjunto muy raro, aún cuando solamente unas pocas aparezcan en grandes cantidades en el universo (protones, neutrones, electrones y fotones). Como dijo una vez Sybren S. de Groot cuando estudiaba neutrinos, uno realmente se enamora de ellos. Mis estudiantes y yo amábamos esas partículas cuyo comportamiento era un gran misterio. Los leptones, por ser casi puntuales, son los más sencillos, y por tener espín se ven afectados por la interacción que actúa sobre ellos de forma muy complicada, pero la interacción débil estaba bastante bien documentada por entonces.

Los hadrones son mucho más misteriosos. Los procesos de choque entre ellos eran demasiado complicados para una teoría respetable. Si uno se los imagina como pequeñas esferas hachas de alguna clase de material, aún quedaba el problema de entender los quarks y encontrar la razón por la que se siguen resistiendo a los intentos de los experimentadores para aislarlos.
Emilio Silvera Vázquez
Si queréis saber más sobre el tema, os recomiendo leer el libro Partículas de Gerard ´t Hooft.
Sep
13
De lo pequeño a lo grande y, conocer la Naturaleza…¡No será...
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)
“Una formulación muy hermosa que, creo, procede de América es la siguiente: alguien que ha golpeado a otro afirma que sólo ha movido sus puños libremente; el juez, sin embargo, replica: «La libertad de movimiento de tus puños está limitada por la nariz de tu vecino».
Debido al principio de exclusión de Pauli, es imposible que dos fermiones ocupen el mismo cuántico (al contrario de lo que ocurre con los bosones). La condensación Bose-Einstein es de importancia fundamental explicar el fenómeno de la super-fluidez. A temperaturas muy bajas (del orden de 2×10-7º K) se formar un condensado de Bose-Einstein, en el que varios miles de átomos forman una única entidad (un super-átomo). efecto ha sido observado con átomos de rubidio y litio. Como ha habréis podido suponer, la condensación Bose-Einstein es llamada así en honor al físico Satyendra Nath Bose (1.894 – 1.974) y a Albert Einstein. Así que, el principio de exclusión de Pauli tiene aplicación no sólo a los electrones, sino también a los fermiones; pero no a los bosones.
Las reglas de la mecánica cuántica tienen que ser aplicadas si queremos describir estadísticamente un sistema de partículas que obedece a reglas de ésta teoría en vez de las de la mecánica clásica. En estadística cuantica, los estados de energía se considera que están cuantizados. La estadística de Bose-Einstein se aplica si cualquier de partículas puede ocupar un estado cuántico dado. Dichas partículas (como dije antes) son los bosones que, tienden a juntarse.
Los bosones tienen un angular n h / 2p, donde n es cero o un entero y h es la constante de Planck. bosones idénticos, la función de ondas es siempre simétrica. Si solo una partícula puede ocupar un cuántico, tenemos que aplicar la estadística Fermi-Dirac y las partículas (como también antes dije) son los fermiones que tienen momento angular (n+½) h/2p y cualquier función de ondas de fermionesidénticos es siempre antisimétrica.
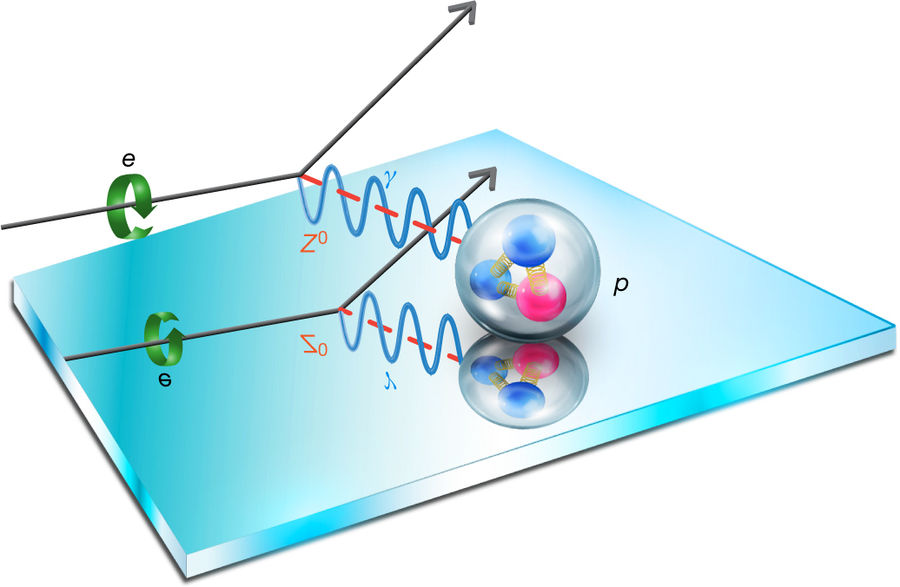
La mejor teoría explicar el mundo subatómico nació en 1928 cuando el teórico Paul Dirac combinó la mecánica cuántica con la relatividad especial para explicar el comportamiento del electrón. El resultado fue la mecánica cuántica relativista, que se transformó en un ingrediente primario en la teoría cuántica de campos. Con unas pocas suposiciones y ajustes ad-hoc, la teoría cuántica de campos ha probado ser suficientemente poderosa para formar la base del modelo estándar de las partículas y las fuerzas.

La relación el espín y la estadística de las partículas está demostrada por el teorema espín-estadística. En un espacio de dos dimensiones es posible que existan partículas (o cuasipartículas) con estadística intermedia entre bosones y fermiones. Estas partículas se conocen con el de aiones; para aniones idénticos la función de ondas no es simétrica (un cambio de fase de+1) o antisimétrica (un cambio de fase de -1), sino que interpola continuamente entre +1 y -1. Los aniones pueden ser importantes en el análisis del efecto Hall cuántico fraccional y han sido sugeridos como un mecanismo para la superconductividad de alta temperatura.

Resulta fácil comprender cómo un campo magnético la partícula cargada que gira, pero ya no resulta tan fácil saber por qué ha de hacer lo mismo un neutrón descargado. Lo cierto es que cuando un rayo de neutrones incide sobre un hierro magnetizado, no se comporta de la misma forma que lo haría si el hierro no estuviese magnetizado. El magnetismo del neutrón sigue siendo un misterio; los físicos sospechan que contiene cargas positivas y negativas equivalente a cero, aunque por alguna razón desconocida, logran crear un campo magnético cuando gira la partícula.

Particularmente creo que, si el neutrón masa, si la masa es energía (E = mc2), y si la energía es electricidad y magnetismo (según Maxwell), el magnetismo del neutrón no es tan extraño, sino que es un aspecto de lo que en realidad es materia. La materia es la luz, la energía, el magnetismo, en definitiva, la fuerza que reina en el universo y que está presente de una u otra forma en todas partes (aunque no podamos verla).
Sea fuere, la rotación del neutrón nos da la respuesta a esas preguntas:

La primera demostración efectiva de antimateria se tuvo en Brookhaven en 1.965
¿Qué es el antineutrón? Pues, simplemente, un neutrón cuyo movimiento rotatorio se ha invertido; su polo sur magnético, por decirlo así, está arriba y no abajo. En realidad, el protón y el antiprotón, el electrón y el positrón, muestran exactamente el mismo fenómeno de los polos invertidos. Es indudable que las antipartículas pueden combinarse para formar la antimateria, de la misma que las partículas corrientes forman la materia ordinaria.
La primera demostración efectiva de antimateria se tuvo en Brookhaven en 1.965, donde fue bombardeado un blanco de berilio con 7 protones BeV y se produjeron combinaciones de antiprotones y antineutrones, o sea, un anti-deuterón. entonces se ha producido el antihelio 3, y no cabe duda de que se podría crear otros anti-núcleos más complicados aún si se abordara el problema con más interés.
Pero, ¿existe en realidad la antimateria? ¿Hay masas de antimateria en el universo? Si las hubiera, no revelarían su presencia a cierta distancia. Sus efectos gravitatorios y la luz que produjeran serían idénticos a los de la materia corriente. Sin embargo, cuando se encontrasen las masas de las distintas materias, deberían ser claramente perceptibles las reacciones masivas del aniquilamiento mutuo resultante del encuentro. Así pues, los astrónomos observan especulativamente las galaxias, tratar de encontrar alguna actividad inusual que delate interacciones materia-antimateria.
…, ¿Hay masas de antimateria en el Universo? ¿Galaxias de antimateria?
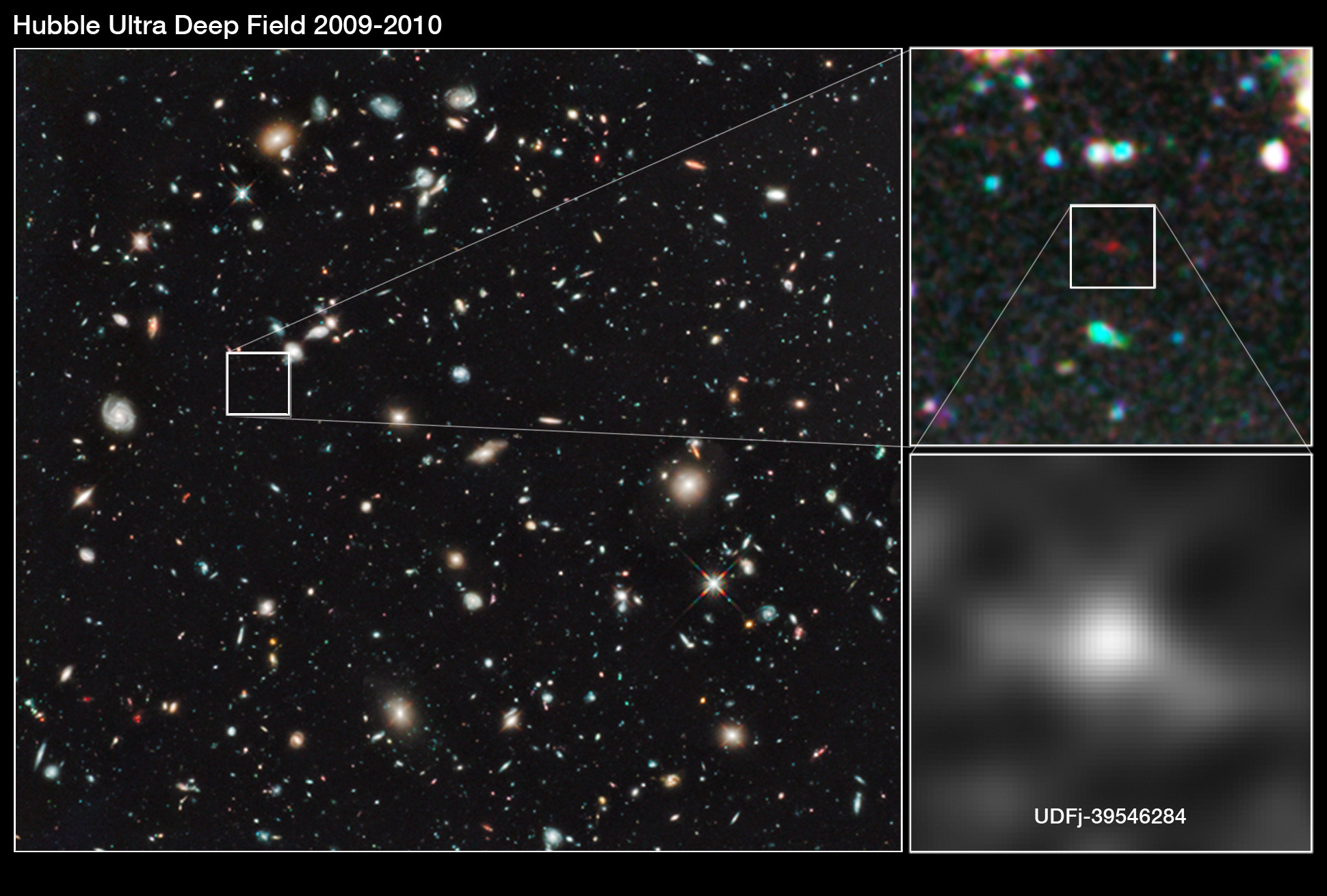
Bueno, sabemos que no son las galaxias las que se alejan, sino que es el espacio el que se expande. Lo que no sabemos es encontrar antimateria en el espacio interestelar y, si la hay y está presente… ¡Aún no la hemos podido localizar! Algunos dicen que hay galaxias de antimateria y, yo digo que tengo un pariente en la galaxia Astrinia del cúmulo Ultramón a diez mil millones de años-luz de nuestra región.
No parece que dichas observaciones, al menos hasta el , hayan sido un éxito.
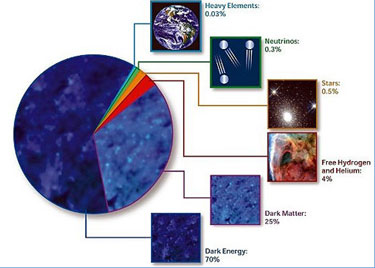
Según estimaciones recientes, resumidas en gráfico de la NASA, alrededor del 70% del contenido energético del Universo consiste en energía oscura, cuya presencia se infiere en su efecto sobre la expansión del Universo pero sobre cuya naturaleza última no se sabe casi nada.
¿Es posible que el Universo este formado casi enteramente por materia, con muy poca o ninguna antimateria? Y si es así, ¿por qué? dado que la materia y la antimateria son equivalentes en todos los aspectos, excepto en su oposición electromagnética, cualquier fuerza que crease una originaria la otra, y el Universo debería estar compuesta de iguales cantidades de la una y de la otra.

Este es el dilema. La teoría nos dice que debería haber allí antimateria, pero las observaciones lo niegan, no lo respaldan. ¿Es la observación la que falla? ¿Y qué ocurre con los núcleos de las galaxias activas, e incluso más aún, con los causares? ¿Deberían ser estos fenómenos energéticos el resultado de una aniquilación materia-antimateria? ¡No creo! Ni siquiera ese aniquilamiento parece ser suficiente, y los astrónomos prefieren aceptar la noción de colapso gravitatorio y fenómenos de agujeros negros como el único mecanismo conocido para producir la energía requerida.
Estábamos hablando de mecánica cuántica y me pasé, sin que me diera , al ámbito de la antimateria y el espacio del macro universo de las galaxias. Sin embargo, y aunque parezcan temas dispares, lo cierto es que, a medida que profundizamos en estas cuestiones, todas nos llevan, de una u otra manera, a relacionar el “mundo de lo muy pequeño” con el “mundo” de lo muy grande que, al fín y al cabo, está hecho de lo que existe en el primero, es decir, partículas infinitesimales de materia y… ¡de antimateria! para que todo quede compensado.
Sus dimensiones y masa le permiten ¡lo imposible! para nosotros. La tensión superficial es una consecuencia de que todas las moléculas y los átomos se atraen unos a otros con una fuerza que nosotros llamamos fuerza de Van der Vaalls. esta fuerza tiene un alcance muy corto. para ser más precisos, diremos que la intensidad de esta fuerza a una distancia r es aproximadamente proporcional a 1/r7. Esto significa que si se reduce la distancia entre dos átomos a la mitad, la fuerza de Van der Vaalls con la que se atraen uno a otro se hace 2 x 2 x 2 x 2 x 2 x 2 x 2 = 128 veces más intensa. Cuando los átomos y las moléculas se acercan mucho unos a otros quedan unidos muy fuertemente a través de esta fuerza.
La mecánica cuántica domina en el micro-mundo de los átomos y de las partículas “elementales”. Nos enseña que en la naturaleza cualquier masa, por sólida o puntual que pueda parecer, tiene un aspecto ondulatorio. Esta onda no es como una onda de agua. Se parece más a una ola de histeria que se expande: es una onda de información. Nos indica la probabilidad de detectar una partícula. La longitud de onda de una partícula, la longitud cuántica, se hace menor cuanto mayor es la masa de esa partícula.

Por el contrario, la relatividad general era siempre necesaria cuando se trataba con situaciones donde algo viaja a la velocidad de la luz, o está muy cerca o donde la gravedad es muy intensa. Se utiliza para describir la expansión del universo o el comportamiento en situaciones extremas, como la formación de agujeros negros.
La fuerza nuclear fuerte es la más potente del Universo. Mantiene a los Quarks cinfinados
Sin embargo, la gravedad es muy débil comparada con las fuerzas que unen átomos y moléculas y demasiado débil para tener cualquier efecto sobre la estructura del átomo o de partículas subatómicas, se trata con masas tan insignificantes que la incidencia gravitatoria es despreciable. Todo lo contrario que ocurre en presencia de masas considerables como planetas, estrellas y galaxias, donde la presencia de la gravitación curva el espacio y distorsiona el tiempo.
Como resultado de estas propiedades antagónicas, la teoría cuántica y la teoría relativista gobiernan reinos diferentes, muy dispares, en el universo de lo muy pequeño o en el universo de lo muy grande. Nadie ha encontrado la manera de unir, sin fisuras, estas dos teorías en una sola y nueva de Gravedad-Cuántica.
¿Cuáles son los límites de la teoría cuántica y de la teoría de la relatividad general de Einstein? Afortunadamente, hay una respuesta simple y las unidades de Planck nos dicen cuales son. En realidad, es la propia Naturaleza la que marca esos límites que Stoney-Planck, supieron plasmar en ecuaciones que los marcan.
![46 - Curso de Relatividad General [Agujero de Gusano de Einstein-Rosen] - YouTube](https://i.ytimg.com/vi/cB3Rx-19SkE/hq720.jpg?sqp=-oaymwEhCK4FEIIDSFryq4qpAxMIARUAAAAAGAElAADIQj0AgKJD&rs=AOn4CLDf4EPyr6cqdblah7w1y2S_Z6hJXg)
Supongamos que tomamos toda la masa del universo visible y determinamos su longitud de onda cuántica. Podemos preguntarnos en qué momento esta longitud de onda cuántica del universo visible superará su tamaño. La respuesta es: cuando el universo sea más pequeño en tamaño que la longitud de Planck, es decir, 10-33 de centímetros, más joven que el tiempo de Planck, 10-43 segundos y supere la temperatura de Planck de 1032 grados. Las unidades de Planck marcan la frontera de aplicación de nuestras teorías actuales. Para comprender en que se parece el mundo a una escala menor que la longitud de Planck tenemos que comprender plenamente cómo se entrelaza la incertidumbre cuántica con la gravedad. Para entender lo que podría haber sucedido cerca del suceso que estamos tentados a llamar el principio del universo, o el comienzo del tiempo, tenemos que penetrar la barrera de Planck. Las constantes de la naturaleza marcan las fronteras de nuestro conocimiento existente y nos dejan al descubierto los límites de nuestras teorías.
En los intentos más recientes de crear una teoría nueva para describir la naturaleza cuántica de la gravedad ha emergido un nuevo significado para las unidades naturales de Planck. Parece que el concepto al que llamamos “información” tiene un profundo significado en el universo. Estamos habituados a vivir en lo que llamamos “la edad de la información”. La información puede ser empaquetada en formas electrónicas, enviadas rápidamente y recibidas con más facilidad que nunca antes. Nuestra evolución en el proceso rápido y barato de la información se suele mostrar en una forma que nos permite comprobar la predicción de Gordon Moore, el fundador de Intel, llamada ley de Moore, en la que, en 1.965, advirtió que el área de un transistor se dividía por dos aproximadamente cada 12 meses. En 1.975 revisó su tiempo de reducción a la mitad hasta situarlo en 24 meses. Esta es “la ley de Moore” cada 24 meses se obtiene una circuitería de ordenador aproximadamente el doble, que corre a velocidad doble, por el mismo precio, ya que, el coste integrado del circuito viene a ser el mismo, constante.



El Universo esconde muchos secretos
Siempre hemos tratado de buscar información del Universo para saber de nuestro entorno, de nuestro Sistema solar, de nuestra Galaxias, de las galaxias lejanas, y, de las mismas estrellas que alumbran los mundos y permite la vida con su luz y su calor. Hemos llegado a saber que somos “polvo de estrellas”, que los materiales que nos conforman están “fabricados” en sus “hornos nucleares”, la fusión crea elementos que, más tarde, forman parte de los mundos y de los seres vivos.

La velocidad de la luz en el vacío es por definición una constante universal de valor 299.792.458 m/s(suele aproximarse a 3·108 m/s), o lo que es lo mismo 9,46·1015 m/año; la segunda cifra es la usada para definir al intervalo llamado año luz. La información se transmitirá a esa velocidad como máximo, nuestro Universo, no permite mayor rapidez, al menos, por los métodos convencionales.
Los límites últimos que podemos esperar para el almacenamiento y los ritmos de procesamiento de la información están impuestos por las constantes de la naturaleza. En 1.981, el físico israelí, Jacob Bekenstein, hizo una predicción inusual que estaba inspirada en su estudio de los agujeros negros. Calculó que hay una cantidad máxima de información que puede almacenarse dentro de cualquier volumen. Esto no debería sorprendernos.
 (Longitud de Planck que al cuadrado sería de 10-66 cm2)
(Longitud de Planck que al cuadrado sería de 10-66 cm2)
Lo que debería hacerlo es que el valor máximo está precisamente determinado por el área de la superficie que rodea al volumen, y no por el propio volumen. El número máximo de bits de información que puede almacenarse en un volumen viene dado precisamente por el cómputo de su área superficial en unidades de Planck. Supongamos que la región es esférica. Entonces su área superficial es precisamente proporcional al cuadrado de su radio, mientras que el área de Planck es proporcional a la longitud de Planck al cuadrado, 10-66 cm2. Esto es muchísimo mayor que cualquier capacidad de almacenamiento de información producida hasta ahora. Asimismo, hay un límite último sobre el ritmo de procesamiento de información que viene impuesto por las constantes de la naturaleza.

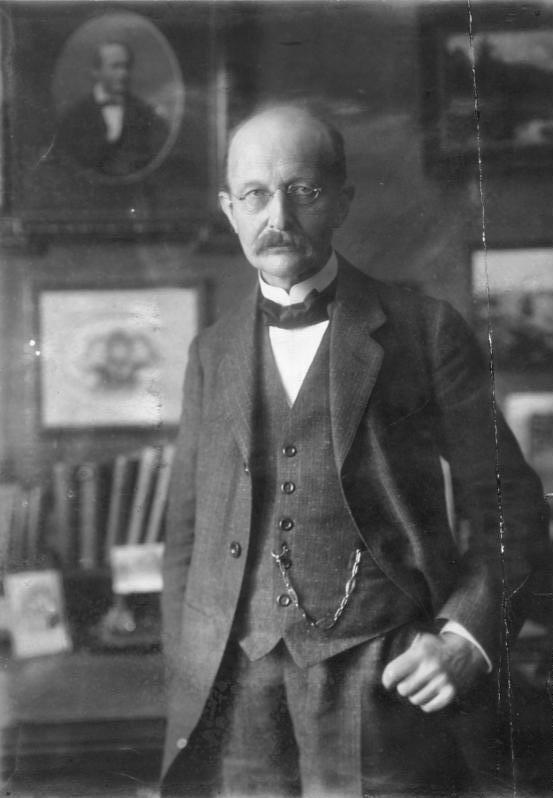
Stoney Planck
No debemos descartar la posibilidad de que seamos capaces de utilizar las unidades de Planck-Stoney para clasificar todo el abanico de estructuras que vemos en el universo, desde el mundo de las partículas elementales hasta las más grandes estructuras astronómicas. Este fenómeno se puede representar en un gráfico que recree la escala logarítmica de tamaño desde el átomo a las galaxias.

Todas las estructuras del universo existen porque son el equilibrio de fuerzas dispares y competidoras que se detienen o compensan las unas a las otras; la atracción y la repulsión. Ese es el equilibrio de las estrellas donde la repulsión termonuclear tiende a expandirla y la atracción (contracción) de su propia masa tiende a comprimirla; así, el resultado es la estabilidad de la estrella. En el caso del planeta Tierra, hay un equilibrio entre la fuerza atractiva de la gravedad y la repulsión atómica que aparece cuando los átomos se comprimen demasiado juntos. Todos estos equilibrios pueden expresarse aproximadamente en términos de dos números puros creados a partir de las constantes e, h, c, G y mprotón

“Tras medir alfa en unas 300 galaxias lejanas, vimos un patrón constante: este número, que nos dice la fuerza del electromagnetismo, no es igual en otras partes que en la Tierra, y parecer variar de forma continua a lo largo de un eje”. Algunos se empeñan en variar la constante de estructura fina y, si eso llegara a producirse… las consecuencias serían funestas para nosotros. Otros estudios nos dicen que esa constante, no ha variado a lo largo de los miles de millones de años del Universo y, así debe ser, o, si varió, lo hizo en una escala ínfima.
|
α = 2πe2 / hc ≈ 1/137 |
|
αG = (Gmp2)2 / hc ≈ 10-38 |
Si varian algunas de las dos en sólo una diezmillonésima, muchas de las cosas que conforman el Universo serían imposible y, la consecuencia sería, la ausencia de vida. La identificación de constantes adimensionales de la naturaleza como a (alfa) y aG, junto con los números que desempeñan el mismo papel definitorio para las fuerzas débil y fuerte de la naturaleza, nos anima a pensar por un momento en mundos diferentes del nuestro. Estos otros mundos pueden estar definidos por leyes de la naturaleza iguales a las que gobiernan el universo tal como lo conocemos, pero estarán caracterizados por diferentes valores de constantes adimensionales. Estos cambios numéricos alterarán toda la fábrica de los mundos imaginarios. Los átomos pueden tener propiedades diferentes. La gravedad puede tener un papel en el mundo a pequeña escala. La naturaleza cuántica de la realidad puede intervenir en lugares insospechados.


Lo único que cuenta en la definición del mundo son los valores de las constantes adimensionales de la naturaleza (así lo creían Einstein y Planck). Si se duplica el valor de todas las masas no se puede llegar a saber, porque todos los números puros definidos por las razones de cualquier par de masas son invariables.
“Todos los físicos del mundo, deberían tener un letrero en el lugar más visible de sus casas, para que al mirarlo, les recordara lo que no saben. En el cartel sólo pondría esto: 137. Ciento treinta y siete es el inverso de algo que lleva el nombre de constante de estructura fina”
Este número guarda relación con la posibilidad de que un electrón emita un fotón o lo absorba. La constante de estructura fina responde también al nombre de “alfa” y sale de dividir el cuadrado de la carga del electrón, por el producto de la velocidad de la luz y la constante de Planck. Tanta palabrería y numerología no significan otra cosa sino que ese solo numero, 137, encierra los misterios del electromagnetismo (el electrón, e–), la relatividad (la velocidad de la luz, c), y la teoría cuántica (la constante de Planck, h).

Todo eso está relacionado: leyes fundamentales, constantes, materia y espacio tiempo… ¡nosotros! Es posible (digo posible), que finalmente no seamos ni tanto ni tan poco como a veces creemos. Dejemos en un término medio nuestra valía en el contexto del Universo, aunque, poder crear ideas y pensamientos… ¡No es cosa baladí!
Emilio Silvera V.
















 Totales: 88.969.257
Totales: 88.969.257 Conectados: 52
Conectados: 52