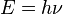Oct
20
¡Fisica! Siempre la Física
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física Cuántica ~
Clasificado en Física Cuántica ~
 Comments (0)
Comments (0)

¡El Universo! ¿Sería eso lo que pasó?
Como nunca dejaremos a aprender cosas nuevas, de desvelar secretos de la Naturaleza, de seguir investigando en busca de “otras verdades”, de elaborar nuevos modelos y nuevas Teorías que nos acerquen, cada vez más a la realidad del mundo (ese es, de momento, nuestro cometido), estamos abocados a tratar de saber lo que no sabemos y que, no pocas veces, creemos que sabemos. Ya lo dijo Popper:
“Cuanto más profundizo en el saber de las cosas, más consciente soy de lo poco que sé. Mis conocimientos son finitos , mi ignorancia, es infinita“.
Lo que nos lleva a la versión antigua del dicho: “Sólo se que no se nada” de Sócrates.

Las sustancias formadas por una sola clase de átomos se llaman elementos químicos. La palabra “átomo” procede del griego ατομος, que significa “indivisible” y el uso de la palabra “elemento” sugiere que se ha llegado a los ladrillos básicos con los que está formada la materia. De hecho, esta es la imagen que se tenía a mediados del siglo XIX cuando se acuñaron estos términos. Sin embargo, hoy sabemos que todo esto es falso, que los átomos se pueden dividir y que, de esta manera, los elementos han dejado de ser verdaderamente elementales. Los físicos continúan con esta nomenclatura aunque sea formalmente incorrecta, ya que, la costumbre, como dicen los juristas, no pocas veces rigen la jerga de las leyes.

“La revolución de la mecánica cuántica empieza a materializarse, y el qubit es el principal protagonista. Siendo la unidad mínima de información de extraño mundo, permitirá procesar toda la información existente en segundos.” El futuro que nos aguarda es inimaginable y cada día que pasa aparecen nuevos logros tecnológicos que nos sitúan en otro mundo, otra sociedad, otras nuevas formas de vivir y de comprender.

Sí, son los electrones los que dan al átomo su forma esférica
A todo esto y hablando de los átomos, por fuerza, nos tenemos que acordar del electrón que da al átomo su esférica. Son partículas cargadas eléctricamente que se mueven alegremente alrededor del núcleo. El electrón es muy ligero: su masa es solamente 1/1.836 de la del núcleo más ligero (el hidrógeno). La carga eléctrica del electrón es de signo opuesto a la del núcleo, de manera que los electrones están fuertemente atraídos el núcleo y se repelen mutuamente. Si la carga eléctrica total de los electrones en un átomo iguala a la del núcleo, lo que generalmente se necesitan varios electrones, se dice que el átomo está en equilibrio o que es eléctricamente neutro.
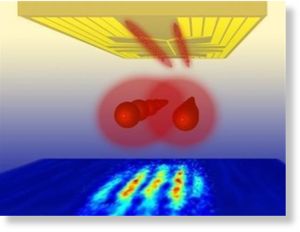
Un experimento realizado por científicos del Centro de Viena para la Ciencia y Tecnología Cuánticas ha demostrado que, en el mundo cuántico, la transición hacia el equilibrio térmico es más interesante y más complicada de lo que se pensaba.
Según destaca el , publicado en ‘Science’, entre un ordenado inicial y un estado final estadísticamente mixto, puede emerger un “cuasi-estacionario estado intermedio”. Este estado intermedio ya exhibe algunas propiedades como el equilibrio, pero parte de las características del estado inicial permanecen visibles durante un período de tiempo muy largo.
El fenómeno se denomina “pre-termalización” y desempeña un papel importante en diversos procesos de no equilibrio en la física cuántica. Podría, por ejemplo, ayudarnos a comprender el estado del universo temprano.

La fuerza a la que obedecen los electrones, la denominada fuerza electrostática o de Coulomb, es matemáticamente bastante sencilla y, sin embargo, los electrones son los responsables de las importantes propiedades de los “enlaces químicos”. Esto se debe a que las leyes de movimiento de los electrones están regidas completamente por la “mecánica cuántica”, teoría que se completó a principios del siglo XX. Es una teoría paradójica y difícil de entender y explicar, pero al mismo tiempo es muy interesante, fantástica y revolucionaria. uno se introduce en las maravillas de la mecánica cuántica es como si hiciera un viaje a un universo que está situado fuera de este mundo nuestro, ya que, las cosas que allí se ven, desdicen todo lo que dicta nuestro sentido común de cómo tiene que ser el mundo que nos rodea.
Sincronización perfecta, ¡es una sinfonía!
No solamente los electrones, sino también los núcleos atómicos y los átomos en su conjunto obedecen y se rigen por la mecánica cuántica. La Física del siglo XX empezó exactamente en el año 1900, cuando el físico alemán Max Planck, escribió un artículo de ocho páginas y allí propuso una posible solución a un problema que había intrigando a los físicos durante años. Es el problema de la luz que emiten los cuerpos calentados a una cierta temperatura, y también la radiación infrarroja emitida, con menos intensidad, por los objetos más fríos.
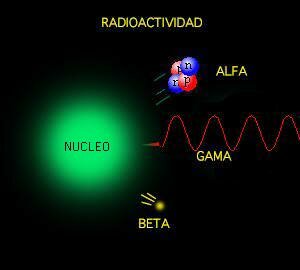

Estaban bien aceptados entonces que esta radiación tenía un origen electromagnético y que se conocían las leyes de la naturaleza que regían estas ondas electromagnéticas. También se conocían las leyes para el frío y el calor, la así llamada “termodinámica”, o al menos eso parecía. Pero si usamos las leyes de la termodinámica para calcular la intensidad de la radiación, el resultado no tiene ningún sentido. Los cálculos nos dicen que se emitiría una cantidad infinita de radiación en el ultravioleta más lejano, y, luego, esto no es lo que sucede. Lo que se observa es que la intensidad de la radiación muestra un pico a una cierta longitud de onda característica, y que la intensidad disminuye tanto para las longitudes mayores como para las longitudes menores. Esta longitud característica es inversamente proporcional a la temperatura absoluta del objeto radiante (la temperatura absoluta se define por una escala de temperatura que empieza a 273 ºC bajo cero). Cuando a 1.000 ºC un objeto se pone al “rojo vivo”, el objeto está radiando en la zona de luz visible.

El espectro electromagnético se extiende la radiación de menor longitud de onda, como los rayos gamma y los rayos X, pasando por la luz ultravioleta, la luz visible y los rayos infrarrojos, hasta las ondas electromagnéticas de mayor longitud de onda, como son las ondas de radio. Se cree que el límite la longitud de onda más pequeña posible es la longitud de Planck mientras que el límite máximo sería el tamaño del Universo.
Lo que Planck propuso fue simplemente que la radiación sólo podía ser emitida en de un tamaño dado. La cantidad de energía de uno de esos paquetes, o cuantos, es inversamente proporcional a la longitud de la onda y, por lo tanto, proporcional a la frecuencia de la radiación emitida. La sencilla fórmula es:
donde h es la constante de Planck (cuyo valor es 6,626 × 10−34 J·s). Sólo los fotones con una frecuencia alta (por encima de un valor umbral específico) podían provocar la corriente de electrones. Por ejemplo, la luz azul emitía unos fotones con una energía suficiente para arrancar los electrones del metal, mientras que la luz roja no. Una luz más intensa por encima del umbral mínimo puede arrancar más electrones, pero ninguna cantidad de luz por debajo del mismo podrá arrancar uno solo, por muy intenso que sea su brillo.


El esquema del Efecto fotoeléctrico nos muestra como la luz arranca electrones de la placa.
Poco tiempo después, en 1905, Einstein formuló esta teoría de una forma mucho más tajante: el sugirió que los objetos calientes no son los únicos que emiten radiación en de energía, sino que toda la radiación consiste en múltiplos de los paquetes de energía de Planck. El príncipe francés Louis-Victor de Broglie, dándole otra vuelta a la teoría, propuso que no sólo cualquier cosa que oscila tiene una energía, sino que cualquier cosa con energía se debe comportar como una “onda” que se extiende en una cierta región del espacio, y que la frecuencia, v, de la oscilación verifica la ecuación de Planck. Por lo tanto, los cuantos asociados con los rayos de luz deberían verse como una clase de partículas elementales: el fotón. Todas las demás clases de partículas llevan asociadas diferentes ondas oscilatorias de campos de fuerza.
El curioso comportamiento de los electrones en el interior del átomo, descubierto y explicado por el famoso físico danés Niels Bohr, se pudo atribuir a las ondas de De Broglie. Poco después, en 1926, Erwin Schrödinger descubrió escribir la teoría ondulatoria de Debroglie con ecuaciones matemáticas exactas. La precisión con la cual se podían realizar cálculos era asombrosa, y pronto quedó claro que el comportamiento de todos los objetos pequeños estaban exactamente determinados por la recién descubiertas “ecuaciones de onda cuánticas”.

Pocas dudas nos pueden caber a estas alturas de que la mecánica cuántica (de Planck) y, la Relatividad –tanto especial general- (de Einstein), además de ser las dos teorías más importantes de la Física de nuestro tiempo, funcionan de tal forma que uno, cuando profundiza en sus predicciones y las compara con lo que ocurre en el Universo, no por menos que, asombrarse, al comprobar como unas mentes humanas han sido capaces de llegar a estos profundos pensamientos que nos acerca a la realidad de la Naturaleza, al mismo tiempo que nos aleja de nuestra propia realidad.

Sí, están ahí pero, en realidad, no sabemos, a ciencia cierta, ni cómo se formaron las galaxias
¿Qué encontraremos cuando sea posible verificar la Teoría de cuerdas? ¿Qué hay más allá de los Quarks? ¿Sabremos alguna vez lo que es una singularidad? ¿Será verdad la existencia de esa materia oscura de la que tanto se habla? ¿Podremos al fín, encontrar esa fuente de energía que tanto necesita la Humanidad para dar ese segundo paso el futuro? ¿Tendremos, acaso, algún destino que no sea el de la irremisible extinción?
¡Preguntas! Preguntas y más preguntas que no podemos contestar. Es desesperante estar inmersos en inmenso océano de ignorancia. ¿Cuándo sabremos? El el epitafio que Hilbert ordenó esculpir en su Tumba, nos lo prometía: “Tenemos que saber, sabremos”. Si, ¿pero cuándo?

Lo cierto es que, las reglas de la mecánica cuántica tienen que ser aplicadas si queremos describir estadísticamente un sistema de partículas que obedece a reglas de ésta teoría en vez de las de la mecánica clásica. En estadística cuantica, los estados de energía se considera que están cuantizados. La estadística de Bose-Einstein se aplica si cualquier de partículas puede ocupar un estado cuántico dado. Dichas partículas (como dije antes) son los bosones que, tienden a juntarse.
Los bosones tienen un angular n h / 2p, donde n es cero o un entero y h es la constante de Planck. bosones idénticos, la función de ondas es siempre simétrica. Si solo una partícula puede ocupar un cuántico, tenemos que aplicar la estadística Fermi-Dirac y las partículas (como también antes dije) son los fermiones que tienen momento angular (n+½) h/2p y cualquier función de ondas de fermiones idénticos es siempre antisimétrica.
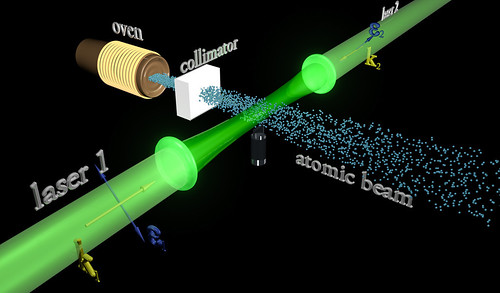
La mejor teoría explicar el mundo subatómico nació en 1928 cuando el teórico Paul Dirac combinó la mecánica cuántica con la relatividad especial para explicar el comportamiento del electrón. El resultado fue la mecánica cuántica relativista, que se transformó en un ingrediente primario en la teoría cuántica de campos. Con unas pocas suposiciones y ajustes, la teoría cuántica de campos ha probado ser suficientemente poderosa para formar la base del modelo estándar de las partículas y las fuerzas que rigen el universo.

La relación el espín y la estadística de las partículas está demostrada por el teorema espín-estadística. En un espacio de dos dimensiones es posible que existan partículas (o cuasipartículas) con estadística intermedia entre bosones y fermiones. Estas partículas se conocen con el de aiones; para aniones idénticos la función de ondas no es simétrica (un cambio de fase de+1) o antisimétrica (un cambio de fase de -1), sino que interpola continuamente entre +1 y -1. Los aniones pueden ser importantes en el análisis del efecto Hall cuántico fraccional y han sido sugeridos como un mecanismo para la superconductividad de alta temperatura.
Debido al principio de exclusión de Pauli no es imposible que dos fermiones ocupen el mismo espacio cuántico (al contrario de lo que ocurre con los bosones). Y, precisamente por eso, se degeneran electrones y neutrones dando lugar a la formación de estrellas enanas blancas y de neutrones que, encuentran la estabilidad frenando la fuerza de gravedad.
La condensación de Bose-Einstein es de importancia fundamental explicar el fenómeno de la superfluidez. A temperaturas muy bajas (del orden de 2×10-7k) se formar un condensado de Bose-Einstein, en el que varios miles de átomos forman una única entidad (un superátomo). efecto ha sido observado con átomos de rubidio y litio. Este efecto (condensación Bose-Einstein), ya habréis podido suponer, es llamado así en honor al físico Satyendra Naht Bose (1.894-1.974) y de Albert Einstein.

Más reciente es la obtención del Condensado de Bose-Einstein (BEC); en este caso las bases teóricas se postularon en la década de los 20 en manos de Satyendra Nath Bose y Albert Einstein. El primero describe ciertas reglas para determinar si dos fotones deberían considerarse idénticos o diferentes (Estadísticas de Bose) y Einstein aplica dichas reglas a los átomos intentando averiguar como se comportarían. Así, halla los efectos de que a muy bajas temperaturas los átomos están al mismo nivel cuántico produciendo fenómenos como la superfluidez o la superconductividad.
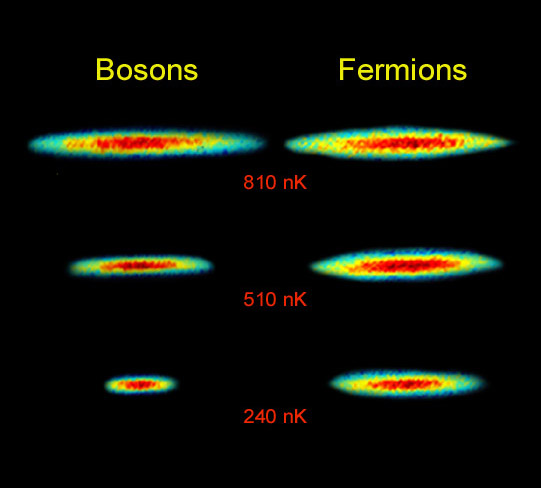
Distribución de momentos que confirma la existencia de un estado de agregación de la materia, el condensado de Bose-Einstein. obtenidos en un gas de átomos de rubidio, la coloración indica la cantidad de átomos a cada velocidad, con el rojo indicando la menor y el blanco indicando la mayor. Las áreas blancas y celestes indican las menores velocidades. A la izquierda se observa el diagrama inmediato anterior al condensado de Bose-Einstein y al centro el inmediato posterior. A la derecha se observa el diagrama luego de cierta evaporación, con la sustancia cercana a un condensado de Bose-Einstein puro. El pico no es infinitamente angosto debido al Principio de indeterminación de Heisenberg: dado que los átomos están confinados en una región del espacio, su distribución de velocidades posee necesariamente un cierto ancho mínimo. La distribución de la izquierda es para T > Tc (sobre 400 nanokelvins (nK)), la central para T < Tc (sobre 200 nK) y la de la derecha para T << Tc (sobre 50 nK).

… del sistema binario descubierto a 7,000 años luz de la Tierra, que está formado por una estrella de neutrones (el círculo más grande) y enana blanca (el …
Las estrellas enanas blancas, de neutrones y los púlsares existen, precisamente, por el principio de exclusión de Pauli que, degenera electrones y neutrones cuando las estrellas masivas, al final de su existencia, explotan como Supernovas y´su masa se contraen sobre sí misma más y más. Si la estrella es demasiado masiva, entonces ni ese principio de exclusión puede frenar a la Gravedad y se convierte en un Agujero negro.
Así que, el principio de exclusión de Pauli tiene aplicación no sólo a los electrones, sino también a los fermiones; pero no a los bosones. Si nos fijamos en todo lo que estamos hablando aquí, nos daremos de que la mecánica cu´çantica es extraña y siendo fácil comprender como forma un campo magnético la partícula cargada que gira, no resulta tan fácil saber por qué ha de hacer lo mismo un neutrón descargado.
Lo cierto es que ocurre así. La prueba directa más evidente de ello es que cuando un rayo de neutrones incide sobre un hierro magnetizado, no se comporta de la misma que lo haría si el hierro no estuviese magnetizado. El magnetismo del neutrón sigue siendo un misterio; los físicos sospechan que contiene cargas positivas y negativas equivalentes a cero, aunque por alguna razón desconocida, lograr crear un campo magnético cuando gira la partícula.
emilio silvera
Oct
20
Coreografía de un par de electrones
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)

Físicos y químicos nos sorprenden cada día con el control que pueden ejercer sobre la materia. Por primera vez, investigadores españoles y alemanes hemos conseguido obtener la película del movimiento de los dos electrones que constituyen el átomo de helio e incluso controlar los pasos de esta singular pareja de baile. Para ello, hemos empleado una combinación de pulsos de luz visible y ultravioleta con una duración de tan solo unos pocos cientos de attosegundos (un attosegundo es una mil millonésima de una milmillonésima parte de un segundo). El control sobre el movimiento de pares de electrones podría revolucionar nuestra visión de la química, ya que los enlaces entre los distintos átomos que constituyen las moléculas, desde el agua al ADN, son el resultado del apareamiento de dos electrones. Por tanto, la perspectiva de utilizar láseres de attosegundos para controlar el destino de los electrones apareados en un enlace abre el camino a la producción de sustancias que no pueden ser sintetizadas utilizando procedimientos químicos convencionales.

Representación animada de un átomo de deuterio, uno de los isótopos del hidrógeno.
Para explicar algunas características extrañas en el espectro del átomo de hidrógeno, en 1913, el físico Niels Bohr introdujo un modelo planetario en el que el electrón cargado negativamente, unido al núcleo cargado positivamente por la fuerza electrostática de Coulomb, está restringido a moverse solamente a lo largo de órbitas muy concretas. Esta cuantificación del movimiento electrónico abrió un nuevo capítulo de la física y química modernas, sin el cual no se podría haber alcanzado el conocimiento de la materia del que se dispone hoy en día. En el modelo de Bohr, las cosas suceden rápidamente: el año sideral, es decir, el tiempo que el electrón necesita para completar la órbita más corta alrededor del núcleo, tiene la increíblemente corta duración de 0.000 000 000 000 000 152 segundos, o 152 attosegundos (as), un valor que se hace aún más pequeño cuando se consideran elementos más pesados en la tabla periódica de los elementos químicos.

… investigadores de la UAM consigue por primera vez utilizar pulsos láser con una duración de attosegundos para observar el movimiento de los electrones …
El attosegundo es, de hecho, la escala de tiempo natural en el que los electrones se mueven en la materia ordinaria. El movimiento ultrarrápido predicho por el modelo de Bohr no pudo ser confirmado directamente hasta que, a comienzos de este siglo, una serie de avances revolucionarios generó la tecnología láser capaz de producir destellos de luz suficientemente cortos (el récord mundial es de 67 as) para hacer fotografías del movimiento de un electrón y así generar la película de ese movimiento. En contraste con el mundo macroscópico, una película del movimiento del electrón no revela un desplazamiento a lo largo de una trayectoria bien definida. Como consecuencia del comportamiento ondulatorio de la materia a nivel atómico, el electrón aparece como una nube difusa (o paquete de ondas) en movimiento. La densidad de la nube indica la probabilidad de encontrar al electrón en distintas regiones del espacio.

Observar el comportamiento de los electornes es todo un espectáculo
En los sistemas más grandes que el hidrógeno, con varios electrones, la misma fuerza de Coulomb que une a un electrón con el núcleo también actúa repulsivamente entre los electrones. El efecto de tal repulsión es apantallar la carga nuclear, debilitando así el efecto atractivo del núcleo sobre cada uno de los electrones. Sin embargo, en gran medida, los electrones siguen actuando como partículas independientes y, por tanto, el movimiento del paquete de ondas que representa a todos los electrones no es mucho más complicado que el observado para un solo electrón en el átomo de hidrógeno. Hasta ahora, los experimentos llevados a cabo para seguir el movimiento de los paquetes de onda en átomos complejos fueron capaces de poner en marcha un solo electrón a la vez, confirmando esta imagen de que los electrones se mueven de forma casi independiente los unos de los otros.

La repulsión electrostática entre los electrones, sin embargo, tiene un efecto secundario, más sutil. De la misma manera que un pasajero de autobús evita sentarse al lado de otros pasajeros y toparse con ellos a medida que camina por el pasillo, los electrones tratan de evitarse el uno al otro cuando se mueven en el interior de un átomo o una molécula; el movimiento de los electrones se dice que está correlacionado. De este modo, los electrones minimizan su repulsión mutua y, como consecuencia, estabilizan el átomo o molécula a la que pertenecen. Dicha estabilización es responsable del balance energético de todos los procesos naturales, y es clave para nuestra comprensión y control del comportamiento de la materia, como la transferencia de energía en sistemas fotosintéticos, la protección de datos en los futuros ordenadores cuánticos, etcétera. A pesar de ello, el movimiento de dos electrones correlacionados ha eludido la observación experimental directa hasta el momento presente. Además, es muy difícil de reproducir teóricamente, ya que, incluso para el átomo de helio, que es el sistema más simple con dos electrones, las ecuaciones físico-cuánticas que describen este movimiento no pueden resolverse exactamente y, en su lugar, deben realizarse costosos cálculos numéricos en superordenadores.
Para poder tomar en cuenta la indistinguibilidad de los dos electrones del helio siguiendo las reglas de la Mecánica Cuántica, lo cual requiere que en una …
Esta semana, en la revista Nature, los investigadores teóricos de la Universidad Autónoma de Madrid, Luca Argenti y Fernando Martín, en colaboración con el grupo experimental de Thomas Pfeifer, del Instituto Max Planck de Heidelberg, explicamos cómo hemos reconstruido por primera vez el movimiento simultáneo de dos electrones excitados en el helio, a partir de datos experimentales y cálculos de física cuántica inéditos. Hemos utilizado una versión de alta resolución de una técnica conocida como espectroscopia de absorción transitoria de attosegundos, mediante la cual se midió la transparencia de una muestra de helio a destellos cortos de luz ultravioleta en función del tiempo transcurrido entre este destello y otro de luz roja generado por un láser de titanio-zafiro.

Al igual que un adulto empuja a un niño en un columpio, el pulso ultravioleta lleva el átomo a un estado excitado, donde ambos electrones oscilan. Actuando de manera adecuada, las piernas de los niños pueden amplificar o amortiguar las oscilaciones del columpio. Y midiendo la amplitud de dichas oscilaciones se puede deducir el punto en el que el niño movió las piernas, es decir, reconstruir el movimiento original del columpio. De una manera similar, en el experimento, el pulso de luz roja fortalece o debilita la absorción de la luz ultravioleta en función del tiempo transcurrido entre los dos pulsos. A partir de la modulación de la absorción ultravioleta, hemos logrado reconstruir la oscilación de los dos electrones, y de ahí deducir la evolución del correspondiente paquete de ondas. Más allá del seguimiento de este movimiento, también pudimos modificarlo y controlarlo aumentando la intensidad del pulso rojo. Volviendo a la analogía del columpio, es como si el niño estuviera, además, sujetando una cometa: un fuerte golpe de viento alteraría por completo la oscilación del columpio.
Con este trabajo, consideramos que hemos abierto el camino para la observación directa del movimiento electrónico correlacionado en átomos y moléculas, y quizá para controlar el movimiento de los electrones apareados en enlace químicos, lo que permitiría la producción de sustancias que no pueden ser obtenidas con procedimientos químicos convencionales.
Luca Argenti y Fernando Martín son investigadores teóricos del Departamento de Química de la Universidad Autónoma de Madrid
















 Totales: 72.364.480
Totales: 72.364.480 Conectados: 42
Conectados: 42