Dic
26
Cosas que nos gusta conocer
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)
En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es:
H, He, (Li, Be, B) C, N, O… Fe
¿Apreciáis la maravilla? Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del universo y… de la vida inteligente.

Pero está claro que todo el proceso estelar evolutivo inorgánico nos condujo desde el simple gas y polvo cósmico a la formación de estrellas y nebulosas solares hasta los planetas, la Tierra en particular, en cuyo medio ígneo describimos la formación de las estructuras de los silicatos, desplegándose con ello una enorme diversidad de composiciones, formas y colores, asistiéndose, por primera vez en la historia de la materia, a unas manifestaciones que contrastan con las que hemos mencionado en relación al proceso de las estrellas.
Desde el punto de vista del orden es la primera vez que nos encontramos con objetos de tamaño comparables al nuestro, en los que la ordenación de sus constituyentes es el rasgo más característico.

Al mismo tiempo nos ha parecido reconocer que esos objetos, es decir, sus redes cristalinas “reales”, almacenan información (memoria) que se nos muestra muy diversa y que puede cobrar interés en ciertos casos, como el de los microcristales de arcilla, en los que, según Cairns-Smith, puede incluso llegar a transmitirse.
Porque, ¿qué sabemos en realidad de lo que llamamos materia inerte? Lo único que sabemos de ella son los datos referidos a sus condiciones físicas de dureza, composición, etc; en otros aspectos ni sabemos si pueden existir otras propiedades distintas a las meramente físicas.
¿No os hace pensar que nosotros estemos hechos, precisamente, de lo que llamamos materia inerte?
Pero el mundo inorgánico es sólo una parte del inmenso mundo molecular. El resto lo constituye el mundo orgánico, que es el de las moléculas que contienen carbono y otros átomos y del que quedan excluidos, por convenio y características especiales, los carbonatos, bicarbonatos y carburos metálicos, los cuales se incluyen en el mundo inorgánico.
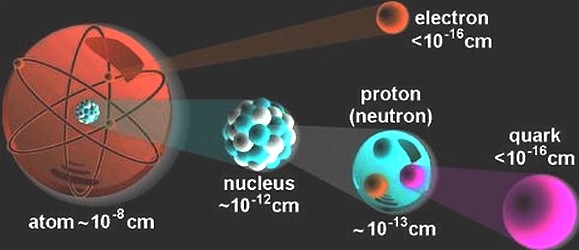
Según he podido explicar en muchos otros trabajos, los quarks u y d se hallan en el seno de los nucleones (protones y neutrones) y, por tanto, en los núcleos atómicos. Hoy día, éstos se consideran como una subclase de los hadrones.
La composición de los núcleos (lo que en química se llama análisis cualitativo) es extraordinariamente sencilla, ya que como es sabido, constan de neutrones y protones que se pueden considerar como unidades que dentro del núcleo mantienen su identidad. Tal simplicidad cualitativa recuerda, por ejemplo, el caso de las series orgánicas, siendo la de los hidrocarburos saturados la más conocida. Recordad que su fórmula general es , lo que significa que una molécula de hidrocarburo contiene n átomos de carbono (símbolo C) y (2n+2) átomos de hidrógeno (símbolo H).
El número de protones y neutrones determina al elemento, desde el hidrógeno (el más simple), al uranio (el más complejo), siempre referido a elementos naturales que son 92; el resto son artificiales, los conocidos transuránicos en cuyo grupo están el einstenio o el plutonio, artificiales todos ellos.
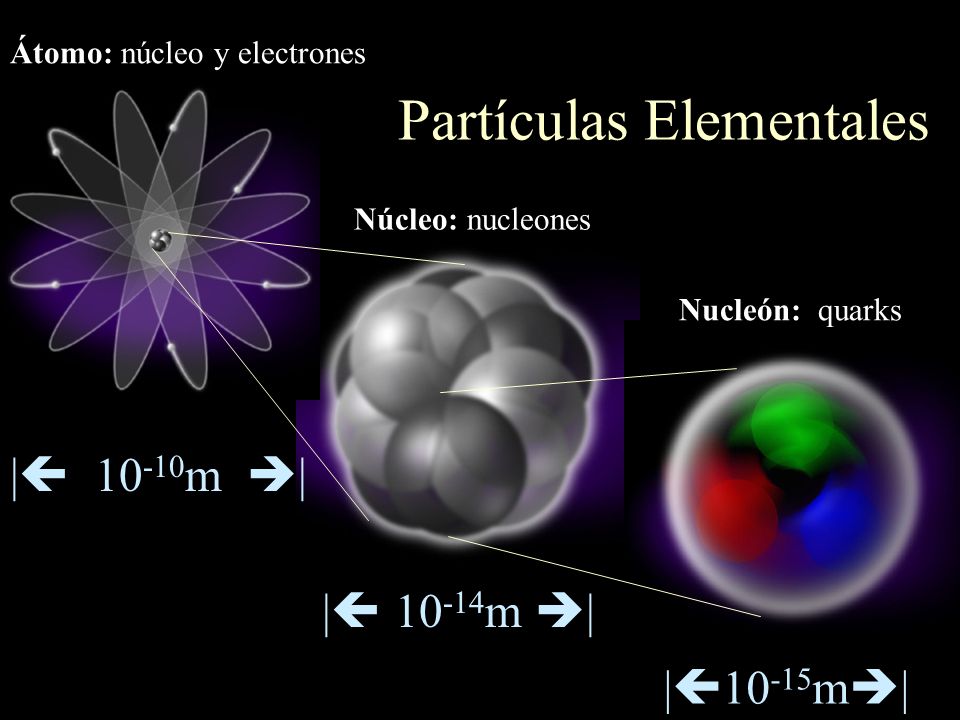
Los núcleos, como sistemas dinámicos de nucleones, pertenecen obviamente a la microfísica y, por consiguiente, para su descripción es necesario acudir a la mecánica cuántica. La materia, en general, aunque presumimos de conocerla, en realidad, nos queda mucho por aprender de ella.
Hablemos un poco de moléculas.
El número de especímenes atómicos es finito, existiendo ciertas razones para suponer que hacia el número atómico 173 los correspondientes núcleos serían inestables, no por razones intrínsecas de inestabilidad “radiactiva” nuclear, sino por razones relativistas. Ya antes me referiría a las especies atómicas, naturales y artificiales que son de unos pocos millares; en cambio, el número de moléculas conocidas hasta ahora comprende varios millones de especímenes, aumentando continuamente el número de ellas gracias a las síntesis que se llevan a cabo en numerosos laboratorios repartidos por todo el mundo.
Una molécula es una estructura con individualidad propia, constituida por núcleos y electrones. Obviamente, en una molécula las interacciones deben tener lugar entre núcleos y electrones, núcleos y núcleos y electrones y electrones, siendo del tipo electromagnético.
Debido al confinamiento de los núcleos, el papel que desempeñan, aparte del de proporcionar la casi totalidad de la masa de la molécula, es poco relevante, a no ser que se trate de moléculas livianas, como la del hidrógeno. De una manera gráfica podríamos decir que los núcleos en una molécula constituyen el armazón de la misma, el esqueleto, cuya misión sería proporcionar el soporte del edificio. El papel más relevante lo proporcionan los electrones y en particular los llamados de valencia, que son los que de modo mayoritario intervienen en los enlaces, debido a que su energía es comparativamente inferior a la de los demás, lo que desempeña un importante papel en la evolución.
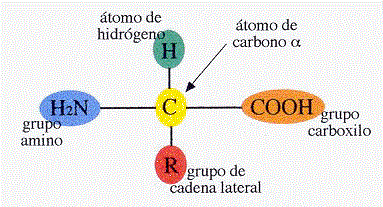
Estructura de los aminoácidos
Desde las moléculas más sencilla, como la del hidrógeno con un total de 2 electrones, hasta las más complejas, como las de las proteínas con muchos miles de ellos, existe toda una gama, según decía, de varios millones. Esta extraordinaria variedad de especies moleculares contrasta con la de las especies nucleares e incluso atómicas.
Sin entrar en las posibles diferencias interpretativas de estas notables divergencias, señalaré que desde el punto de vista de la información, las especies moleculares la poseen en mucho mayor grado que las nucleares y atómicas.
Dejando aparte los núcleos, la información que soportan los átomos se podría atribuir a la distribución de su carga eléctrica, y en particular a la de los electrones más débilmente ligados. Concretando un poco se podría admitir que la citada información la soportan los orbitales atómicos, pues son precisamente estos orbitales las que introducen diferencias “geométricas” entre los diferentes electrones corticales.

La forma en que son ocupados los electrones de un átomo en su estado fundamental o basal ocuparán los niveles de más baja energía posible, de acuerdo con el Principio de exclusión de Pauli. Por tanto, para escribir la configuración electrónica de un elemento, se deben seguir ciertas reglas.
Justamente esa información es la que va a determinar las capacidades de unión de unos átomos con otros, previo el “reconocimiento” entre los orbitales correspondientes. De acuerdo con la mecánica cuántica, el número de orbitales se reduce a unos pocos. Se individualizan por unas letras, hablándose de orbitales s, p, d, f, g, h. Este pequeño número nos proporciona una gran diversidad.
La llamada hibridación (una especie de mezcla) de orbitales es un modo de aumentar el número de mensajes, esto es, la información, bien entendido que esta hibridación ocurre en tanto y en cuanto dos átomos se preparan para enlazarse y formar una molécula. En las moléculas, la información, obviamente, debe abarcar todo el edificio, por lo que en principio parece que debería ser más rica que en los átomos. La ganancia de información equivale a una disminución de entropía; por esta razón, a la información se la llama también negantropía.
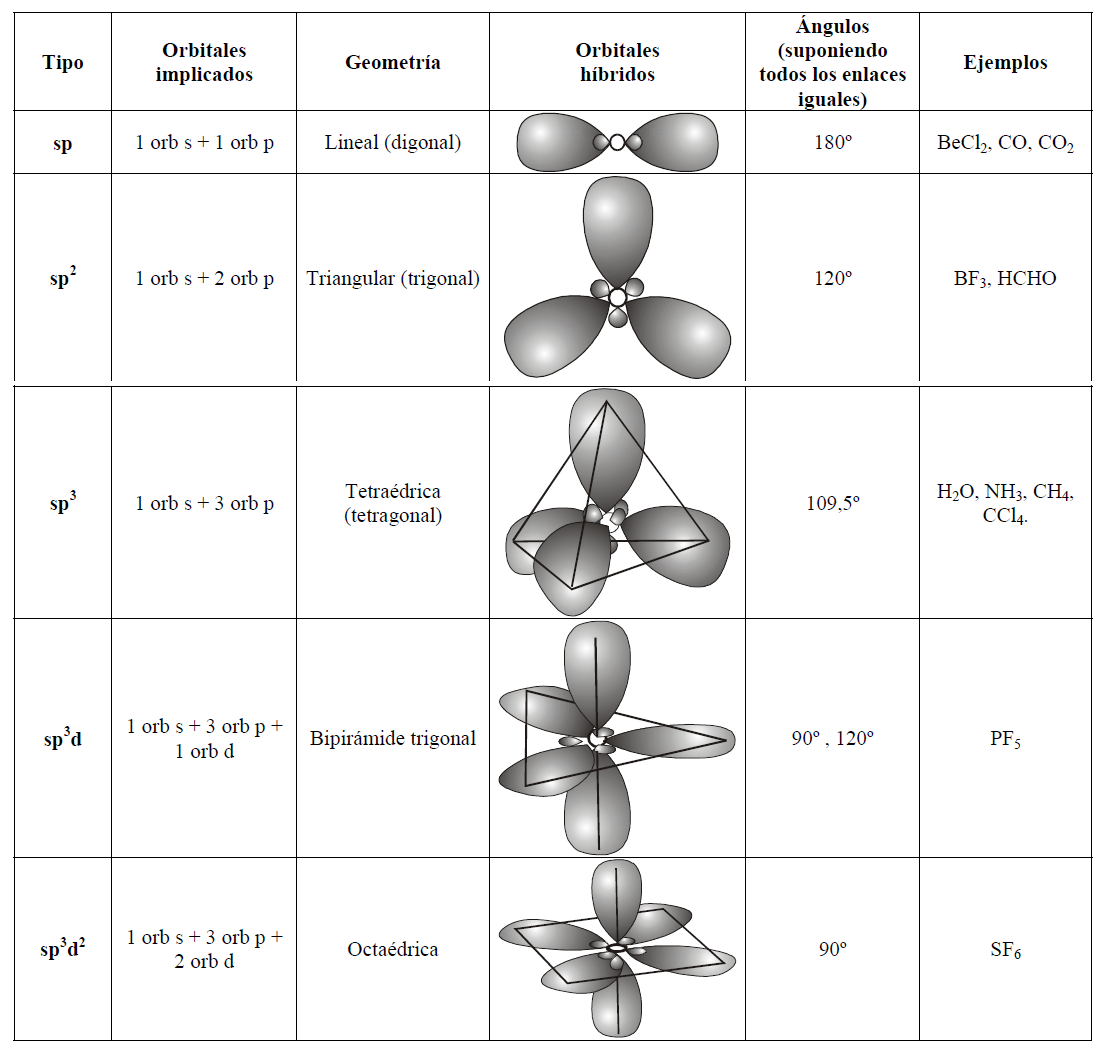
En términos electrónicos, la información se podría considerar proporcionada por un campo de densidad eléctrica, con valles, cimas, collados, etc, es decir, curvas isoelectrónicas equivalentes formalmente a las de nivel en topografía. Parece razonable suponer que cuanto más diverso sean los átomos de una molécula, más rica y variada podrá ser su información, la información que pueda soportar.
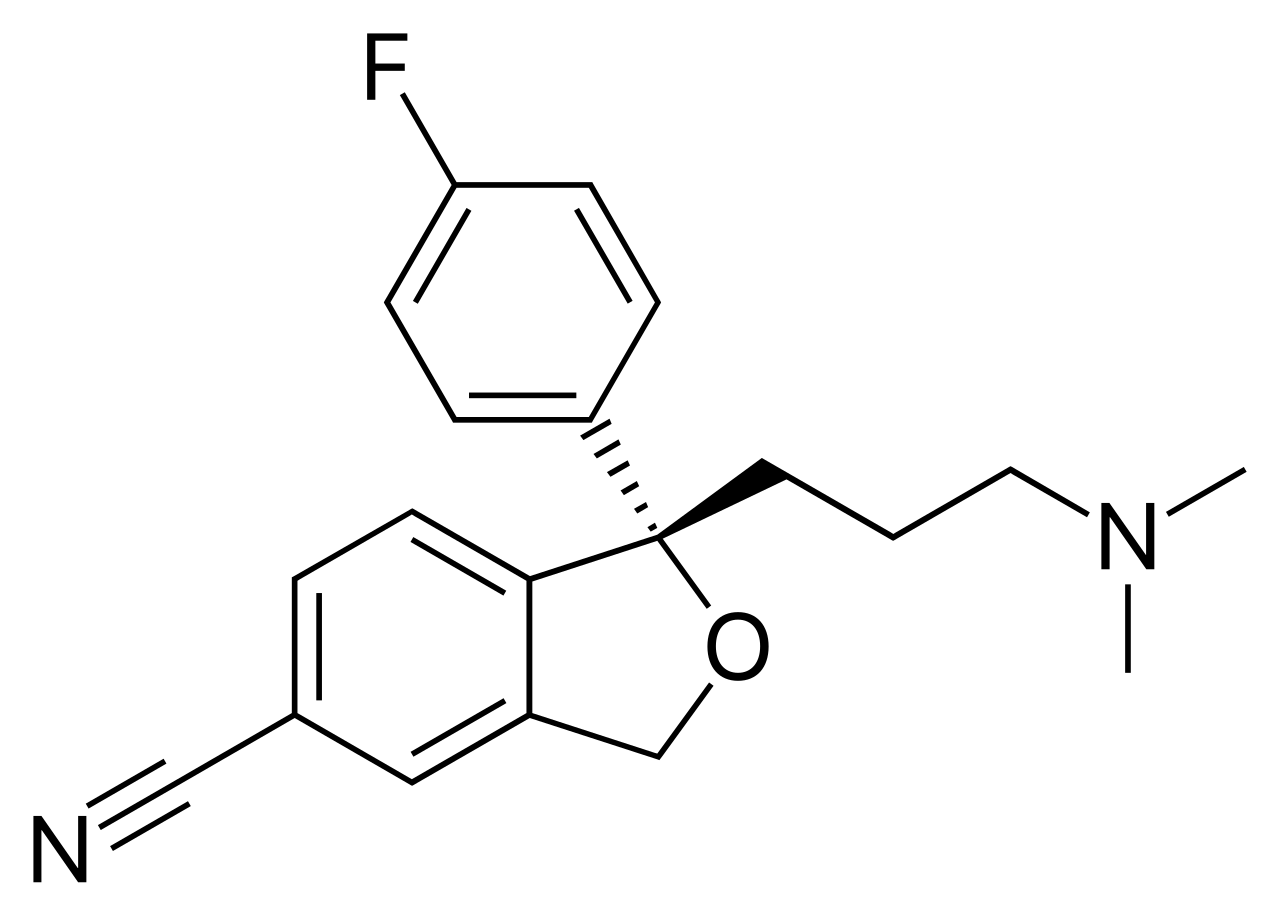
La enorme variedad de formas, colores, comportamientos, etc que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetravalencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.
El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor.
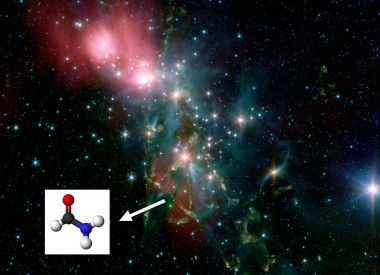
“Los ladrillos básicos de la vida flotan en el espacio: son moléculas orgánicas, forjadas en el interior de frías y espesas nubes de gas y polvo. Materiales que, gracias a los ciclos vitales de las estrellas, terminan desparramándose por todas partes, “contaminando” el medio interestelar. Y con un poco de suerte, pueden incorporarse a la materia prima que dará origen a nuevos soles y planetas. Durante las últimas décadas, los telescopios y radiotelescopios han detectado la presencia de estas estructuras, basadas en el carbono, en varios rincones de nuestra galaxia. Sin embargo, también se han descubierto distintas clases de moléculas orgánicas en nuestra vecindad más inmediata: hay montones de cometas, asteroides y satélites del Sistema Solar salpicados por esos compuestos químicos. Son los mismos que, día a día, y sin que nos demos cuenta, “llueven” sobre la Tierra, a bordo de partículas rocosas y meteoritos. Y todo indica que esa lluvia orgánica fue tremendamente más intensa durante la violenta infancia del planeta, hace más de 4000 millones de años. Es más, el primigenio aporte cósmico podría extenderse –vía cometas- incluso al agua, socia inseparable de la biología.”
“Las primeras pistas sobre la presencia de moléculas orgánicas cósmicas llegaron en 1937, con la detección (mediante espectroscopia) de combinaciones simples de átomos de hidrógeno y carbono en masas gaseosas del medio interestelar. El siguiente hito se hizo esperar, pero valió la pena: a fines de los ´60, y mediante técnicas de radioastronomía, se descubrieron moléculas de agua y amoníaco (NH3). La cosa iba tomando color. Sin embargo, había un problema: la radiación ultravioleta de las estrellas difícilmente permitiría la formación de moléculas más complejas. Por lo tanto, si efectivamente existían, esas moléculas debían forjarse en ambientes protegidos. Y qué mejor que buscarlas en el interior de las densas, opacas y frías nubes de hidrógeno molecular (H2) que se esconden en las grandes nebulosas. Allí, los átomos de oxígeno, carbono, o nitrógeno (forjados en el interior de estrellas que, al morir, los devolvieron al espacio) pueden combinarse tranquilamente con los de hidrógeno, formando un amplio repertorio de moléculas, entre ellas, largas cadenas de hidrocarburos (combinaciones de hidrógeno y carbono), y todo un surtido de nitrilos (formados por carbono y nitrógeno), compuestos que son especialmente importantes desde el punto de vista biológico (ciertos nitrilos, por ejemplo, pueden reaccionar con agua líquida, dando lugar a aminoácidos, los bloques químicos que forman parte de las proteínas y ácidos nucleicos). “

Acordáos de cuando publiqué aquella noticia de que Astrónomos de la NASA habían logrado descubrir las esquivas moléculas de carbono en el espacio, conocidas por los especialistas como “Buckyball”. Las Buckyball son moléculas que tienen la forma de un balón de fútbol y fueron observadas por primera vez en un laboratorio hace ahora cerca de 30 años. Su nombre se debe a que su forma recuerda a las cúpulas geodésicas diseñadas por el arquitecto Buckminster Fuller, las que se caracterizan por círculos entrelazados en la superficie de una esfera parcial.
Lo dicho, la Naturaleza nunca dejará de asombrarnos.
Emilio Silvera
















 Totales: 72.403.607
Totales: 72.403.607 Conectados: 53
Conectados: 53